Материал: Модифікування полісульфонових мембран з альфа-амілазою, інкорпорованою в полімерні міцели
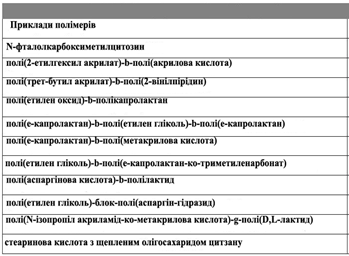
Табл.2 Амфіфільні кополімери, що були досліджені для утворення міцел
.2.4 Полімерні міцели, чутливі до факторів навколишнього середовища
Мікросередовище-основний фактор, який впливає на утворення міцел та їх стабільність. Два основні методи міцелізації - це діаліз і випаровування співрозчинника. У першому методі полімер розчиняють у органічному розчиннику ,який потім забирають діалізом з водного буферу. У другому методі полімер розчиняють у суміші органічного та водного розчинників, органічний розчинник потім забирають розпилюючим сушінням або у роторному випарнику. Щоб продемонструвати залежність міцелізації від препараційного методу, були проведені дослідження,які показали, що міцели приготовані цими двома способами мають істотну різницю у розмірах і розподілі як було визначенодинамічним лазерним розсіюванням світла. Міцели, приготовані випаровуванням співрозчинника були менші (приблизно 30 нм) і більш рівномірні за індексом полідисперсності (ПІ), який становив 0,07, в той час як міцели отримані діалізом були більші(приблизно 110нм) і більш дисперсними з ПІ=0,27. Важають, що різниця у розмірах залежить від шляху утворення і може бути результатом змін у темпі досягнення рівноваги . Відмінність у розмірах міцел, яка базується на препараційному методі цікаве питання для дослідження. Дослідження цього питання показало , що навіть малі зміни (температури, зміни молекулярної маси відрізку діалізної мембрани) у препараційному методі мають сильний вплив на розмір міцел [30].
Зміни у умовах розчинення мають відчутний вплив на ККМ та розмір міцел,які формуються. Дослідження утворення полі(молочної-ко-гліколевої кислоти)-полі(етилен гліколевих) міцел проводили у розчинниках різного складу змінюючи тип і концентрацію органічного розчиннику для солюбілізації полімерного ланцюга для даної розчиннико-водної системи.Чотири різні розчинники з різним ступенем змішування з водою -ТГФ(тетра-гідрофуран), ДМФ(диметилформамід),ацетон та ацетонітрил-використовувались у дослідженні. Результати показують основне співвідношення між змішуванням води і розчинника та розміром міцели ,де збільшення змішування призвело до зменшення розмірів міцел. Такі ж результати були отримані при дослідженні впливу вибору розчинника на розмір та дисперсність міцел, сформованих з метокси полі(етилен оксид)-блок-полі-капролактан [31]. Використання ацетону як органічного розчинника веде до утворення міцел з діаметром 87,8±9,4 нм із відносно рівномірним розподілом з індексом полідисперсності =0,11. На відміну від ацетону, при використанні ТГФ у якості органічного розчинника утворені міцели були більшого розміру ,приблизно 109±29 нм і також були більш дисперсними ,їхній індекс полідисперсності становив 0,52. Обидва з вищезазначених прикладів дали прекрасні рекомедації для вибору співрозчинника при міцелізації.
Вплив температури на внутрішньо-міцелярні рухи ланцюга. Наприклад, полі-DL-лактидне ядро полі-(етилен гліколь)-полі-DL-лактидної міцели стало більш мобільним при температурах вище температури склування. Як результат ККМ зростає при більшій температурі, що демонструє залежність впливу температури на термодинамічну стабільність.
Міцелоутворення -
вкрай чутливий процес сприйнятливий до впливів багатьох внутрішніх і зовнішніх
чинників. Навіть коли формується стабільна міцела ,можуть бути ускладнення при
ліофілізації, які виникають, при недостатньому охопленні ПЕГу або інших
гідрофільних компонентів[32].
.3 Концентраційна поляризація
.3.1 Модель гель-поляризації
Першою запропонованою моделлю ,яка б пояснювала ефекти концентраційної поляризації при ультрафільтрації(UF),була модель гель-поляризації[33].Основним припущенням цієї моделі було те, що вище певного значення рабочого тиску , швидкість проникненя мембрани обмежує наявність гель-шару, який нанесений на поверхню мембрани ,який збільшує ефективну товщину мембрани і , таким чином, знижує її гідравлічну проникність. Наступним припущенням, яке виконується в традиційній версії цієї моделі, було те, що осмотичні тиски високомолекулярних розчинів завжди незначні. Пізніше, деякі дослідники відзначили, що це припущення не є цілком правильним:концентрація макромолекул може мати значний осмотичний тиск ;насправді , осмотичний тиск може бути того ж порядку , що й робочий(прикладений) тиск ,який використовують при ультрафільтрації.[34].
У 1970 році Майкл та його колеги
[35] запропонував перший всебічний аналіз концентраційної поляризації при UF
і ввів термін "гель-поляризаця". Якщо припустити, що граничний опір
потоку знаходиться в динамічно сформованому вторинному або гель-шарі , можливо
розрахувати швидкість водопроникності мембрани (потік) на основі масопереносу
мембранно-фіксованих зразків (розведені розчини або колоїдні матеріали) з
поверхні мембрани в основний потік [36] (рис.2). Тому що
динамічний шар гелю , як передбачається, повинен мати фіксовану концентрацію
гелю (Сg),
але може вільно змінюватися залежно від товщини або пористості (різної
проникості або опору потоку). При такому аналізі, потік розчинника (Jv)
не буде залежати від сили ,яка керована тиском або проникності мембрани,
оскільки опір гель-шару потоку буде налаштовуватись сам-по-собі, доки
конвекційний транспорт розчинником нерозподіленого зразку до поверхні мембрани
(JvC)
якраз дорівнює зворотньо-дифузійному транспорту [D(dC/dx)](Рис.2).

Рис.2. Схематичне зображення концентраційної
поляризації.
Таким чином, у стабільному стані:
![]()
Де D-це коефіцієнт дифузії для транспорту розчиненої речовини у розчиннику, С-концентрація мембранно-фіксованої розчиненої речовини або колоїдного зразку і dC/dx -градієнт концентрації розчиненої речовини.
Модель гель-поляризації [Eq.(1)]
може бути змінена, якщо задані граничні умови;концентрація розчиненої речовини
блія поверхні мембрани фіксується верхньою границею (насиченням
,Сg ),
і об’ємна концентрація
потоку відома( Cg ).
Тоді,

Дослідження Fluid
Management бути спрямовані на зменщення товщини примембранного шару , або ,
інакше кажучи, у бік збільшення коефіцієнта масопереносу, k,
де

Справедливість рівняння (3) була
продемонстрована для великої кількості високомолекулярних розчинів і колоїдних
зразків. Масопереносо-теплопереносні аналогії добре відомі у хімічній
інженерній літературі , зробили можливим оцінку коефіцієнта масопереносу та
забезпечення розуміння будови мембрани та умов рідинного потоку ,які можуть
бути задані для оптимізації потоку.
1.3.2 Модель осмотичного тиску
Обмеження потоку в моделі осмотичного тиску
розглядається як такий, що виникає через збільшений осмотичний протитиск ,
викликаний високою концентрацією розчиненої речовини у білямембранному
просторі.[37].Одна з
моделей осмотичного тиску це модель Spiegler-Kedem та розчинно-дифузійна модель
.Робочі рівняння цієї моделі [38]
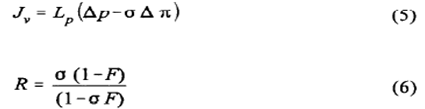
Де ![]()
та![]()
де R
справжнє відхилення(rejection) Δp
падіння тиску при проходженні через мембрану , Δπ-падіння
осмотичного тиску при проходженні через мембрану , σ-коефіцієнт
відбиття, який зображує відхиляючу здатність мембрани ,(тобто якщо σ=0
, це
означає ,що немає відхилення і якщо σ=1-це
означає 100% відхилення ) і Pm
-загальний
коефіцієнт проникнення. Комбінуючи рівняння (5) та (8) з теоретичною моделлю
[рівняння (2)] дають
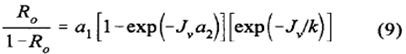
де α1=σ/(1-σ).
Використовуючи нелінійний метод оцінки параметрів та експериментальні дані
спостереженого відхилення (R0)
і потік розчинника (Jv
) взяті при певному тиску , шидкості подачі і
концентрації, параметри мембрани σ
та Рм , і k
можна вирахувати разом.
.3.3 Коефіцієнт масопереносу
Більшість моделей, які використовуються для характеристики зворотнього осмосу та ультрафільтрації мембран , такі як осмотично-тискова модель трьох параметрів (Spiegler-Kedem модель) та модель (гель) концентраційної поляризації, використовують коефіцієнт масопереносу для того, щоб підрахувати концентрацію біля мембранної стінки , Сw .
Це співвідношення емпіричнобазоване
по Chilton-Colburn
аналогії [39,40].
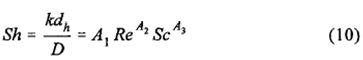
де Sh
-число Шервуда , dn-гідравлічний
діаметр каналу потоку, А1 до А3-емпіричні константи , Re
-число Рейнольдса і Sc
-число Шмідта . Основане на Chilton-Colburn
та Deissler
аналогії , рівняння (10) можна комбінувати з рівнянням film
theory
(тобто,гель-шару) [рівняння (3)], щоб отримати

Дозволяє підрахувати Cw , коли k-відомий.
Вищевказані співвідношення запозичені з рівнянь
для непористого гладкого канального потоку . Їхнє застосування у випадку
мембранних операції було критиковане багатьма авторами оскільки ні пористість
,ні дифузійність через концентраційну поляризацію не беруться до уваги .
and
Hallstrom
[41] оприлюднили чудий огляд по адаптації існуючого рівняння Шервуда до мембранний
операцій під турбулентним канальним потоком. Їхня робота включала обговорення
факторів , які впливають на масоперенос під час зворотнього осмосу або
ультрафільтрації , таких як пористість і жорсткість мембранної стінки та зміна
коефіцієнта в’язкості та дифузії через сильний концентраційний градієнт. Вони
відзначили, що багато з рівнянь представлених в літературі за багатьох умов та
типів рідин у турбулентній області мають асимптотичну форму (Re
>10,000 та Sc
>100)
![]()
де m=1 або ½ . Залежність числа Шервуда від фактору тертя (f) являється функцією від типу експерименту і постановляє, що формула Бласіуса , яка співвідносить f з Re , є в основному більш прийнятною. Як-не-як , у випадку мембранних операцій керованих тиском , виявлено ,що f залежить від пористості та жорсткості стінки , та від потоку пермеату. Проміжок 2,300<Re <10,000 не є чистим , і нема простого рівняння Шервуда для цього проміжку.
Проблема оцінки коефіцієнту масопереносу ,k, при зворотньому осмосі є дуже важливою. Було винайдено безліч методів, та використання прямих вимірювань, використовуючи оптичні та мікро-електродні методи , непрямих вимірювань, у яких дійсне відхилення підраховується екстраполяцією нескінченної кривої циркуляції, а також непрямі вимірювання , в яких модель концентраційної поляризації комбінована з моделлю мембранного транспорту використовується для підрахунку коефіцієнту масопереносу [33].
РОЗДІЛ 2. ЕКСПЕРИМЕНТАЛЬНА
ЧАСТИНА
.1 Об’єкти та матеріали дослідження
В роботі були використані промислові
полісульфонові мембрани UF-PES-030H
(Mіcrodyn
Nadir,
Німеччина) з cut of
30 000 Да.
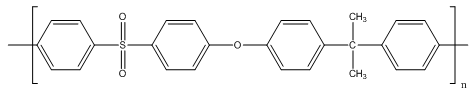
Рис. 2.1.
Структурна формула полісульфону
Для модифікування мембрани використовували :
- Synperonic
F 108 -
поліетиленгліколь-блок-поліпропіленгліколь-блок- поліетиленгліколь
(б-ПЕГ-б-ППГ-б-ПЕГ), молекулярна маса якого 2250 (Fluka,
Франція):
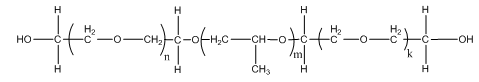
Рис. 2.2.
структурна формула поліетиленгліколь-блок-поліпропіленгліколь-блок- полі
етиленгліколю
- як модельний фермент використовували α-амілазу з Bacillus subtilis (Fluka, Швейцарія).
Даний фермент бере участь в
гідролізі α-зв’язків
полісахаридів, таких як крохмаль і глікоген, що в результаті перетворюються на
глюкозу і мальтозу. α-амілаза
- це основна форма даного типу ферментів, знайдена в людському організмі та в
організмах інших ссавців, в яких її секреція відбувається за рахунок роботи
слинних залоз та підшлункової залози. Вона також міститься в зернах крохмалю та
синтезується декількома видами грибів.
Рис. 2.3.
Модель структури α-амілази
Для перевірки активності α-амілази використовували:
- крохмаль водорозчинний (Міранда, Україна);
- KI (Міранда, Україна);
- I2 (Міранда, Україна).
Для визначення ККМ ПАР
використовували барвник Судан ІІІ (Sigma-Aldrich,
США).
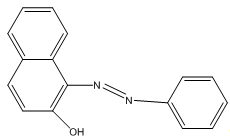
Рис. 2.4.
Структурна формула Судану ІІІ
.2 Прилади та обладнання
аналітичні терези лабораторні 2 класу моделі ВЛР-200 г (100 мг - 900 мг);
ваги електронні AD-200 (AXIS, Польща);
магнітна мішалка IKA ® C-MAG HS 7;
рН-метр-мілівольтметр рН-150МА;
- спектрофотометр UV-1200 (LAB instech);
- термостат Incucell (BMT, Чехія);
- ультрафільтраційна комірка
непроточного типу Amicon
8050 (Milipore,
США).
.3 Методики модифікації мембран та дослідження їхніх транспортних та каталітичних властивостей
мембрана випромінювання модифікація каталітичний
2.3.1 Методика визначення критичної концентрації міцелоутворення поверхнево-активних речовин
Критичну концентрацію міцелоутворення (ККМ) блок-кополімеру визначали фотометричним методом
Для цього готували серію розчинів
поліетиленгліколю-блок-поліпропіленгліколь-блок-поліетиленгліколь з
концентраціями від 4·10-3 до 4·10-2 %. До одержаних
розчинів додавали барвник Судан-ІІІ, після чого струшували протягом доби. Після
солюбілізації барвника розчини відфільтровували та вимірювали значення оптичної
густини при 540 нм. ККМ розраховували з графіку залежності опичної
густини від концентрації розчину.
.3.2 Методика модифікування полісульфонових мембран полімерними міцелами
Для модифікації використовували промислові мембрани з полісульфону Microdyn-Nadir UF-PES-030H. Готували розчин 0,1% ПАР з 1мг/мл -α-амілази.
Розчин залишали струшуватись
протягом доби для вбудовування ферменту в структуру міцели. Іммобілізацію міцел
проводили адсорбцією з розчинів протягом 30 хв. Модифіковані мембрани відмивали
у дистильованій воді протягом 20 діб.
.3.3 Методика пришивання полімерних міцел до полісульфонових мембран
Прищеплення полімерних міцел з
ферментом до поверхні мембран здійснювали за допомогою УФ-опромінення при
довжині хвилі 254 нм в комірці для УФ-ініційованого прищеплення (рис.
2.5). Час опромінювання варіювали у межах від 1 до 5 хв.
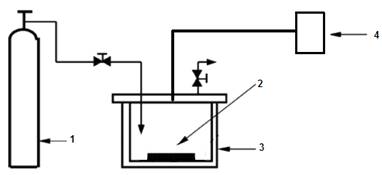
Рис. 2.5.
Комірка для УФ-ініційованого прищеплення: 1 - балон із аргоном, 2 - мембрана, 3
- кварцова комірка, 4 - джерело УФ-опромінення.
.3.4 Визначення транспортних характеристик мембран
Для визначення розділювальних
характеристик мембран (проникності та розділювальної здатності) використовували
стандартну циліндричну комірку непроточного типу Amicon
8050, (виробництво Millipore,
США). Всі
елементи комірки, що контактують з розчинами, виготовлені з некородуючих
матеріалів. Схематично установка непроточного типу представлена на рис.
2.6.
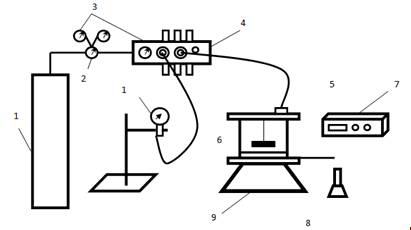
Рис. 2.6. Схема
ультрафільтраційної установки непроточного типу: 1 - балон зі стиснутим азотом;
2 - газовий редуктор; 3 - манометри; 4 - розподілювач газу; 5 - мембранна
комірка; 6 - мембрана; 7 - індикатор швидкості обертання пристрою для
перемішування (строботахометр); 8 - збірник фільтрату; 9 - магнітна мішалка; 10
- манометр.
Внутрішній об‘єм комірки складав 50 мл, площа робочої поверхні мембрани - 13,4·10-4 м2, робочий тиск від 50 до 350 кПа. Для зниження впливу концентраційної поляризації на процеси розділення комірка обладнана магнітною мішалкою. Швидкість обертання мішалки складала 200±10 об/хв. Досліди з ультрафільтрації проводили при 293±2 К. Робочий тиск у комірці задавали за допомогою стисненого азоту.