Материал: Методическое пособие. Общая микробиология
д) Метод флуоресцирующих антител основан на появлении специфического свечения в местах локализации вируса при обработке зараженной ткани флуоресцирующими антителами. Заражаемую культуру ткани выращивают на стеклянных пластинках. Препарат промывают физиологическим раствором, подсушивают и фиксируют в ацетоне при 4°С в течение 10 мин. Затем препарат окрашивают специфической флуоресцирующей сывороткой в течение 30 мин при 37°С. После окраски препарат промывают физиологическим раствором и высушивают. Просмотр препарата производят с помощью люминесцентного микроскопа.
2. а) Вскрытие куриных эмбрионов. Работу проводят в стерильных условиях. Яйцо ставят воздушным мешком кверху, место вскрытия смазывают спиртом, йодом, еще раз спиртом, обжигают, снимают колпачок и ножницами удаляют прилегающую к отверстию часть скорлупы. Пинцетом снимают подскорлупную оболочку, прокалывают пастеровской пипеткой хорионаллантоисную оболочку и из полости отсасывают аллантоисную жидкость, содержащую вирус. Жидкость помещают в стерильную пробирку.
Для исследования хорионаллантоисной оболочки из яйца удаляют всё содержимое. Оболочка остается на внутренней поверхности скорлупы или выпадает вместе с содержимым яйца. Оболочку осторожно вынимают пинцетом, помещают в чашку Петри, промывают физиологическим раствором, тщательно расправляют и рассматривают на темном фоне изменения, имеющиеся в ней. Изменения на оболочке строго специфичны. Например, вирус осповакцины вызывает образование многочисленных беловатых втянутых в центре бляшек.
б) Реакция гемагглютинации. Аллантоисную жидкость проверяют на содержание вируса путем агглютинации куриных эритроцитов на стекле (и в пробирках - титрование вируса). Для постановки реакции на стекле к капле вируссодержащего материала добавляют одну каплю 5% взвеси эритроцитов. Реакция проходит в течение 5 мин.
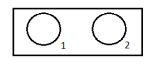
Реакция гемагглютинации
|
|
1 – опыт (к капле аллантоисной жидкости, содержащей вирус гриппа, добавляют каплю 5% взвеси куриных эритроцитов) 2 – контроль (эритроциты + физ. р-р). |
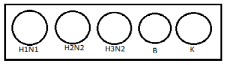
Схема определения типа вируса реакцией торможения гемагглютиниции.
|
|
В каплю вируссодержащей жидкости добавляют каплю типовой сыворотки и каплю 5% взвеси эритроцитов. К– контроль (эритроциты + физ. раствор). |
|
Заключение:__________________________________________________________ _____________________________________________________________________
|
|
Контрольные вопросы
Как обнаруживают наличие вируса в культуре ткани?
Почему при размножении вируса цвет среды не изменяется?
С какой целью может быть использован метод цветных проб?
Какие изменения наступают в клетках при размножении вируса?
Как ставят реакцию гемадсорбции? Как выглядит положительная реакция гемадсорбции?
Что собой представляет метод бляшек?
Как обнаруживают вирус гриппа в курином эмбрионе?
Как вскрывают зараженный эмбрион?
Почему происходит реакция агглютинации эритроцитов в присутствии вируса гриппа? Каков механизм этой реакции?
Что такое реакция торможения (нейтрализация) гемагглютинации? Для чего она используется?
Как обнаруживают изменения в хорионаллантоисной оболочке, вызванные вирусом?
Приложение к ЗАНЯТИЮ 9.
Классификация цитопатического действия (ЦПД) вирусов в культуре ткани.
1. Равномерная мелкозернистая деструкция клеток (вирусы Коксаки, ЕСНО, полиовирусы).
2. Очаговая мелкозернистая дегенерация (вирусы гриппа, клещевого энцефалита и др.).
3. Гроздевидная дегенерация (аденовирусы).
4. Крупнозернистая равномерная деструкция (вирус герпеса).
5. Симпластообразование (обезьяньи вирусы, вирусы кори, осповакцины, RS-вирус).
Методы обнаружения вируса в культуре ткани
1. Цитопатический эффект.
2. Реакция гемадсорбции.
3. Метод цветных проб.
4. Метод бляшек.
5. Иммунофлуоресцентный метод.
6. Реакция связывания комплемента.
7. Реакция гемагглютинации.
8. Заражение животных, восприимчивых к данному вирусу.
9. Реакция преципитации в агаре.
Методы определения типа вирусов (идентификация, типирование вирусов)
Определение типа вирусов в вируссодержащем материале основано на реакции нейтрализации биологического действия вируса (РНБД) типоспецифическими сыворотками. Конечный результат реакции может быть установлен на основании следующих признаков:
1) нейтрализация ЦПД;
2) нейтрализация реакции гемадсорбции;
3) цветная проба;
4) задержка (торможение) гемагглютинации;
5) свечение клеток, содержащих вирус, под влиянием типоспецифических флуоресци-рующих сывороток;
6) нейтрализация в опыте на животных.
Вопросы к итоговому контролю «Общая вирусология и генетика МО».
-
Чем вирусы отличаются от всех остальных живых организмов?
-
Что такое вирион, капсид, нуклеокапсид, тип симметрии, суперкапсид?
-
Критерии классификации вирусов.
-
Типы вирусных геномов.
-
Методы культивирования вирусов.
-
Заражение лабораторных животных. Правила, способы.
-
Заражение куриных эмбрионов. Правила, способы.
-
Культуры клеток (тканей). Определение, классификация, получение.
-
Признаки размножения вирусов в курином эмбрионе.
-
Методы обнаружения вируса в культуре клеток.
-
Цитопатический эффект, определение, классификация.
-
Методы типирования вирусов.
-
Сущность реакции гемадсорбции.
-
Сущность метода цветных проб.
-
Сущность метода бляшек.
-
Сущность реакции гемагглютинации для обнаружения вирусов.
-
Методы микробиологической диагностики вирусных инфекций.
-
Что такое вирусоскопический метод диагностики?
-
Что такое вирусологический метод диагностики?
-
Типы вирусных инфекций.
-
Особенности и механизмы противовирусного иммунитета.
-
Механизмы персистирования вирусов в организме.
-
Механизмы проникновения вируса в клетку.
-
Где в хозяйской клетке размножаются ДНК- и где РНК-содержащие вирусы?
-
Стадии взаимодействия вируса с клеткой.
-
Что такое вирогения?
-
Механизмы противовирусного действия интерферона.
-
Что такое протоонкоген и онкоген?
-
Формы обмена генетическим материалом у бактерий.
-
Что такое конъюгация, ее механизм.
-
Что такое трансдукция, ее механизмы?
-
Что такое плазмиды, их биологические особенности.
-
Основные классы плазмид.
-
Бактериофаги. Их химический состав и морфология.
-
Типы инфекций, вызываемых бактериофагом. Их особенности.
-
Какая разница между вирулентным и умеренным бактериофагом?
-
Что такое лизогения? Лизогенная конверсия?
-
Стадии взаимодействия Т-чётного фага с бактериальной клеткой.
-
Для чего используются фаги в медицинской практике?
-
Что такое фаготипирование?
З А Н Я Т И Е 10
Дата ______________
Тема: Микрофлора окружающей среды и организма человека. Санитарно-показательные микроорганизмы (СПМО). Санитарно-бактериологическое исследование воды, воздуха, почвы (1 день).
План занятия:
1. Знакомство с микрофлорой человеческого тела: посев отпечатков пальцев, посев слизи из зева.
2. Разбор понятия «санитарно-показательные микроорганизмы», знакомство с их основными группами.
3. Санитарно-бактериологическое исследование воды питьевой:
а) определение ОМЧ (разбор схемы);
б) титрационный метод (разбор схемы);
в) метод мембранной фильтрации (разбор схемы).
4. Санитарно-бактериологическое исследование воздуха:
а) посев воздуха седиментационным методом Р. Коха;
б) аспирационный метод (разбор).
5. Санитарно-бактериологическое исследование почвы (разбор).
а) определение общего количества бактерий в почве;
б) определение бактерий группы кишечных палочек (бродильный (титрационный) метод, метод мембранных фильтров, прямой поверхностный посев на плотные питательные среды);
в) определение перфрингенс-титра (посев почвенных разведений в среду Вильсона-Блера, использование сред накопления для определения клостридий в почве);
г) определение нитрифицирующих бактерий.
Методические указания
1. Сделать посев отпечатков пальцев руки на пластинки МПА и среды Эндо.
При помощи стерильного ватного тампона взять материал со слизистой оболочки зева и произвести посев на простой и кровяной МПА.
2. Критерии для СПМО (разбор). Три группы СПМО.
3. Разбор нормируемых микробиологических показателей качества воды: общее микробное число (ОМЧ), общие колиформные бактерии (ОКБ), термотолерантные колиформные бактерии (ТКБ), коли-фаги.
а) Определение ОМЧ (разбор схемы).
Для определения ОМЧ воды чаще всего используют метод 10-кратных разведений, когда концентрация микроорганизмов каждого последующего разведения в 10 раз меньше предыдущего, затем разведения высевают на питательные среды. В пустые стерильные чашки Петри, соблюдая правила асептики, стерильной пипеткой вносят 1 см3 из заранее приготовленного разведения. Чашки предварительно маркируют (со стороны донышка, а не крышки!), чтобы исключить случайную замену их при падении, сдвиге и др.
Разведения выбирают с таким расчётом, чтобы на чашке выросло от 30 до 300 колоний. Из каждой пробы засевают два разведения. Не позднее чем через 15 мин после внесения материала (разведения) в чашку наливают расплавленного и остуженного до 45+ 5°С 10-12 см3 питательного агара (питательную среду), толщина слоя которого должна быть 4-5 мм. Расплавленную среду и посевной материал незамедлительно тщательно перемешивают круговыми движениями, чтобы микроорганизмы равномерно распределились в массе среды. Чашки Петри оставляют на холодной горизонтальной поверхности на 10-15 мин для охлаждения и застывания среды, после чего посевы помещают в термостат и инкубируют при заданной температуре и экспозиции.
Для дальнейшей работы выбирают чашки, на которых выросло от 30 до 300 колоний, а при посеве нативного материала - от 1 до 300 колоний. Количество колоний на поверхности и в глубине агара подсчитывают визуально или при помощи лупы с 2-5-кратным увеличением.
б) Определение ОКБ и ТКБ титрационным методом.
Метод основан на накоплении бактерий после посева определенных объемов воды в жидкие питательные среды, с последующим пересевом на дифференциальную плотную среду с лактозой и идентификации колоний по культуральным и биохимическим тестам. При исследовании питьевой воды качественным методом (текущий санэпиднадзор) засевают три объема по 100 см3. При исследовании воды с целью количественного определения ОКБ и ТКБ (повторный анализ) засевают соответственно 100, 10 и 1 см3 — по три объема каждой серии.
в) Определение ОКБ и ТКБ методом мембранных фильтров.
Метод основан на фильтровании определенных объемов воды через мембранные фильтры. Для этих целей используют фильтры с диаметром пор 0,45 мкм и размером 35 или 47 мм в диаметре (отечественные фильтры «Владипор» МФАС–С–1, МФАС–С–2, МФАС–МА (№ 4–6) или зарубежные — ISO 9000 или EN 29000). При исследовании воды неизвестного качества для получения изолированных колоний фильтруют следующие объёмы воды: 10, 40, 100 и 150 см3 соответственно на 4 фильтра. Далее фильтры помещают на чашки со средой Эндо и инкубируют при 37°С или 44°С в течение 24 ч. Если на фильтрах нет роста колоний или отмечен рост плёнчатых, губчатых, плесневых, прозрачных или расплывчатых колоний, то выдаётся отрицательный ответ.
4. Для санитарно-бактериологической оценки состояния воздуха используют седиментационный и аспирационный методы.
а) Седиментационный метод Коха прост, не требует специальной аппаратуры. Суть метода: чашка с питательной средой ставится на рабочем столе, открывается на 10 мин, закрывается и ставится в термостат, где выдерживается двое суток при температуре 37°С, а затем двое суток при комнатной температуре. После этого проводится подсчет выросших колоний по формуле Омелянского.
Для выявления грибов в воздухе посев проводится на среду Сабуро, и чашка выдерживается при 22-25°С до 5 суток. Для выявления патогенных бактерий посевы проводят на дифференциально-диагностические среды: для золотистого стафилококка — на желточно-солевой агар, для энтеробактерий — на среду Эндо с добавлением генцианвиолетта (для торможения роста сапрофитов), для псевдомонад — на среду № 9 (ГФ XI, т. 2). Чашки выдерживают в открытом виде 1 час, после чего ставят в термостат для культивирования при 37°С на двое суток с последующим выдерживанием при комнатной температуре в течение 2 суток.
Расчет по модифицированной формуле Омелянского ведется на 1 м2 поверхности:
X = n.104 / .r2.t ,
где X - ОМЧ воздуха обследуемого помещения (КОЕ); п - количество колоний на чашке (КОЕ); t - время экспозиции чашки (мин); .r2 - площадь чашки Петри (см2); 104 - пересчет м2 в см2.
Формула Омелянского, даже модифицированная, имеет ряд существенных недостатков: 1) нельзя определить точный объем воздуха, из которого микробы оседают на чашку; 2) мелкодисперсная фаза аэрозоля (а с ним и микробы) практически не оседает и токами воздуха постоянно поддерживается во взвешенном состоянии.
Результаты, получаемые с помощью этого метода, позволяют сравнить, сопоставить степень микробной обсемененности разных помещений и ориентироваться при разработке мероприятий по очищению воздушной среды.
б) Аспирационный метод изучения микрофлоры воздуха основан на использовании ударной струи воздуха, получаемый с помощью аппарата Кротова или других подобных ему аппаратов (импактеры (ПУ-1Б), импинджеры (ПОВ-1), система HiAir PetriTM . Последняя позволяет пропускать до 1000 л воздуха за 200 сек.). Достоинства этого метода:
- точно учитывается объем воздуха, пропускаемого через чашку с питательной средой, установленную в аппарате;
- принцип ударной струи воздуха способствует фиксации на влажной поверхности питательной среде всех взвешенных частиц аэрозоля.
Таким образом, удается фиксировать на поверхности плотной питательной среды максимальное количество микроорганизмов, обитающих в воздухе. Используя различные виды элективных и дифференциально-диагностических питательных сред, можно выявлять в воздухе все основные группы патогенных и условно-патогенных микроорганизмов.
5. Для санитарно-бактериологической оценки состояния почвы используют определение общего количества бактерий, бактерий группы кишечной палочки, а также определение перфрингенс-титра и нитрифицирующих бактерий.
а) При определении общего количества бактерий в почве посев проводят в 1,5% МПА – не менее двух различных разведений пробы в зависимости от степени предполагаемого загрязнения исследуемой почвы. Перед посевом каждое разведение тщательно перемешивают стерильной пипеткой, забирают 1 см3 суспензии и переносят на дно стерильной чашки Петри. Из каждого разведения посев проводят минимум в две параллельные чашки. После этого в чашки вливают 15-20 см3 предварительно расплавленного и остуженного до температуры 45 °С питательного агара, тщательно перемешивают с почвенной суспензией и оставляют до застывания в строго горизонтальном положении. После застывания агара чашки с посевами помещают в термостат в перевёрнутом виде (крышкой вниз) при температуре 37 °С на 24 ч. После инкубации подсчитывают выросшие колонии и проводят пересчёт на 1 г почвы.
б) Определение бактерий группы кишечных палочек проводят несколькими методами: бродильным (титрационным), методом мембранных фильтров и прямым поверхностным посевом в плотные питательные среды.
Бродильный (титрационный) метод. При анализе почвы с невысокой степенью фекального загрязнения рекомендуют проводить определение БГКП титрационным методом с использованием среды Кесслер или лактозного бульона с трифенилтетразолием хлорида (ТТХ). 10 см3 почвенной суспензии первого разведения (1:10) засевают во флакон с 50 см3 среды, что соответствует посеву 1 г почвы. Последующие разведения высевают по 1 см3 в пробирки с 9 см3 той же среды. Перед посевом в каждую пробирку с лактозным бульоном добавляют 0,3 см3 2% водного раствора ТТХ, а в каждый флакон – по 1,5 мл. Методика посева с использованием ТТХ основана на способности кишечной палочки восстанавливать бесцветное соединение ТТХ в трифенилформазан, выпадающий в осадок, придающий среде коричнево-красный цвет. Кишечная палочка устойчива к действию формазана, в то время как развитие другой микрофлоры подавляется. Посевы на среде Кесслер-Свенертона инкубируют 48 ч при температуре 43 или 37 °С. Отсутствие через 48 ч газообразования и помутнения в бродильных сосудах позволяет дать отрицательное заключение о наличии БГКП. Отрицательное заключение при использовании лактозного бульона с ТТХ дают через 24 ч в том случае, если в пробирках и флаконах цвет среды не изменился. При наличии признаков бактериального роста проводят высев на среду Эндо или розоловый агар. Чашки с посевами инкубируют при температуре 37 °С 24 ч. В случае отсутствия признаков роста на чашках дают отрицательное заключение. Красные, розовые с металлическим блеском, жёлтые и оранжевые колонии на розоловой среде типичны для кишечных палочек. На заключительном этапе исследования проводят идентификацию выросших на агаризованных средах характерных колоний (аналогично анализу БГКП в воде). Результаты анализа выражают коли-титром.
Метод мембранных фильтров используют в качестве ускоренного метода анализа слабозагрязнённых почв. Через стерильные мембранные фильтры № 3 с помощью фильтровального аппарата Зейтца пропускают 5–10 см3 почвенной суспензии первого разведения, которую предварительно центрифугируют при 2000 об./мин в течение 5 мин. Дальнейшее исследование проводят аналогично анализу БГКП в воде методом мембранных фильтров.
Прямой поверхностный посев на плотные питательные среды применяют для исследования почвы из мест интенсивного фекального загрязнения. Проводят прямой поверхностный посев почвенной суспензии в количестве 0,1 или 0,05 см3 на среды Эндо. При анализе сравнительно чистых почв посев проводят из разведений 1:10-1:100, для загрязнённых почв используют разведение 1:106. Посевы инкубируют в термостате при температуре 37 °С в течение 24 ч. На следующем этапе исследования идентифицируют выделенные бактерии (аналогично определению БГКП в воде).
Результаты двух последних методов исследований выражают коли-титром или коли-индексом.
в) Определение перфрингенс-титра проводят по двум общепринятым методикам.
Посев почвенных разведений в среду Вильсона-Блера. Из всех почвенных разведений (до 1:106) образцы по 1 см3 переносят в 2 параллельных ряда пробирок. Один ряд пробирок прогревают при температуре 80 °С в течение 15 мин и/или при 90 °С – 10 мин. Затем во все пробирки добавляют по 9-10 см3 свежеприготовленной среды Вильсона-Блера. Инкубацию посевов проводят при температуре 37 или 43 °С в течение 24 ч. Учёт можно проводить и несколько раньше, так как санитарно-показательные клостридии, преимущественно С. perfringens, через несколько часов образуют колонии чёрного цвета. Обнаружение в мазках колоний характерных грамположительных палочек указывает на наличие С. perfringens. Общепринятая методика определения С. perfringens на среде Вильсона-Блера имеет существенный недостаток – питательная среда в определённой степени ингибирует рост микроорганизма. Для устранения этого явления предложена модификация методики.
Использование сред накопления для определения клостридий в почве. По 1 см3 прогретых и нативных почвенных разведений засевают в пробирки с полужидкими и жидкими питательными средами, предварительно регенерированными кипячением (Клодницкого, Китт-Тароцци, бульона Мартена с ватой и др.). После инкубации посевов в течение 18-20 ч при температуре 37 °С проводят высев 0,5-1 см3 материала из помутневших пробирок в среду Вильсона-Блера или сульфит-полимиксин-неомициновую среду. Посев, инкубацию и учёт при этом проводят аналогично первому способу.