Материал: Методическое пособие. Общая микробиология
З А Н Я Т И Е 7
Дата ______________
Тема: Бактериофагия. Генетика микроорганизмов. Мутации и рекомбинации.
План занятия:
1. Явление бактериофагии. Демонстрация феномена бактериофагии на жидких и плотных средах.
2. Методы титрования фага.
3. Типы и механизмы генетических рекомбинаций: трансформация, трансдукция, конъюгация (разбор схем).
а) Опыт трансдукции (разбор)
б) Постановка опыта конъюгации.
2.Плазмиды бактерий. Классы и свойства R-плазмиды.
3.Молекулярные механизмы мутаций у бактерий (разбор).
4.Получение рекомбинантных молекул ДНК (разбор).
Методические указания
1. Зарисовать феномен бактериофагии на плотной питательной среде.
2. Для титрования бактериофага используются различные методы. Наиболее точным является метод агаровых слоев, предложенный Грациа. Сущность этого метода состоит в следующем.1,5%-ный МПА с генцианвиолетом (0,1 мл 0,1% генционвиолета на 1 л среды), который добавляется для предохранения от загрязнения грамположительной воздушной микрофлорой, накануне опыта разливают по 25-30 мл в чашки Петри. Чашки хорошо просушивают в термостате или под бактерицидной лампой, после чего оставляют на ночь при комнатной температуре.
Перед опытом 0,7% МПА расплавляют и разливают по 2,5 мл в пробирки, охлаждают до 46-47°С и затем добавляют в пробирки по 1 мл исследуемого фага (предварительно разведенного) и 0,1 мл эталонной культуры, все это быстро и тщательно перемешивают, вращая пробирку между ладонями, после чего выливают в чашки на поверхность 1,5% агара. Смесь осторожными движениями распределяют так, чтобы над слоем 1,5% агара образовался слои 0,7% агара, содержащего бактериофаг и чувствительную к нему культуру бактерий. Для застывания добавленного агара чашки оставляют на столе на 1-1,5 часа, а затем помещают в термостат при 37°С . Для получения четких результатов необходимо соблюдение следующих условий: а) чашки с 1,5% агаром должны быть хорошо высушены; б) чашки должны находиться после добавления 0,7% агара строго в горизонтальном положении во избежание стекания агара в одну сторону; в) расплавленный 0,7% агар после охлаждения до 46°С нельзя долго хранить, так как он может приобрести гелеобразную консистенцию.
Учет результатов титрования можно производить после 5-6-часового инкубирования в термостате. Для этого подсчитывают количество колоний фага («стерильных» пятен) и умножают полученное число на фактор разведения. Например, при посеве 1 мл фага, разведенного в 10-7 на чашке обнаружено 45 колоний, следовательно, титр фага равен 45×107 = 4,5×108 Зарисовать демонстрационный опыт титрования фага по Грациа.
|
|
|
|
Бактериофагия на плотной ПС («стерильные» пятна) |
Титрование фага по методу агаровых слоёв (по Грациа) |
3. а) Опыт трансдукции.
К 1 мл 3-часовой бульонной культуры реципиента Е. соli 1ас- добавляют в таком же количестве трансдуцирующий фаг, выделенный из культуры Е. соli 1ас+, в концентрации 106-107 . Смесь инкубируют при 37°С в течение часа, после чего 0,1 мл высевают на среду Эндо. В качестве контроля на среду Эндо высевают также культуру Е.соli lас+ (реципиент без фага). Посевы ставят на сутки в термостат. Учет результатов производят по числу выросших окрашенных колоний.
б) Опыт конъюгации.
Сущность опыта заключается в том, что от донорных клеток путем конъюгации передаются гены, контролирующие способность синтезировать треонин и лейцин, клеткам-реципиентам, ауксотрофным по этим аминокислотам.
В качестве донора используется культура Е. coli Hfr с генотипом tre+, lei+, met-, strs (strs – чувствительность к стрептомицину). Реципиентом служит культура Е. coli F– с генотипом tre-, lei-, met+, strr (strr - устойчивость к стрептомицину) .
Для выделения рекомбинантов используют солевую среду М-9 со стрептомицином, содержащую глюкозы 1,0 г; стрептомицина – 200 ед/мл; NH4Cl – 1,0 г; NaС1 – 0,5 г; Na2HРO4 – 6,0 г; КH2PO4 – 3,0 г; Mg2SO4 – 0,2 г; дистиллированной воды – 1,0 л. Для тех же целей может быть использована плотная среда. В этом случае к указанному составу добавляется 20,0 г агар-агара.
На этой среде могут расти только рекомбинанты (трансконъюганты). Культуры донорного и реципиентного штаммов не растут на данной среде, так как первая ауксотрофна по метионину и чувствительна к стрептомицину, а вторая ауксотрофна по треонину и лейцину.
Постановка опыта: к 2 мл 3-часовой бульонной культуры реципиента добавляют 1 мл 3-часовой бульонной культуры донора. Смесь инкубируют в течение 30 минут при 37°С. Затем смесь разводят в 100 и 1000 раз и засевают разведения в объеме 0,1 мл на селективную среду для выделения рекомбинантов. В качестве контроля на такую же среду засевают культуры донора и реципиента в том же объеме. На следующие сутки регистрируют результаты опыта. В пробирках с посевом рекомбинанта наблюдается помутнение среды. В средах с посевами донорной и реципиентной культур роста нет. Аналогичным образом регистрируют результаты посевов на плотных средах.
Просмотреть посевы культур донора, реципиента и рекомбинантов на минимальной среде со стрептомицином. Обратить внимание на рост культуры рекомбинантов. Культуры донора и реципиента не растут на данной среде, так как культура донора ауксотрофна по метионину и чувствительна к стрептомицину, а культура реципиента ауксотрофна по треонину и лейцину.
Контрольные вопросы
Что такое бактериофаг?
Каковы морфология, размеры и химический состав фагов?
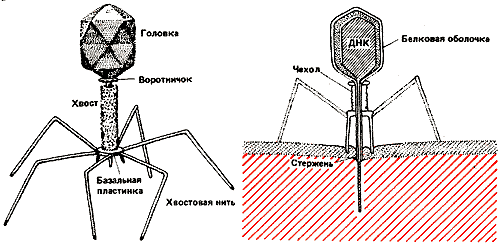
Что содержится в головке бактериофага?
Как устроен хвостик фага и каково его назначение?
Из каких этапов складывается взаимодействие фага с микробной клеткой?
Каким образом фаг вводит свою нуклеиновую кислоту в микробную клетку?
Как осуществляется синтез фаговых частиц внутри микробной клетки?
Какая разница между вирулентным и умеренным фагом?
Что такое лизогения и лизогенная конверсия?
Как выделяют фаги из объектов внешней среды?
Какова методика определения титра фага по Грациа?
Что такое фаготипирование? С какой целью оно применяется?
Что такое ген?
Что таков мутации спонтанные и индуцированные?
Каков молекулярный механизм мутации?
Какие вы знаете мутагены?
Что такое ауксотрофы? Как получают ауксотрофные штаммы бактерий?
Каков механизм генетических рекомбинаций?
Что такое трансформация?
Что такое трансдукция и какими свойствами обладает трансдуцирующий фаг?
Что такое конъюгация бактерий? Как она осуществляется?
Как производят картирование хромосом?
Что такое плазмида?
Какие известны классы плазмид?
Каковы основные свойства плазмид?
Какие существуют типы генетического контроля лекарственной устойчивости у бактерий?
Каковы основные функций F-фактора?
В чем заключается механизм конъюгации бактерий?
Что такое бактериоцины?
Каковы основные свойства Соl -плазмид?
Какими свойствами обладают R-плазмиды?
Как определяют конъюгативные свойства плазмид?
Как получают рекомбинантные молекулы ДНК?
Что такое генетический вектор?
Как у бактерий можно обнаружить плазмиды?
В каких направлениях могут быть использованы достижения генной инженерии?
Приложение к ЗАНЯТИЮ 7.
Определение понятия ген
Ген – универсальная организующая структурная единица живой материи, которая благодаря содержащейся в ней закодированной информации обеспечивает единство и многообразие всех форм существования жизни, ее непрерывность и эволюцию.
Ген – основной носитель и хранитель жизни, а его продукт – белок – способ её существования.
Основные формы обмена генетическим материалом у бактерий
1.Конъюгация - обмен хромосомными и плазмидными генами путем установления контакта между донорной и реципиентной клетками с помощью донорных ворсинок (пилей). Механизм конъюгации контролируется конъюгативными (донорными) плазмидами.
2.Трансдукция - перенос генов от донорной клетки в реципиентную с помощью фагов.
3.Сексдукция - перенос генов от донорной клетки в реципиентную с помощью F-фактора (полового фактора).
4.Трансформация - поглощение компетентными клетками внеклеточной ДНК.
5.Трансфекция - поглощение протопластами свободной фаговой ДНК.
Плазмиды – наипростейшие живые существа, лишенные белковой оболочки и представленные только совокупностью организованных генов, определяющих их специфические свойства, наследственность, а также дополнительные признаки, которыми они наделяют клеткуносителя.
Плазмиды подразделяются на конъюгативные, т,е. способные к самопереносу, и неконъюгативные, перенос которых осуществляется конъюгативными плазмидами.
Передача плазмид среди бактерий происходит как по вертикали, так и по горизонтали, обеспечивая их эпидемическое распространение.
Специфические функции плазмид
1.Саморепликация.
2.Конъюгативность, или способность к самопереносу (у конъюгативных плазмид).
3.Мобилизуемость, или способность к мобилизации на перенос конъюгативными плазмидами (у неконъюгативных плазмид).
4.Контроль явления несовместимости.
5.Контроль явления поверхностного исключения.
6.Контроль числа копий на хромосому клетки-хозяина.
7.Контроль стабильности поддержания и распределения между дочерними клетками.
8.Способность наделять клетку-хозяина дополнительными важными селективными свойствами. Фенотипические проявления этих свойств определяют класс плазмид.
Классы плазмид
|
КЛАСС |
ФУНКЦИЯ |
|
F-плазмиды |
Донорные функции |
|
R-плазмиды |
Устойчивость к лекарственным препаратам |
|
Col-плазмиды |
Синтез колицинов |
|
Ent-плазмиды |
Синтез энтеротоксинов и факторов адгезии |
|
Hly-плазмиды |
Синтез гемолизинов |
|
Биодеградативные |
Разрушение различных органических соединений |
|
Криптические |
Функции неизвестны |
|
Схема строения крупного Т-чётного фага |
|
|
З А Н Я Т И Е 8
Дата ______________
Тема: Морфология и ультраструктура вирусов. Клеточные культуры. Репродукция вирусов. Методы индикации вирусов.
План занятия:
1. Вирусы: а) вирионы вируса оспы в препаратах, окрашенных по Морозову; б) внутриклеточные включения при бешенстве – микроскопия телец Негри.
2. Методы культивирования вирусов. Заражение материалом, содержащим вирусы, лабораторных животных.
3. Культивирование вирусов в культурах клеток. Получение первично-трипсинизированных клеток. Питательные среды и солевые растворы.
4. Подсчет количества клеток.
5. Культуры перевиваемых клеток. Микроскопия незараженных культур клеток.
6. Рассев клеток перевиваемых штаммов по пробиркам.
7. Заражение культуры клеток вирусом осповакцины (или каким-либо другим вирусом).
8. Культивирование вирусов в куриных эмбрионах: а) изучение методов заражения куриных эмбрионов; б) заражение куриных эмбрионов вирусом гриппа.
Методические указания
1. а) Элементарные тельца (вирионы) вируса оспы (тельца Пашена) в препаратах, окрашенных по Морозову, выглядят в виде мелких точек круглой или удлиненной формы, темно-коричневого цвета.
б) Внутриклеточные включения при бешенстве (тельца Бабеша-Негри – выкристаллизовавшиеся нуклеокапсиды вируса) обнаруживаются в нервных клетках аммонова рога и в клетках Пуркинье мозжечка. В препарате, окрашенном по Туревичу, цитоплазма и ядра нервных клеток окрашенны в желто-зеленый (защитный) цвет. Тельца Негри расположены в цитоплазме рядом с ядром клетки и окрашены в малиново-красный цвет. При окраске по Манну - тельца Негри красного цвета на голубом фоне цитоплазмы.
Все рассмотренные препараты зарисовать.
|
|
|
|
Вирионы оспы (тельца Пашена) окраска по Морозову |
Тельца Бабеша-Негри при бешенстве окраска по________________ |
2. Методы заражения животных разнообразны: внутрибрюшинный, внутривенный, внутримышечный, интраназальный, заражение в мозг и другие.
Заражение в мозг (метод применяют при работе с нейротропными вирусами). Для заражения чаще используют белых мышей. Левой рукой плотно прижимают мышь к столу, большим и указательным пальцами оттягивают кожу головы назад. Туберкулиновым шприцем с предохранительной муфтой на игле прокалывают лобную кость несколько латеральнее средней линии и вводят 0,02-0,03 мл материала. Игла вводится на глубину 1,5-2 мм, при этом отчетливо ощущается "провал" в полость черепа.
При заражении новорожденных мышей (2-3-дневного возраста) их лучше брать руками в перчатках, чтобы после заражения мышата не имели постороннего запаха (пота, дезинфицирующих веществ, антибиотиков и т.д.), так как самка съедает мышат, имеющих посторонний запах. Материал вводят в количестве 0,01 мл. Вытекающую жидкость удаляют сухим стерильным ватным тампоном без дезинфицирующих веществ. После заражения мышат помещают в отдельную банку (в свое гнездо), а через 20-30 мин подсаживают к ним самку.
Больных мышат самка также съедает. Поэтому надо уловить момент извлечения зараженных животных для завершения опыта. Первые два дня просматривают мышат 1-2 раза в день, а затем чаще. Через 3-4 дня здоровый мышонок в два раза больше зараженного.
3. Кроме животных для культивирования вирусов используют куриные эмбрионы и культуры клеток различных тканей. Культуры ткани - это клетки ткани выращенные вне организма на специальной питательной. среде. Клетки ткани в искусственных условиях сохраняют присущий им обмен и восприимчивость к определенным вирусам. Для культивирования вирусов особенно пригодны клетки с быстрым ростом. По этой причине широко применяют эмбриональные ткани (фибробласты куриных эмбрионов, клетки человека и др., а также культуры тканей опухолей (клетки Неla, Нер-2 и др.).
Кулътивирование клеток может производиться в специальных флаконах (колбы-матрацы, флаконы Карреля) и в пробирках. Культура клеток для роста должна иметь какую-либо опору, например, стенку пробирки.
В выросшую культуру ткани, которая покрывает стенку сосуда в виде однослойного клеточного пласта, засевают материал, содержащий вирус. Работу производят в стерильных условиях. Для подавления роста микрофлоры вируссодержащий материал предварительно обрабатывают антибиотиками, чаще пенициллином и стрептомицином.
О наличии и размножения вируса в клетках узнают по так называемому цитопатическому эффекту: в результате размножения вируса клетки гибнут, и под микроскопом заметны дегенеративные изменения клеток. Пласты зараженных клеток отслаиваются от стенки пробирки или флакона. Так как рост клеток прекращается, pН среды мало изменяется по сравнению с контролем (клетки без вируса).
Питательной средой для культуры ткани могут быть различные растворы, состав которых приближается к составу жидкости организма (синтетическая среда 199, солевой раствор Хенкса с сывороткой, гидролизат лактальбумина с сывороткой и другие).
Получение первично-трипсинизированных клеток.
Живые клетки для однослойных культур ткани могут быть получены из эмбрионов и органов взрослых животных (напр., из почек) и человека. Для диспергирования ткани используют 0,25-0,3% раствор трипсина, который разрушает межклеточные мостики из соединительной ткани и освобождает клетки.
Метод трипсинизации тканей состоит в следующем: ткань измельчают ножницами (или другим способом) на мелкие кусочки размером 1-3 мм, промывают в буферном растворе Хенкса для удаления крови 2-3 раза, до тех пор, пока жидкость не станет почти прозрачной. Для диспергирования отмытые кусочки ткани обрабатывают раствором трипсина (добавляют 2 объема раствора трипсина) при температуре 32-37°С. Трипсинизацию проводят в течение нескольких минут (до 10 мин) при постоянном перемешивании пипеткой или в смесителе на электромагнитной мешалке. Суспензию клеток собирают в сосуд, помещенный на лед для прекращения действия фермента. К оставшейся ткани добавляют свежие порции трипсина, т.е. процесс повторяют 6-8 раз, иногда и более – до прекращения помутнения раствора трипсина.
Жидкость, содержащую клетки, фильтруют через марлю для отделения от неё комочков ткани и соединительнотканных волокон, центрифугируют при 2000 об/мин в течение 5 минут, надосадочную жидкость сливают, а клетки отмывают раствором Хенкса. Отмытые клетки добавляют к питательной среде (гидролизат лактальбумина с сывороткой, или среда 199 , или др.) в разведении 1:200.
4. С помощью камеры Горяева подсчитают количество клеток в 1 мл. Клетки считают по всей камере под малым увеличением микроскопа. Количество клеток в 1 мл вычисляют по формуле:
Количество клеток в 1 мл =
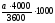 ;
;
где а - количество клеток в камере;
3600 - количество квадратов в камере;
1/4000 мм - объем одного квадрата.
Так как в одном мл 1000 мм , то полученный результат умножают на 1000. После первого разведения (1:200) концентрация клеток достигает 600000-1300000 на 1 мл. Клетки куриных эмбрионов разводят той же средой до концентрации 400000 клеток в 1 мл.
Взвесь клеток разливают по 1 мл в пробирки, которые плотно закрывают стерильными резиновыми пробками для того, чтобы среда не выщелачивалась. Пробирки помещают в термостат при 37°С почти в горизонтальном положении (под углом в 5°) в специальных штативах. Через 3-4 дня при микроскопии виден сплошной слой размножившихся клеток. Пробирки с хорошим ростом ткани отбирают для заражения вирусом.