Материал: Методическое пособие. Общая микробиология
Для выделения бактероидов по 0,1 мл из этих же разведений материала засевают на КАБ (кровяной агар бактероидов) с неомицином и культивируют по модифицированному методу Фортнера: площадь посева закрывают преципитационными (малого диаметра) чашками, создавая строго анаэробные условия, необходимые для культивирования бактероидов.
По 0,1 мл разведений 10-7, 10-6 и 10-5 засевают на молочно-растительную среду /МРС/ - для выделения лактобацилл. Из разведений 10-6 и 10-5 делают посев по 0,1 мл на среду Эндо - для изоляции энтеробактерий; 0,1 мл из разведения 10-6 засевают на кровяной агар - для выявления гемолитической активности аэробной микрофлоры.
Для выявления энтерококков используют среду Калины, засевая по 0,1 мл из разведений 10-6 и 10-5.
По 0,1 мл из разведения 10-4 засевают на чашечную среду Симмонса, позволяющую изолировать наиболее часто встречаемые УПЭ (представителя рода Цитробактер и трибы Клебсиелла) и на желточно-солевой агар - для выделения стафиллококков.
0,1 мл из разведения 10-3 засевают на среду Сабуро с полимиксином - для выделения дрожжей и дрожжеподобных грибов. Для выделения клостридий по 0,1 мл из разведений 10-3 и 10-4 засевают на среду Вильсон-Блера.
Все посевы инкубируют в термостате при 37 °С.
На второй день исследования:
1. Производят учёт роста на среде Эндо. Подсчитывают общее число, выросших колоний кишечных палочек, обращая внимание на их характер (цвет, наличие металлического блеска, диссоциацию, формы с пониженной ферментативной активностью). При обнаружении лактозоотрицательных колоний анализ ведут как при выявлении патогенных представителей семейства энтеробактерий.
2. Кровяной, желточно-солевой агар и среду Сабуро извлекают из термостата и оставляют для дальнейшей инкубации при комнатной температуре, а желточно-солевой агар - при действии рассеянного света - для лучшего выявления пигментообразования.
На третий день исследования:
1. Производят учёт роста УПЭ на среде Симмонса. Помимо УПЭ (представителей родов Цитробактер, Энтеробактер, Клебсиелла, Гафния, наиболее часто выделяемых из фекалий, а также Провиденсия, изолируемых из этого материала реже), дающих белые или окрашенные в цвет среды мелкие и средней величины слизистые или сухие колонии, часто в R-форме, изменяющие (в случае утилизации цитрата натрия) цвет среды до синего или не изменяющие его, вырастают кишечные палочки, в том числе и с пониженной ферментативной активностью, в виде очень мелких, прозрачных, зеленовато-белых колоний. Подсчитывают общее число колоний УПЭ, выросших на среде Симмонса, - делая перерасчёт на 1 г. В случае роста на чашке колоний УПЭ нескольких типов ведут подсчёт каждого из них и соответствующий пересчёт на 1 г фекалий.
Для идентификации УПЭ производят посев части изучаемой колонии на скошенный МПА, а другой части - на среду Кларка.
2. Учитывают количество колоний стафилококка, подтверждённого изучением морфологии в окрашенном по Граму мазке, на желточно-солевом агаре, делают пересчёт на 1 г, определяют пигментообразование и образование лецитиназы (лецитовителлазы), производят отсев колонии для выделения чистой культуры и дальнейшего определения вида стафилококка.
3. Производят подсчёт числа колоний энтерококка на среде Калины (с пересчётом на 1 г), определяют наличие или отсутствие протеолитической активности.
4. На кровяном агаре отмечают наличие или отсутствие гемолиза, в положительном случае определяют морфологию микроорганизма; подсчитывают % гемолитических форм к общему количеству выросших на этой среде колоний.
5. Отмечают наличие чёрных колоний на среде Вильсон-Блера, подсчитывают их общее количество (с переводом на 1 г), подтверждают принадлежность выросших микроорганизмов к клостридиям изучением морфологии в окрашенном по Граму мазке. Нередко на этой среде вырастают, представители рода Протеус и Цитробактер, давая колонии, схожие с колониями клостридий.
6. Регистрируют рост на среде Сабуро с полимиксином, где вырастают дрожжи и дрожжеподобные грибы, давая белые средней величины и крупные колонии. Морфологию микроорганизмов подтверждают микроскопией окрашенных по Граму препаратов. Определяют общее количество выросших колоний, делают пересчёт на 1 г, а для дифференциации дрожжей от дрожжеподобных грибов рода Кандида, делают посев на картофельный или крахмальный агар (для определения филаментации, характерной для грибов рода Кандида и отсутствующей у дрожжей).
На четвёртый день исследования:
I. Учитывают рост бифидобактерий на среде Блаурокка. Для этого из каждой пробирки с ростом готовят мазки, окрашивают по Граму и микроскопируют. При микроскопии препаратов отмечается характерная для бифидобактерий морфология и расположение. Учитывают предельное разведение материала, в котором ещё регистрируется рост бифидобактерий, подтверждённый нахождением этих микроорганизмов в окрашенных по Граму препаратах. При этом, не допуская большую ошибку, можно перевести предельное разведение материала на количество бифидобактерий в 1 г фекалий. Допустим, предельным разведением материала, в котором зарегистрирован рост бифидобактерий, подтверждённый изучением морфологии в мазке, было 10-10. С большой долей вероятности можно считать, что количество бифидобактерий в 1 г фекалий соответствует 1010 (этот пересчёт необходим для дальнейшего определения соотношения бифидобактерий и других микроорганизмов).
2. Регистрируют рост лактобацилл на МРС, подсчитывают общее число колоний этих микроорганизмов, приводят к 1 г. Лактобациллы на МРС растут в виде мелких беловато-серых с ровными краями или более крупных желтовато-серых с изведенными краями колоний, дифференцировать которые от колоний других микроорганизмов не предоставляет особого труда. Лактобациллы довольно хорошо растут на среде Сабуро с полимиксином.
3. Производят учёт бактероидов на КАБах. На этой среде указанные микроорганизмы растут в виде мелких беловато-серых колоний; в мазке - это грамоотрицательные мелкие палочки, расположенные без особого порядка. Делают пересчёт для определения количества бактероидов в 1 г фекалий. Для дифференциации бактероидов от лактобацилл, спорообразующих бактерий и др. микроорганизмов производят посев части колонии на КАБ с последующим культивированием в аэробных условиях, а также окраску, на выявление спор.
4. Повторно учитывают рост грибов рода Кандида на среде Сабуро с полимиксином (при отсутствии роста на этой среде через 24-48 часов); при наличии роста, производят изучение как в п.6 третьего дня исследования.
5. Для идентификации УПЭ производят посев чистой культуры со скошенного МПА на среды с аминокислотами (лизином, аргинином, орнитином).
На пятый день исследования:
1. Производят учёт филаментации (если предварительно были подозрительные колонии на среде Сабуро).
2. Учитывают тесты, дифференцирующие бактероиды от лактобацилл и аэробов (по отсутствию роста на МРС и на КАБах в аэробных условиях).
3. Для идентификации УПЭ производят учёт изменений со сред с аминокислотами, а также результатов реакции Фогес-Проскауэра и с метиловым красным, что в ряде случаев даст возможность установить род и вид; в том случае, когда идентификацию по указанным тестам провести не удаётся, проводят посев на дополнительные углеводы.
4. Выдача ответа.
В ответе следует указать количество анаэробов (бифидобактерий, бактероидов, лактобацилл), а также количество аэробных микроорганизмов различных родов, изолированных из 1г фекалий.
В заключении следует указать на отсутствие или наличие дисбактериоза кишечника и степень его выраженности.
Основой для заключения должно быть соотношение количества бифидобактерий (как основных представителей анаэробной группы бактерий, выполняющих наиболее важную для организма физиологическую функцию) и аэробов.
При установлении пограничных состояний между нормой и патологией очень важным показателем является соотношение между бифидобактериями и E.coli.
Для его установления количество бифидобактерий, определённых в конкретном образце, подтверждённых изучением морфологии в окрашенных по Граму препаратах, принимают за 100 %, а количество E. coli за Х. Составляют пропорцию и высчитывают значение X.
Например, количество бифидобактерий в I г = 1010, а количество E. coli = 700 млн.
Составляем пропорцию:
1010 ------ 100 %
700 млн ----- X
X = 7 %
Данный показатель превышает норму (5 %) и свидетельствует о начальных сдвигах в микрофлоре (нарушение соотношения между бифидобактериями и E. coli), что может быть определено как дисбактериоз I степени. Однако такие расчёты следует проводить не во всех случаях, а только тогда, когда имеются затруднения в дифференциации дисбактериоза I степени и эубиоза.
Приложение к ЗАНЯТИЮ 11
Количественный и качественный состав микрофлоры кишечника в норме
|
Названия микроорганизмов |
Дети до 1 года |
Дети старшего возраста |
Взрослые |
|
Бифидобактерии |
1010 – 1011 |
109 – 1010 |
108 – 1010 |
|
Лактобактерии |
106 – 107 |
107 – 108 |
106 – 108 |
|
Эшерихии |
106 – 107 |
107 – 108 |
106 – 108 |
|
Бактероиды |
107 – 108 |
107 – 108 |
107 – 108 |
|
Пептострептококки |
103 – 105 |
105 – 106 |
105 – 106 |
|
Энтерококки |
105 – 107 |
105 – 108 |
105 – 108 |
|
Сапрофитные стафилококки |
≤104 |
≤104 |
≤104 |
|
Патогенные стафилококки |
- |
- |
- |
|
Клостридии |
≤103 |
≤105 |
≤105 |
|
Кандида |
≤103 |
≤104 |
≤104 |
|
Патогенные энтеробактерии |
- |
- |
- |
З А Н Я Т И Е 12
Дата ______________
Тема: Санитарно-микробиологическое исследование пищевых продуктов (разбор схемы). Бактериологический контроль качества стерилизации и дезинфекции.
План занятия:
1. Проведение санитарно-микробиологического исследования пищевых продуктов на наличие санитарно-показательных микроорганизмов.
а) определение количества бактерий группы кишечных палочек;
б) методы обнаружения сальмонелл;
в) методы выявления и определения количества Staphylococcus aureus в колбасных изделиях.
2. Исследование пищевых продуктов на наличие возбудителей пищевых токсикоинфекций: посев на среды обогащения и дифференциально-диагностические среды.
3. Изучение морфологических и тинкториальных свойств сальмонелл и кишечной палочки.
4. Методика посева смывов на общую бактериальную обсемененность.
5. Метод отпечатков на «Бактотест» со средой Эндо при санитарно-бактериологическом контроле на объектах питания.
Методические указания
1. а) При определении количества бактерий группы кишечных палочек навеску анализируемого продукта (1,00,001 г по СанПиН 2.3.2.1078-01), в которой не должно быть БГКП, смешивают с 9 частями жидкой питательной среды (чаще всего используют среду Кесслер, содержащую в своём составе генцианвиолет, угнетающий рост грамположительных бактерий). Из пробирок с забродившей средой (помутнение, наличие газа в поплавках) делают посевы на чашки со средой Эндо. Посевы выдерживают в термостате при температуре 37 °С в течение 18-24 ч. Из колоний, типичных для БГКП (красных, с металлическим блеском, розовых, бледно-розовых), готовят мазки и окрашивают их по Граму.
б) Методы обнаружения сальмонелл. Пробу мяса или мясного продукта дважды пропускают через мясорубку, перемешивают, взвешивают 25 г, затем помещают в стерильную банку смесителя с 225 см3 буферной пептонной водой и гомогенизируют. Далее в асептических условиях переносят содержимое смесительной банки в стерильную колбу вместимостью 500 см3. Колбу выдерживают в термостате при температуре (37±1) °С не менее 16 и не более 20 ч, после чего приступают к анализу.
Выявление сальмонелл проводится в четыре последовательных этапа: первичный (прямой) посев, обогащение, посев со среды обогащения и подтверждение.
Первичный посев производится путем посева взвеси исследуемого материала на плотные элективные среды. Эти среды выдерживают в термостате при температуре 37 °С и исследуют на присутствие колоний, которые являются типичными или подозрительными на сальмонеллы.
На элективных средах сальмонеллы растут, образуя характерные колонии:
-
на фуксин-сульфитном агаре (агаре Эндо) сальмонеллы растут в виде круглых, бесцветных или слегка розоватых прозрачных, или полупрозрачных колоний;
-
на эозин-метиленовом синем агаре (агаре Левина) сальмонеллы растут в виде прозрачных, бледных, нежно-розовых или розовато-фиолетовых колоний.
Обогащение проводят путем посева на жидкие селективные среды (среды Мюллера, Кауфмана и Киллиана, селенитовый Ф-бульона и хлористо-магниевая среды "М"). Эти среды выдерживают в термостате при температуре 37 °С. На селенитовом бульоне лучшей температурой для накопления сальмонелл является 43 °С.
В случае отсутствия роста бактерий сальмонелл при первичном (прямом) посеве на элективных средах, через 12-24 ч проводят высев на селективные среды со сред обогащения. Предварительно содержимое флаконов перед пересевом тщательно перемешивают и высевают штрихом петлей диаметром 2,5-3 мм на чашку с висмут-сульфитным агаром, бактоагаром Плоскирева или агаром Эндо. Посевы помещают в термостат на 18-24 ч при температуре 37 °С, а посевы на висмут-сульфитном агаре на 48 ч.
На селективных средах сальмонеллы растут, образуя характерные колонии:
-
на бактоагаре Плоскирева сальмонеллы растут в виде бесцветных колоний, но колонии более плотные и несколько меньшего размера, чем на среде Эндо;
-
на висмут-сульфитном агаре сальмонеллы растут в виде черных или коричневых колоний с характерным металлическим блеском.
Далее проводят подтверждение пересев подозрительных на сальмонеллы колоний и определение их биохимических и серологических характеристик. В соответствии с нормативами санитарно-биологических показателей для мяса и мясных продуктов содержание сальмонелл в 25 г исследованного продукта не допустимо.
в) Методы выявления и определения количества Staphylococcus aureus в колбасных изделиях и продуктах из мяса.
Сущность метода заключается в определении морфологии, характера роста на питательных средах и в способности отдельных стафилококков продуцировать лецитиназу и коагулировать цитратную плазму крови кролика под воздействием фермента коагулазы.
Методика проведения анализа заключается в следующем. Из разведения анализируемой взвеси продукта (1:10) проводят посевы на молочно-солевой агар, содержащий 65 г/дм3 хлористого натрия, для выявления пигмента или желточно-солевой агар, содержащий 65 г/дм3 хлористого натрия, для выявления лецитиназной активности. Взвесь наносят на поверхность агара в количестве 0,2 см3 и равномерно растирают по всей поверхности агаровой среды. Посевы термостатируют в течение 24 ч при температуре 37 °С и 24 ч выдерживают при комнатной температуре.
На поверхности питательной среды колонии стафилококка имеют вид плоских или слегка выпуклых блестящих колоний с ровным краем. При этом на молочно-солевом агаре лучше выявляется пигмент (эмалево-белый или золотистый), а на желточно-солевом агаре колонии стафилококков могут образовывать «радужный венчик», что является одним из признаков их патогенности.
Из подозрительных колоний готовят препараты, которые окрашивают по Граму. При наличии стафилококков в препарате обнаруживаются грамположительные мелкие кокки, располагающиеся неправильными гроздьями.
Для подтверждения признаков патогенности стафилококков ставят реакцию плазмокоагуляции. В прибор с 0,5 см3 цитратной плазмы крови кролика, разведенной физиологическим раствором в соотношении 1:4, вносят петлю чистой суточной культуры стафилококка и ставят в термостат при температуре 37 °С. Реакцию плазмокоагуляции учитывают через 3-4 ч (не встряхивая пробирку) и оставляют в термостате на сутки для окончательного учета через 24 ч.
Тест на коагулазу считают положительным, если культура показала, по крайней мере, 3+ оценку коагулазной реакции, отмеченной на рисунке 1. Реакцию на 1+ или 2+ оценивают как промежуточную.
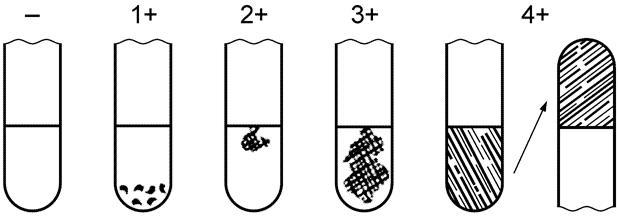
Рис. 1. Результаты коагулазного теста
отрицательная оценка: не отмечено образования фибрина;
1+ положительная оценка: небольшие несформировавшиеся комочки;
2+ положительная оценка: небольшой сформировавшийся комок;
3+ положительная оценка: большой сформировавшийся комок;
4+ все содержимое пробирки скоагулировано и не меняет своего положения при переворачивании пробирки.
Для определения количества стафилококков учитывают колонии стафилококков, давшие положительную реакцию плазмокоагуляции.
Количество S. aureus в 1 см3 или 1 г продукта определяют исходя из количества коагулазоположительных стафилококков, принадлежность которых к S. aureus подтверждена по образованию ацетоина, определению ферментации в аэробных условиях мальтозы и, при необходимости, определению термостабильной нуклеазы и гемолитической активности. При расчете на 1 г продукта количество подсчитанных колоний умножают на степень разведения и делят на количество посевного материала.
2. Приготовить взвесь в физиологическом растворе кусочка пищевого продукта, зараженного сальмонеллами, и произвести посев взвеси на среду обогащения и на дифференциально-диагностическую среду Плоскирева или Эндо.
3. Приготовить препараты-мазки из культур сальмонелл и кишечной палочки, окрасить по Граму, промикроскопировать и сравнить морфологию бактерий во всех препаратах. Препараты зарисовать.