Материал: магістерський іспит з хімії 1
69. Якісний функціональний аналіз
Належність органічних речовин до певних класів встановлюється функціональним аналізом, їх чистота – хроматографією, будова – усіма існуючими фізико-хімічними методами.
Якісний елементний аналіз дозволяє визначити, з атомів яких елементів побудовані молекули органічної речовини; кількісний елементний аналіз встановлює елементний склад сполуки та емпіричну формулу.
При виконанні елементного аналізу органічні речовини “мінералізують” і подальше визначення проводять звичайними методами аналітичної хімії.
Функціональна група |
Основні якісні реакції |
Спостереження |
Подвійний зв’язок |
1. Розчин Br2/CCl4 (жовтий розчин). 2. Розчин KMnO4 (малиновий розчин). |
Знебарвлення. Знебарвлення. |
Потрійний зв’язок Кінцевий потрійний зв’язок |
1. Розчин Br2/CCl4 (жовтий розчин). 2. Розчин KMnO4 (малиновий розчин). Амоніачний розчин [Cu(NH3)2]Cl, або[Ag(NH3)2]OH. |
Знебарвлення. Знебарвлення. Осад купрум ацетиленіду або осад арґентум ацетиленіду. |
Ароматичні системи |
1. CHCl3, AlCl3. 2. HNO3, H2SO4. |
Забарвлені продукти. Нітросполука жовтого кольору. |
Галогени (крім Флуору) |
1. Проба Бейльштейна. 2. Сплавлення з натрієм, потім додавання розчину AgNO3. |
Забарвлення полум’я газового пальника у зелений колір. Осад: білий AgCl, жовтуватий AgBr, жовтий AgI. |
Гідроксильна група в спиртах |
1. Проба Лукаса ZnCl2+HCl. 2. Окиснення хромовою сумішшю K2Cr2O7+H2SO4. |
Спирти: первинні - не реагують; вторинні - помутніння через 10 хв; третинні - помутніння на протязі 3-5 хв. Спирти: первинні - зелене забарвлення; вторинні - зелене забарвлення; третинні - не реагують. |
Гідроксильна група в фенолах |
1. Розчин FeCl3. 2. Бромна вода. 3. Реакція з діазосполуками. |
Фіолетове чи синє забарвлення (червоне, зелене). Осад. Забарвлені сполуки. |
Карбонільна група в альдегідах |
1. 2,4-динітрофенілгідразин. 2. Семікарбозид. 3. NaHSO3. 4. [Ag(NH3)2]OH (реакція срібного дзеркала, реакція Толленса), нагрівання 5. Реактив Фелінга, нагрівання 6. Фуксиносірчиста кислота |
Жовтий або червоний осад 2,4-динітрофенілгідразину карбонільної сполуки. Осад семікарбозону карбонільної сполуки. Осад гідроген сульфатних (ІV) похідних карбонільної сполуки. Металічне срібло у вигляді дзеркального шару. Жовтий або червоний осад Cu2O (ароматичні альдегіди цю реакцію не дають). Інтенсивно рожево-фіолетове забарвлення. |
Карбоксильна група (карбонові кислоти) |
1. Індикатор. 2. Насичений розчин натрій гідргенкарбонату NaHCO3. 3. Одержання похідних: взаємодія зі спиртами у кислому середовищі, нагрівання. |
Зміна кольору індикатора або індикаторного паперу. Виділення бульбашок вуглекислого газу. Утворення естерів зі специфічним запахом. |
Аміногрупа Первинні аміни Первинні аліфатичні Первинні ароматичні Вторинні аміни Третинні аміни |
1. Індикатор. 2. Ізонітрильна проба (NaOH+CHCl3) , нагрівання. 3. HNO2 (NaNO2+HCl). 4. HNO2 (NaNO2+HCl+нафтол). 5. HNO2 (NaNO2+HCl). 6. HNO2 (NaNO2+HCl
|
Аміногрупа Первинні аміни Первинні аліфатичні Первинні ароматичні Вторинні аміни Третинні аміни аліфатичні і чисто ароматичні Третинні аміни жирноароматичні Третинні аміни |
68.Ідентифікація органічних речовин
Ідентифікацію невідомих речовин проводять у певній послідовності.
Попереднє дослідження. Вивчення речовини починають із зовнішнього огляду. При цьому фіксують агрегатний стан, форму кристалів або аморфність для твердих речовин, консистенцію рідких (рухома, в'язка, масляниста і т.д.), забарвлення, запах. Відзначають, наскільки зберігається забарвлення при перекристалізації або при перегонці речовини.
Вивчення забарвлення і запаху дозволяє зробити висновок про можливу наявність деяких класів або навіть індивідуальних речовин. Забарвленими є хінони, деякі -дикетони, азо-, нітрозо-, нітропохідні, полігалогенопохідні, сполуки з великим числом спряжених зв'язків. Багато органічних сполук володіють специфічним запахом, за яким можна визначити, до якого класу вони відносяться (ефіри, феноли, нітросполуки, аміни й ін.).
Для віднесення речовини до того або іншого класу визначають її розчинність у ряді розчинників. Це також дозволяє підібрати розчинник для перекристалізації твердої речовини. В пробірку вносять краплю рідкої або близько 0,01 г твердої досліджуваної речовини і по краплях 0,2 мл розчинника. Після додавання кожної краплі пробірку струшують. Якщо сполука повністю розчинилася, її реєструють як розчинну. Якщо речовина погано розчиняється або зовсім не розчиняється при кімнатній температурі, суміш нагрівають до кипіння. При поганій розчинності в розчинах кислот і лугів твердий залишок фільтрують, а фільтрат нейтралізують. Це помутніння вказує на кислі або основні властивості речовини.
Необхідну інформацію дає також прожарювання. Для цього на кришку тигля поміщають 0,1 мл рідкої або на кінчик шпателя 0,01 г твердої речовини і вносять кришку або шпатель у верхню або бічну частину безбарвного полум'я пальника, поступово пересуваючи їх в більш гарячу частину. Якщо речовина горить майже блакитним полум'ям, то в ньому присутні кисневмісні функціональні групи. Жовте полум'я, яке світиться (коптить), характерне для речовин, багатих вуглецем (ароматичні і ацетиленові вуглеводні). Відзначають також, повністю згорає речовина чи ні. В останньому випадку речовина може бути сіллю органічної кислоти (карбонової, сульфо- і т.д.). Забарвлення полум'я може вказати також на природу катіона.
Після очищення речовини за допомогою хроматографії переконуються в її індивідуальності. При хроматографуванні невідомої речовини потрібно використовувати декілька систем елюентів. У цьому випадку наявність тільки однієї основної плями з великим ступенем вірогідності свідчить про наявність у пробі єдиної органічної речовини.
Відкриття функціональних груп. Визначивши приблизно клас аналізованої речовини за наслідками дослідження фізичних властивостей і розчинності, проводять якісні реакції на передбачувані функціональні групиНаприклад, встановлено, що рідка, безбарвна речовина не містить азоту, сірки і галогенів, добре розчиняється у воді, має нейтральну реакцію. Така речовина може бути спиртом, альдегідом або кетоном, тому для уточнення проводять якісні реакції на спиртову, альдегідну і кетонну групи. Ідентифікація конкретних сполук. Після встановлення класу досліджуваної сполуки, можна оцінити число атомів у ній і зіставити константи даної сполуки з константами окремих членів ряду, узятими з довідкової літератури. Виписують з них ті, які найбільш близько підходять до властивостей досліджуваної речовини. Для остаточного встановлення, яка з вибраних речовин відповідає аналізованій, останню перетворюють у характерні для цього класу похідні.
67. Елементний аналіз.
За зовнішнім виглядом не завжди можна відрізнити органічні речовини від неорганічних. Для попереднього визначення використовують прожарювання. Органічні речовини за прожарювання перетворюються на газуваті сполуки й повністю випаровуються. Більшість неорганічних речовин за прожарювання утворюють сухий залишок.Після одержання органічну речовину перевіряють на чистоту(за фізичними константами) та проводять якісний елементний аналіз. Визначивши якісний склад, а потім кількісний, виводять найпростішу формулу сполуки.. Потім за допомогою якісних реакцій визначають функціональні групи.
В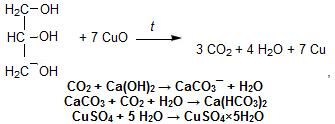 ідкриття
Карбону і Гідрогену. У
суху пробірку з газовідвідною трубкою
вносять суміш досліджуваної речовини
(гліцерол) з купрум(ІІ) оксидом і
закріплюють її горизонтально. Кінець
газовідвідної трубки занурюють у другу
пробірку, заповнену вапняною або
баритовою водою. Спочатку суміш нагрівають
повільно, потім дужче. Помутніння
вапняної води свідчить про наявність
СО2. Надлишок СО2 розчинює осад. Якщо
досліджувана речовина містить Гідроген,
то утворюється вода, яку можна визначити,
пропускаючи пару у пробірку робірку з
безводним CuSO4.
Утворюється мідний купорос голубого
кольору .
ідкриття
Карбону і Гідрогену. У
суху пробірку з газовідвідною трубкою
вносять суміш досліджуваної речовини
(гліцерол) з купрум(ІІ) оксидом і
закріплюють її горизонтально. Кінець
газовідвідної трубки занурюють у другу
пробірку, заповнену вапняною або
баритовою водою. Спочатку суміш нагрівають
повільно, потім дужче. Помутніння
вапняної води свідчить про наявність
СО2. Надлишок СО2 розчинює осад. Якщо
досліджувана речовина містить Гідроген,
то утворюється вода, яку можна визначити,
пропускаючи пару у пробірку робірку з
безводним CuSO4.
Утворюється мідний купорос голубого
кольору .
В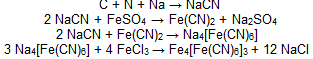 ідкриття
Нітрогену. в)
загальний метод відкриття Нітрогену
(проба Ласеня) можна використовувати
для будь-якихсполук. Дослід проводити
у витяжній ша-фі!Упробірку вміщують
~0,1 г досліджуваної речовини (сечовини,
амінокислоти або ін.) та шматочок (з
півгорошини) очищеного від гасу
металічного натрію. Суміш обережно
нагрівають на газовому пальнику до
появи білого диму, потім пробірку
забирають з полум’я(проходить бурхлива
реакція). Після реакції пробірку ще
трохи нагрівають, а потім охолоджують,
суміш розчиняють у 3…4 мл дистильованої
води, доливають свіжопрокип’ячений
насичений розчин FeSO4
і підкислюють соляною кислотою. Утворення
берлінської лазурі (синього кольору)
після додавання 2…3 крапель FeCl3
свідчить про наявність Нітрогену в
сполуці. Реакції, які протікають при
цьому, схематично можна записати так:
ідкриття
Нітрогену. в)
загальний метод відкриття Нітрогену
(проба Ласеня) можна використовувати
для будь-якихсполук. Дослід проводити
у витяжній ша-фі!Упробірку вміщують
~0,1 г досліджуваної речовини (сечовини,
амінокислоти або ін.) та шматочок (з
півгорошини) очищеного від гасу
металічного натрію. Суміш обережно
нагрівають на газовому пальнику до
появи білого диму, потім пробірку
забирають з полум’я(проходить бурхлива
реакція). Після реакції пробірку ще
трохи нагрівають, а потім охолоджують,
суміш розчиняють у 3…4 мл дистильованої
води, доливають свіжопрокип’ячений
насичений розчин FeSO4
і підкислюють соляною кислотою. Утворення
берлінської лазурі (синього кольору)
після додавання 2…3 крапель FeCl3
свідчить про наявність Нітрогену в
сполуці. Реакції, які протікають при
цьому, схематично можна записати так:
Відкриття Сульфуру. б) загальний метод, придатний для всіх сульфурвмісних сполук, базується на спалюванні речовини в присутності металічного натрію. При цьому утворюється натрій сульфід.У суху пробірку кладуть ~0,1 г досліджуваної речовини і шматочок(з півгорошини) очищеного від гасу та сполуки окиснення металічного натрію. Суміш нагрівають у витяжній шафі. Пробірку охолоджують. Одержаний залишок, який містить Na2S, розчиняють у 3…4 мл дистильованої води. Розчин розливають у дві пробірки і в одній з них відкривають Сульфур плюмбум(ІІ) ацетатом, у другій – натрій нітропрусидом.Відкриття галогенів. загальний метод дає можливість відкривати Хлор, Бром, Йод. Він ґрунтується на сплавленні речовини з металічним натрієм. Утворюється натрій галогенід, який відкривають за допомогою арґентум) (нітрату (утворення осаду):NaHal + AgNO3 ® AgHal ¯ + NaNO3У суху пробірку вміщують ~0,1 г досліджуваної речовини та шматочок (з півгорошини) очищеного металічного натрію. Суміш обережно нагрівають на газовому пальнику у витяжній шафі. Пробірку охолоджують, розплав, який містить галогенід натрію, розчиняють у 2…3 мл води і додають НNO3. У пробірку наливають розчин арґентум) нітрату(І , з’являються помутніння або осад арґентум)(І галогеніду: AgCl – білий, AgBr – жовтуватий, AgІ – жовтий.
65. Підготовка речовини до аналізу
Методи виділення та очищення залежать від фізичних та хімічних властивостей органічних речовин. Найбільш поширеними у лабораторній практиці є методи перекристалізація, перегонка, возгонка , хроматографічні методи.
Перекристалізацію застосовують для очищення твердих речовин. Цей метод ґрунтується на різниці у розчинності речовини, яку очищають, у певному розчиннику за різних температур: без нагрівання та при нагріванні до температури кипіння розчинника.
Процес перекристалізації здійснють у кілька стадій: вибір розчинника ( експериментально розчинник вибирають так: невелику пробу речовини вміщують у пробірку, додаючи до неї кілька крапель розчинника. Якщо речовина розчиняється без нагрівання, такий розчинник не придатний для перекристалізації. Вибір розчинника вважається правильним, якщо речовина погано розчиняється в ньому без нагрівання, добре – при кипінні, а при охолодженні гарячого розчину відбувається її кристалізація.); приготування насиченого гарячого розчину (ефективне очищення сильно забруднених речовин можливе за допомогою різноманітних адсорбентів (активоване вугілля, силікагель тощо).); "гаряче" фільтрування(для відокремлення від механічних домішок та адсорбенту гарячий розчин фільтрують); охолодження розчину; відділення кристалів, що утворилися; промивання кристалів чистим розчинником; висушування.
Перегонка- це процес розділення рідкої суміші на окремі компоненти, внаслідок нагрівання суміші до кипіння і конденсації її парів у холодильнику у вигляді дистиляту.
Перегонка з водяною парою застосовується для виділення і очищення нерозчинних і малорозчинних у воді високо киплячих речовин, які розкладаються при перегонці при атмосферному тиску. Це найефективніший метод очищення таких речовин від смолистих домішок, а також розділення природних масел і смол на фракції. Перегонку з парою можна застосовувати і для розділення суміші високо киплячих речовин, з яких лише одна відганяється з парою.
Сублімація (возгонка)- це процес випаровування твердої речовини з наступною конденсацією її пари у твердий стан, минаючи рідкий. Цим способом користуються для очищення твердих речовин, маючих достатньо великий тиск пара при порівняно невеликій температурі. Возгонка приміняється особливо у тих випадках, коли очищення твердої органічної речовини від смольних сумішей шляхом кристалізації не досягає мети. Частіше всього возгонка - відносно повільний процес. Швидкість возгонки прямопропорційна тиску пара речовини при даній температурі і зворотньопропорційна зовнішньому тиску в приборі. Чим менша різниця між зовнішнім тиском і тиском пари речовини, тим швидше возгонка. Крім того швидкість возгонки прямо пропорційна величині поверхні випаровуваної речовини і тому препарат треба дуже тонко змільчувати.
Хроматографія- процес розділення компонентів суміші на основі різниці у рівномірному розподіленні їх руху поміж двох фаз, що не змішуються; де одна рухома, а інша - нерухома.
Хроматографічне розділення можливе лише у тому випадку, якщо компоненти зразка будуть розчинятися у рухомій фазі та будуть взаємодіяти з нерухомою фазою. В основі цієї взаємодії лежать сорбційні процеси. Хроматографічні методи розділяються за механізмом взаємодії між фазами, за технікою експерименту, агрегатному стану рухомої та нерухомої фаз. За агрегатним станом рухомої фази хроматографію ділять на газову та рідинну.