Материал: магістерський іспит з хімії 1
74. Поляризація молекул
Полярність молекули кількісно оцінюють величиною дипольного моменту μ, що є добутком абсолютного значення заряду електрона на відстань між центрами позитивного і негативного зарядів у молекулі μ = ql.
Поляризація молекул полягає у розподілі в просторі спільної електронноїхмари. Якщо має місце s-зв’язок двохатомної молекули з однаковими атомами,то електронна хмара розподіляється симетрично відносно ядер обох атомів.
Ефектом Зеємана називають розщеплення спектральних ліній і рівнів енергії в зовнішньому магнітному полі.
У 1913 р. Й. Штарк відкрив явище розщеплення спектральних ліній в електричному полі для бальмерівської серії гідрогену. Це явище розщеплення енергетичних рівнів і спектральних ліній під дією на речовину зовнішнього електричного поля називають ефектом Штарка.
Є два основні методи магнітного резонансу: ЯМР – ядерний магнітний резонанс; ЕПР – електронний парамагнітний резонанс.
ЯМР - резонансне поглинання або випромінювання електромагнітної енергії речовиною, що містить ядра з ненульовим спіном у зовнішньому магнітному полі, на частоті ν (званою частотою ЯМР), зумовлене переорієнтацією магнітних моментів ядер. ЕПР — фізичне явище, яке полягає у вибірковому поглинанні електромагнітних хвиль парамагнітною речовиною, яку помістили у зовнішнє магнітне поле.
Методом ЕПР можна досліджувати лише частинки, які мають парамагнітний момент, тобто частинки, для яких сумарний електронний спін не дорівнює 0 – наприклад радикали. Метод ЯМР застосовують для дослідження речовин, що мають магнітні ядра (ядра з ненульовим спіном): 1Н, 13С, 31Р і т.д.
Електромагнітне випромінювання будь-якої природи може характеризуватися спектром коливань, на які можна розкласти його за довжиною хвилі або частотою. Залежно від характеру поширення електромагнітних хвиль оптичні спектри поділяють на спектри випромінювання, поглинання, розсіювання і відбиття.Оптичні спектри спостерігають візуально за допомогою спектральних приладів і фіксують, як правило, фотографічним способом або за допомогою фотоелементів. Спектри можуть бути:а) суцільними, що охоплюють широкий діапазон довжин хвиль; б) лінійчастими, що складаються з окремих спектральних ліній певної довжини хвилі X; в) смугастими — набір окремих смуг, що належать певному інтервалу довжин хвиль.
Спектроскопія - вивчає закономірності взаємодії електромагнітної радіації з речовиною, яка супроводжується процесом поглинання, випромінювання і розсіювання світла. Із спектроскопічних даних можна одержати інформацію, як про структуру і властивості молекул, так і про сили міжмолекулярної взаємодії, а відповідно про будову речовини в цілому.Спектральними термами атомів називаються енергетичні рівні електронної підсистеми атомів, переходи між якими визначають спектри випромінювання й поглинання.
Потенціал Морзе - функція потенційної енергії електростатичного поля, запропонована американським фізиком Філіпом Морзе як наближення для енергії двохатомної молекули.
75. Електричні та магнітні властивості атомів і малих молекул
Дипольний момент – це векторна величина, яка характеризує асиметрію розподілу позитивного та негативного зарядів в електрично нейтральній системі.
Природною одиницею вимірювання дипольного заряду в системі СІ є кулон-метр.
Дія електричного поля на нейтральну систему зарядів й електричне поле, створене електрично нейтральною системою, визначаються в першу чергу дипольним моментом.
Нейтральні системи зарядів з відмінним від нуля дипольним моментом називають диполями.
Квадрупольний момент визначає поведінку поля, створеного системою зарядів, на великій віддалі у випадку, коли система загалом нейтральна, а її дипольний момент дорівнює нулю. Така система зарядів називаєтьсяквадруполем.
78. Математична модель хімічних перетворень
Тепловим ефектом реакції називають кількість теплоти, що виділяється або
поглинається в реакції при сталому тиску або об'ємі, причому продукти реакції мають таку жтемпературу, що й вихідні речовини, і відсутні інші види робіт, крім роботи проти силзовнішнього тиску. Якщо реакція ендотермічна, то знак теплового ефекту додатний, аекзотермічна - від'ємним.
Закон Гесса: тепловий ефект хімічної реакції не залежить від шляху реакції, тобто від проміжних стадій, а визначається лише початковим і кінцевім станами системи. Рівняння є математичними виразами закону Гесса.
QV= ΔU (зміна внутрішньої енергії) Qp = H2 - H1 = ΔH (зміна ентальпії)
Для охарактеризування процесів, що відбуваються в закритих системах, введено термодинамічні функції стану: ізобарно-ізотермічний потенціал (вільна енергія Гіббса) G - критерій напрямку процесу при сталих Т і р; та ізохорно-ізотермічний потенціал (вільна енергія Гельмгольца) F - критерій напрямку процесу при сталих Т і V.
Хімічної рівновага – стан системи, коли швидкості прямої і зворотної реакцій однакові, а концентрації реагентів та продуктів реакції, які при цьому називають рівноважними, не змінюються. Хімічна рівновага є найбільш стійким станом хімічної системи, до якого вона прагне самодовільно. Хімічна рівновага – динамічна, вона характеризу- 83 ється сталістю рівноважних концентрацій (чи парціальних тисків) всіх учасників реакції при сталості зовнішніх умов і мінімальному значенні енергії Гіббса чи енергії Гельмгольца. Кількісною характеристикою стану рівноваги є константа рівноваги – величина, що дорівнює відношенню добутку концентрацій продуктів реакції, узятих у ступенях, що дорівнюють їх стехіометричним коефіцієнтам, до добутку концентрацій регентів у ступенях, рівних їх стехіометричним коефіцієнтам.
Хімічна рівновага носить динамічний характер і під час змін умов, за яких перебігає реакція, зміщується. Зміщення рівноваги відбувається за принципом Ле-Шательє: «Якщо на систему, що знаходиться в рівновазі чиниться зовнішня дія, то рівновага зміщується у бік тієї з двох протилежних реакцій, яка послаблює цю дію».
Характерною ознакою хімічних перетворень є зміна внутрішньої енергії реагуючих речовин і енергії системи в цілому. Під час хімічних реакцій відбувається перебудова електронних структур атомів, іонів і молекул, яка призводить до виділення або поглинання теплоти, світла, електричного струму та інших форм енергії.
Енергія кристалічної решітки, дорівнює роботі, яку необхідно витратити, щоб розділити і відокремити один від одного частини, що утворюють кристалічну решітку .
Змінення ентальпії ΔН системи внаслідок взаємодії речовин за умов постійного тиску називається тепловий ефект хімічної реакції. Теплові ефекти залежать від агрегатного стану речовин і умов, за яких відбувається реакція. Саме тому в термохімічних рівняннях зазначають агрегатний стан речовин; якщо це спеціально не зазначено, то теплові ефекти вказані для стандартних умов. Якщо речовина існує в кількох алотропних видозмінах, то за нуль приймають теплоту утворення модифікації, стійкої за стандартних умов (графіт, білий фосфор, ромбічна сірка тощо). Для інших модифікацій простих речовин теплоти утворення відрізняються від нуля і мають назву теплот поліморфних перетворень.
Теплота реакції — кількість теплоти, виділена або поглинена системою при протіканні в ній хімічної або фазової (фазового перетворення) реакцій, за умови відсутності якої-небудь іншої роботи, крім роботи розширення.
81. Біогенний обмін речовин у біосфері
Система – це сукупність взаємопов'язаних елементів (компонентів). Залежно від кількості елементів (компонентів), що входять в систему, зв'язки між ними можуть бути прості і складні, прямі і зворотні.
Найбільш організованою системою є біосфера. Біосфера – це відкрита, складна, багатокомпонентна, саморегульована система живої речовини і мінеральних сполук, яка утворює зовнішню оболонку системи. Біосфера – це частина планети, в якій відбувається життя. Головна властивість біосфери як природної системи – це виникнення живої речовини і підтримка умов її існування.
Області розповсюдження живої речовини у біосфері обмежуються п'ятьма параметрами і є необхідними умовами існування живої речовини в біосфері:
- певна кількість СО2 і О2;
- наявність води в рідкій фазі;
- термічний режим;
- наявність елементів мінерального живлення;
- солоність природних вод
Головні складові біосфери:
- біомаса живої рослинності, яка здатна шляхом фотосинтезу і зростання організму фіксувати і перетворювати космічну енергію в хімічну потенційну і зберігати її у вигляді органічних сполук;
- ґрунтовий покров, що забезпечує існування рослин: існування кореневої системи, водне, вуглекислотне, азотне, мінеральне живлення, тепловий режим, накопичення запасів енергії у вигляді гумусу;
- біомаса тих організмів, які живуть на ґрунті і у ґрунті консументів і редуцентів (тварин, простих мікроорганізмів), які споживають фітомасу і доводять її до повної мінералізації;
- гідросфера;
- атмосфера;
- літосфера (оболонка біогенних осадочних порід).
У природі відбувається постійний рух і пересування хімічних елементів. Переміщення хімічних елементів в навколишньому середовищі називають міграцією. Виділяють типи міграції хімічних елементів: механічну, фізико-хімічну, біогенну і техногенну.
Механічна міграція полягає в перенесенні хімічних елементів у складі мінералів гірських порід, органічних залишків без їх хімічної зміни. Це знос мінералів по схилах гір, перенесення їх текучими водами у вигляді суспензій, сольових потоків і т. д.
Фізико-хімічна міграція полягає в переміщенні, перерозподілі хімічних елементів у земній корі і на її поверхні.
Біогенна міграція полягає в участі хімічних елементів у малому біологічному кругообігу.
Техногенна міграція – це переміщення хімічних елементів у будь-якому вигляді за результатом діяльності людини (перекачування води, нафти, газів, транспортування вугілля, нафти, руди, деревини та ін.).
82. Жива речовина біосфери та її біогеохімічні функції
Жива речовина – це сукупність організмів планети або якої-небудь її частини, виражена в одиницях маси, енергії, інформації. Жива речовина володіє двома головними особливостями – організацією (структурою) і здатністю функціонувати.
Організація або структура живої речовини включає поняття про кількість елементів (компонентів), що входять в систему, а також взаємодію цих компонентів. Наприклад, дерево – як жива речовина – має декілька рівнів організації. Найнижчий рівень – це клітка; наступний рівень організації – лист, потім гілка і, нарешті, дерево – найбільш високий рівень організації цієї системи. Чим більше компонентів входить в речовину, тим вона складніша і тим більш складною інформацією володіє.
Друга особливість живої речовини – це здатність функціонувати. Функціонування – це сукупність реакцій, що виникають у живому організмі у відповідь на зовнішні дії, які приводять до зміни внутрішніх властивостей речовини, тобто до його саморозвитку. Чим складніша жива речовина, тим більшою інформацією вона володіє, тим складніше йде її функціонування, тим більша кількість процесів в ній відбувається.
Найбільше скупчення живої речовини спостерігається на межі трьох оболонок: атмо-, гідро- і літосфери (у тропічних лісах)
80. Каталіз та каталізатори. Вивчення впливу неорганічних каталізаторів та ферментів на перебіг хімічних реакцій.
Каталіз – це хімічні реакції, що відбуваються за участю каталі зорів. Одні каталізатори значно прискорюють реакцію – позитивний каталіз, інші – сповільнюють – негативний.
Каталізаторами називають речовини, що змінюють швидкість хімічних реакцій. Механізм дії каталізаторів звичайно пояснюють утворенням проміжних сполук з однією з реагуючих речовин. Так, якщ реакцію А + В = АВ, що відбувається пвільно, проводити за наявністю каталізатора К, то каталізатор вступатиме в хімічну взаємодію з однією з вихідних речовин з утворенням неміцної проміжної сполуки: А + К = АК.
Види каталізу: гомогенний, гетерогенний, мікрогетерогенний. При гомогенному каталізі реагуючі речовини і каталізатор утворюють однофазну систему – газувату або рідку, між каталізатором і речовинами, що реагують, немає поверхні поділу (розклад пероксиду гідрогену за участю розчину солей). При гетерогенному каталізі реагуючі речовини і каталізатор утворюють систему з різних фаз (окиснення аміаку (газ) за наявності платини (тверда)). Мікрогетерогенний — процеси відбуваються у рідкій фазі за участі колоїдних часток металів в якості каталізатора. Механізм кислотно-основного каталізу полягає у протолітичній взаємодії між каталізатором і реагуючою речовиною, внаслідок чого утворюється нестійка проміжна сполука, яка потім розкладається на продукт реакції і каталізатор. Прикладами кислотно-основного каталізу можуть бути реакції гідролізу естерів, етерифікації, гідролізу полісахаридів, ізомеризації, галогенування, конденсації та ін.
Ферменти – це речовини білкової природи, які виробляються клітинами живих організмів і значно збільшують швидкість біохімічних процесів. Характерна особливість дії ферментів є висока чутливість активності ферментів до зовнішніх умов – рН середовища і температури. Ферменти активні лише в достатньо вузькому інтервалі рН і температури, причому для ферментів характерна наявність в цьому інтервалі максимуму активності при деякому оптимальному значенні рН або температури; по обидві сторони від цього значення активність ферментів швидко знижується. Активний центр — особлива частина молекули ферменту, що визначає його специфічність і каталітичну активність.
Для кожного фермента існує певне значення рН середовища, в якому він виявляє максимальну активність. Для пепсину воно становить 1,5 – 2,0, аргінази – 9,5 – 10,0. Проте, більшість ферментів організму людини мають оптимум рН, наближений до нейтрального. Вплив рН на активність фермента пов’язаний із іонізацією функціональних груп амінокислотних залишків білкової молекули, що забезпечує оптимальну конформацію активного центра. Відхилення рН від оптимальних величин порушує іонізацію функціональних груп в активному центрі фермента.
Складні реакції реалізуються через одночасне здійснення декількох перетворень, перебіг яких є незалежним один від одного. Складні реакції можуть бути: оборотними (реакції в яких можливе одночасне перетворення реагентів у продукти так само і взаємодія продуктів з творенням реагентів: хА + уВ ↔ mC + nD); паралельними (реакції, в яких реагенти одночасно зазнають перетворення у декількох напрямках); ланцюговими (реакції, що складаються з ряду взаємопов’язаних стадій, коли частинки, що утворились в результаті кожної стадії, генерують наступні стадії); послідовними (речовини, що утворюються в результаті І-ої стадії цієї реакції є вихідними речовинами для іншої); спряженими (реакції виду А + В = С, А + Д = Е характерною особливістю їх є те, що якщо І-а реакція може йти самостійно, то ІІ-а йде тільки сумісно з першою).
79. Молекулярна енергетика горіння
Адіабатична температура горіння - температура, до якої нагріваються продукти горіння за умов: 1) вихідна горюча суміш знаходиться за стандартних умов; 2) горіння відбувається з надлишком чи нестачею повітря; 3) дисоціація продуктів горіння не відбувається; 4) немає тепловтрат від системи в навколишнє середовище.
Реакція окислення є екзотермічною (тобто відбувається з виділенням тепла) і за певних умов може самоприскорюватися. Цей процес самоприскорення реакції окислення з переходом її в горіння називається самозайманням.Ланцюговий механізм реакції пояснюється перерозподілом надлишкової енергії, яка реалізується в реакції наступним чином: запас хімічної енергії, зосередженої в молекулі продукту первинної реакції, передається однією з реагуючих молекул, яка переходить у хімічно активний стан. Тепловим самозайманням називається явище виникнення горіння, викликане самонагріванням, що виникло при тривалому впливі зовнішнього нагріву речовини вище за температуру самонагрівання.
Адіабатичним називають такий процес, який відбувається без теплообміну системи з навколишнім середовищем. Для здійснення адіабатичного процесу треба оточити систему такою оболонкою, яка не пропускає теплоти, але заважає тому, щоб система виконувала роботу або робота виконувалась над системою. Таку оболонку називають адіабатичною.
Процес вибухового перетворення залежно від природи вибухових речовин, способу ініціювання та ряду інших умов може протікати у формі детонації або у формі горіння. Горіння - процес поширення вибухового перетворення, обумовлений передачею енергії від одного шару вибухової речовини до іншого шляхом теплопровідності і випромінювання тепла газоподібними продуктами.Швидкість процесу горіння в сильному ступені залежить від зовнішніх умов, і в першу чергу від тиску в навколишньому просторі. Зі збільшенням тиску швидкість горіння зростає; при цьому горіння може в деяких випадках переходити у вибух (детонацію). Детонація (повна) - процес поширення вибухового перетворення, обумовлений проходженням ударної хвилі у вибуховій речовині і протікає для даної речовини за даних умов з постійною швидкістю, вимірюваної тисячами метрів в секунду.
Реакція окислення водню.При підпалюванні водень реагує з киснем і горить світло-блакитним, майже непомітним полум’ям. Якщо до отвору пробірки з сумішшю водню та повітря піднести полум’я, то станеться вибух, якому передує свист. О2 + 2Н2 → 2Н2О{\displaystyle {\mathsf {O_{2}+2H_{2}\rightarrow {}\ 2H_{2}O}}}, реакція протікає із вибухом.Суміш двох об'ємів водню та одного об'єму кисню називається гримучим газом. Здатність суміші водню з киснем або повітрям вибухати використовують для перевірки водню на чистоту, тобто на присутність у ньому повітря (кисню).
Розглянемо
протікання екзотермічної хімічної
реакції в закритій посудині, стінки
якого протягом всього процесу підтримуються
при фіксованій температурі T0 .
Температура газу в початковий момент
часу також дорівнює Т0.
Швидкість тепловиділення в посудині
дорівнює q+
= QW
швидкість тепловіддачі в стінки судини
дорівнює
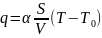 де α
- коефіцієнт тепловіддачі; S і V
- площа
поверхні і об'єм посудини. Кінетика
процесу описується рівнянням
де α
- коефіцієнт тепловіддачі; S і V
- площа
поверхні і об'єм посудини. Кінетика
процесу описується рівнянням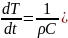 (ρ
- теплоємність при постійному обсязі).
(ρ
- теплоємність при постійному обсязі).