Материал: Летние практики_ocred

таблл. 1, рецепт которого был разработан в Институте биологии внут- ренних вод РАН(г(.г Борок, Ярославская обл..)).
Таблица 1
Раствор для фиксации фитопланктона
|
Раствор I1 |
| |
Раствор IIП |
|
|
|
| |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[KIКТ |
|
|10 |
г |
|Хромовая кислота 1%--ная|| |
|
3 |
| |
|
||
|
|
5 см |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|550[5H2O |
0 |
см’[ |
Ледяная уксусная кислота |
|10 |
см" |
|
|||||
|
|
|
|
3 |
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|I |
| |
5г |
|Формалин 40%-ный |
|80 |
3 |
|
|
|||
|
см |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Оба раствора сливают и хранят в темном месте.. При применении йодных фиксаторов в клетках водорослей хорошо обнаруживаются пиреноидыы, жгутикиики, окрашивается слизь, исчезаюют вакуоли у боль- шинства имеющих их сине-зеленых. Наличие формалина в составе консерванта позволяет хранить пробу длительноевремя.
Фиксированную пробу после отстаивания концентрируют отсасы- ванием воды с помощью трубки-сифона с загнутыгнутым на 2 см вверх
концомм, затянутыатянутым газоом № 70 −— 76, или с помощью устройства для
автоматического концентрирования фитопланктонных проб. Устройй- ство состоит из двух расположенныхна разных уровнях штативов (на
верхний штатив устанавливается сосуд с концентрируемой водой, на
нижний −— мерный цилиндр, в который отсасывается вода), сифона, трубок и двух вентилей (ообычного и соленоидного)). Это устройство позволяет создать стандартные условия концентрирования, а также отрегулировать скорость отсасывания водытаким образом, чтобыисс- ключить возможность попадания в фильтрат мелких видов фитоо- планктона. После отсасывания остаток пробыв 30−—80 мл переливают
всклянку. Туда же сливают воду после ополаскивания стенок сосуда,
вкотором происходило осаждение.
Широкое применение в гидробиологии получил метод мембранн- ной фильтрациир ции, который способствует быстрой концентрации проб и дает возможность просматривать фитопланктон в живом состоянии. Для сгущения фитопланктона пригодны фильтры № 5 с диаметром
10
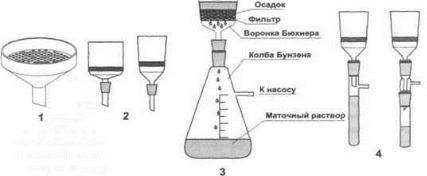
Воронку укрепляют на колбе Бунзена, которуую через верхнийтуу-
бус шлангом соединяют с вакуумным насосом. Возможно соединение
нескольких воронок одной трубкой или системой гибких шлангов,, что
позволяет фильтровать сразу несколько проб.
Пробу фильтруют до определенного объема, оставляя над фильь- тром столбик воды высотой 1| см, или до момента, когда воды над осадком уже нет, но фильтр еще остается влажнымм. Затем планктон осторожно смывают с фильтра мягкой кисточкой и просчитывают в
счетной камере. Желательно сразу после фильтрации просмотреть
живой материалиал, что позволяет не только обнаружить нежные формы водорослей, но и определить общее состояние фитопланктона.. Если нет необходимости просматривать живую пробу, фильтр помещают в пенициллиновую склянку объемом 20 млл, заливаюют 5−—10 мл фильтраа-
та и консервируют до слабо-желтого цветаа. В этом случае за 30 мин до
фильтрации можно провести предварительнульную консервациацию пробы несколькими каплями фиксатора, что предотвратит деформацию во- дорослей на фильтре, которая может иметь место при фильтрации жии- вой пробы.
Опыт работы специалистов показываетывает, что довольно близкие ре-
зультаты с отстойнытойным концентрированием получаются только в слу- чае двойной фильтрации пробы. Причина состоит в том, что при обильных пробах только двойная фильтрация обеспечивает равномерр- ное распределение отфильтрованных водорослей по площади фильь- траа. При одноразовой фильтрации происходит сбивание организмов фитопланктонав кучи или даже склеиваниеих на фильтре.
Изучать организмыв живом состоянии можнои в случае применее- нии метода центрифугированиярования, который позволяет быстро осадить водорослии. Однако применять его при количественном учете фитоо- планктона не следует, так как центрифуга не осаждает сине-зеленые водоросли, содержащие газовые вакуоли, и организмзмы с меньшей плотностью, чем вода..
Важным моментом отбора проб является ее этикетированиеие. Каж- дая проба должна быть снабжена этикеткойй, на которой указывают название водного объекта, номер станциии, глубину, орудие лова, дату
12
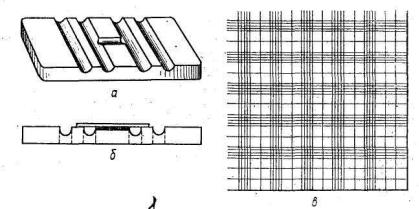
поверхность на два больших внешних поля и три узких внутренних полосыы. Два внешних поля предназначеныдля нанесениязаписей,,в то время как полосы отшлифованыи отполированы. Центральная полоса (дно камеры) имеет два ряда гравированной сетки для подсчета, отде- ленные пропилами. Дно камерыв центральной полосе на 0,1 мм ниже двух внешних полос. Таким образом, когда пластина закрывается по- кровным стеклом, междуним и центральной полосой образуется зазор
в 0,1 ммм..
Уравнение для определения количества частиц (клеток) универ- сальное. Количество частиц (клеток) в 1 мкл объема равно количеству подсчитанных частиц (клеток))., деленному на площадь проанализироо- ванных квадратов (мм”),2 глубину камеры (мм) и разведение. Наприи- мер, просчитано 528 клеток водорослейв пяти больших квадратах при разведении анализируемой водыв 200 раз. Для подсчета количества
водорослей в 1| мкл воды необходимо 528 разделитьнана0,2 (пять квад-
ратов соответствуютвуют площади 0,2 мм”),2 на 0,1 (глуббина камеры0,1 мм) и на разведение 1:200. Получаем 5,28 млн. клеток водорослей в 1| мкл
анализируемойводы..
Процесс подсчета очень трудоемок и требует большой тщательноо-
сти. Существенным моментом является наполнение камеры, перед которыорым проба тщательно перемешивается продуванием воздуха че- рез капилляр с входным отверстием не менее 2 мм.. Этим же капилляя- ром вносится одна-две капли фильтрата, и камеру быстро закрывают покровнымстеклом.. Пробе дают осесть в течение нескольких минут..
При количестве водорослей несколько сотен и десятков тысяч в 1 мл можно ограничиться просчетом пяти –— десяти больших квадратов из 225-ти имеющихсяв камере, при нескольких тысячах клеток в 1| мл необходимо просчитать всю камеру. Определение численности водо- рослей лучше проводить в камерах разных объемов.. Так, крупные и колониальные формыпланктона просчитывают в камерах большого
3
размера (не менее 0,05 −— 0,1 см*), для остальных видов подходят и бо-
3
лее мелкие(0,01 и 0,02 см°)).
Размерыклеток водорослей могут быть важным систематическим признакомм. Клетки измеряют с помощью окуляра-микрометра. Цену
14