Материал: Летние практики_ocred
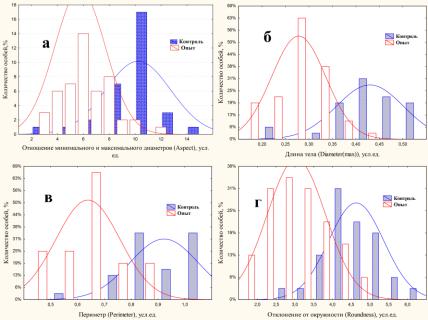

ствия от ЭМП сотовой связи на простейших. 20%-ное отклонение от нормыуказывает на высокую токсичность облучения для инфузорийорий.
2.4. Применение клеточного МТТТ-тест- а для анализа нарушения метаболической активности ветвистоусысых
ракообразных РарйшаDaphnia тагпаmagna
Для анализа цитотоксичности физических и химических факторов окружающей среды применяют методод, в котором используют водо- растворимый 3-(4,5-димет- тилтиазол-2-ил)--2,5.5-дифе- нил-2Н--тетразо- лиум бромид (МТТТ) [3]. МТТ--метод интегрально отражает количество активных форм кислорода,,в том числе, короткоживуущих супероксид- анион-радикалов, инактивациацию сукцинатдегидрогеназ и других мито- хондриальных оксидазаз, соотношение живыхи мертвых клеток и рабо- ту системемы антиоксидантных ферментов. Метод основан на способноо- сти митохондриальных дегидрогеназ восстанавливать проникающийв клетки бесцветный МТТТс образованием нерастворимого окрашенного формазана. Последуюдующщий фотометрический анализ позволяет сопо- ставить изменение оптической плотности раствора по отноношению к контроллю с изменением количества жизнеспособных клеток и оценить эффективностноь цитотоксического действия анализируемого соединее-
нияНИЯ.
Выполнение работы по оценке нарушения метаболической ак- тивности у дафний
1. Растворить 10 мг МТТТв 2 мл водопроводной дехлорированной воды (5 мгг/мл)). Тщательно перемешать (с помощью магнитной мее- шалки) 1| ч в темноте и поместить в термостат на 15 −— 20 мин(37 о°С)). Отфильтровать раствор через мембранный фильтр с диаметром
22 мкм под давлением (водяным или масленыеным насосом)).. Разлить на
аликвотыпо 1| мл в эппендорфыы. Хранить при −—20 °ºС..В качестве рас- творителя формазана использоватьдиметилсульфоксид (ДМСО).)
Для проведения измерения потребуютсяэппендорфынана1,5, млл, ав- томатические микропипетки, наконечники для микропипеток, гомоге- низаторы и 96-луночный планшет, планшетный иммуноферментный
36

анализатор, например, StatЗа FaxЕах 2100 −— AwarenessА\хагепе$$ TechnologyТесбпо]осу, США. VISУ\У!5--модель(рис(рис..12)).
Рис. 12. Планшетный иммуноферментныйанализатор StatЗа FaxЕах 2100
2. В четыре биологические пробирки с 15 мл культуральной воды
отобрать по 20 дафний односуточного возраста. Облучить каждый об-
разец на источнике γу-квантов в однойизиздоз:: 0,1; 1 и 10 Грр. Контрольь-
ную пробиркувсегда держать в тех же условиях,,что и опытные,,но не облучать.
3. После облучения пересадить дафний в стеклянные лабораторные стаканысо 150 мл культуральной среды. Все подписать.
4. После облучения культивировать трое —– четверо суток в климаа- тостате при освещении 12 ч/12 ч свет.:тьма, температуре 20 о°С и по-
стоянном вентилировании.
5. По истечении времени инкубации пересадить дафний из каждой дозовойи контрольной групп в эппендорфы(1,(1,5 мл))..
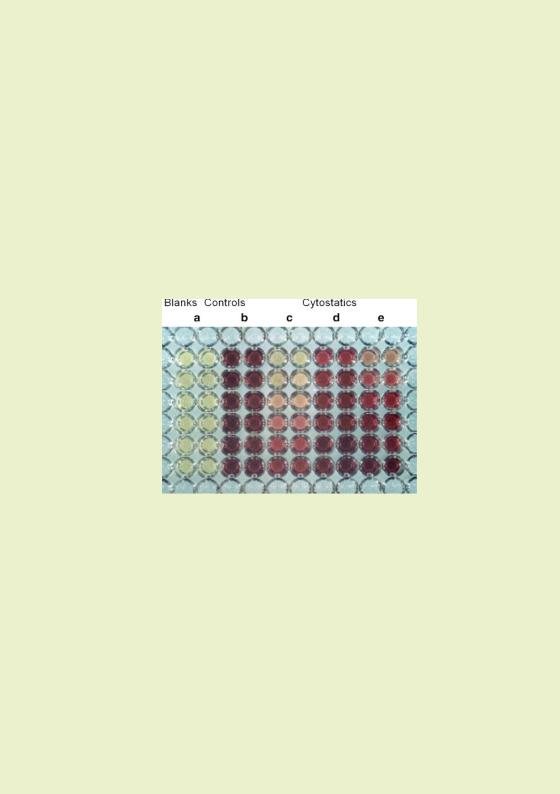
6. Откачать воду из каждой пробы и тут же добавить по 200 мкл раствора МТТ.
7. Инкубировать не менее 60 мин при комнатной температуре без дополнительной аэрации.
8. По истечении времени инкубации откачать МТТ и добавить по 200 мкл ДМСО. Выдержать 10 мин до растворения гранул формазанаана.
9. Гомогенизировати ов ь пробы до состояния суспензии гомогенизато- ром для эппендорфов, не забывая менять гомогенизаторы между об- разцамии.
37

−— где ОПоO –- оптическая плотностьв облученном образцеце; ОПф —–
средняя оптическая плотность фоновых проб; ОП‚к-– оптическая плот- ность в необлученном контроле.
15. Полученные результаты проанализировать с помощью стати- стических программм для выявления уровня радиационного воздей- ствия. 20%--ное отклонения от нормыуказывает на высокую токсич- ность облучения для дафний.
Литература
1. Биологический контроль окружающей среды:: биоиндикация и
биотестирование:: уч. пособие для студентов вузов / Под редд. ОП.П. Мее-
леховой и Е.И.. Сарапульцевой.. Изд..3-3е-е. дополн..и испр. -—– М.:.: Акадее- мия, 2010. 288– с.
2. Левич А..П.., Булгаков Н..Г. Информационнно-аналитическа- я си-
стема «Экологический контроль природной среды по данным биоло- гического и физико-химического мониторинга»». OnОп-Ппеline доступ http://ecogradeр://есоста4е.61bioо.msuтзи.ru/indexги/ш4ехПит.html
3. Сарапульцева Е.И.., Рябченко Н..И.., Иголкина Ю.В.В.,. Иванник Б.П. Использование клеточного биохимического метода для биотести-
рования inт vivoуй?о радиационного загрязнения окружаюющей среды// Ра-
диационная биология.. Радиоэкологияогия, 2013.. Т.. 53.. №66.. С.634-638..
4. Тирас Х..П.., Асланиди К.Б. Тест-система для неклинического
исследования медицинской и экологической безопасности на основе
регенерации планарий:: учебб.-метод. пособие. –- Тула:: ТулГУ, 2013..-–
64с..
5. Ускалова Д..В.., Баранова М..М.,. Сарапульцева Е.И.., Иголкина
Ю..ВВ. Применение метода компьютерной морфометрии в исследова-
нииНИИ биологического действия низкоинтенсивного рарадиочастотного излучения на простейших // Биомедицинская радиоэлектроника, 2013,
№33. С.48-522.
6. Цаценко Л.В. Обнаружение ионов тяжелых металлов в воде мее- тодом аналитического биотестирования с помощью ряски малой
(LemnaГетпа minorттог LГ..) / Труды Кубанского государственного аграрного
университета, 2014. № 48. С. 106-1133.
39