Материал: Лекарственные растения семейства розоцветных (Rosaceae)
Сбор, заготовка, сушка. Плоды черемухи собирают для лечебных целей полностью созревшими, срывая кисти целиком. Сушат любым доступным способом: на солнце, рассыпая кисти тонким слоем, либо в печах и сушилках при температуре 50-60 °С. После сушки кисти перетирают, при этом сухие костянки отделяются от плодоножек. С помощью решет плоды очищают от плодоножек и прочего мусора [3].
Химический состав. Плоды черемухи содержат дубильные вещества, органические кислоты (яблочная, лимонная), жирные масла, гликозиды (амигдонитрилгликозид, пруназин), сахара, фитонциды, аскорбиновую кислоту, флавоноиды.
Все эти действующие вещества формируют основу химического состава черемухи обыкновенной (черемухи кистевой) [3].
Действие и применение. Отвар плодов черемухи благодаря наличию в них дубильных веществ и органических кислот оказывает выраженное вяжущее и противовоспалительное действие. Зрелые плоды черёмухи оказывают закрепляющее, вяжущее <#"818917.files/image001.gif">
Поперечный срез корня кровохлебки
- пробка
- кора
- камбий
- древесина
- друзы оксалата кальция
- сердцевинные лучи
- лубяные волокна, 9 - либриформ
.3 Определение влажности
Под влажностью сырья понимают потерю в массе за счет гигроскопической влаги и летучих веществ, которую определяют в сырье при высушивании до постоянной массы.
Аналитическую пробу сырья измельчили до размера частиц около 10 мм, перемешали и взяли две навески массой 3-5 г, взвешенные с погрешностью +/- 0,01 г. Каждую навеску поместили в предварительно высушенную и взвешенную вместе с крышкой бюксу и поставили в нагретый до 100-105 град. С сушильный шкаф. Время высушивания отсчитывали с того момента, когда температура в сушильном шкафу вновь достигла 100- 105 град. С. Первое взвешивание листьев, трав и цветков проводят через 2 ч, корней, корневищ, коры, плодов, семян и других видов сырья - через 3 ч.
Высушивание проводили до постоянной массы. Постоянная масса считается достигнутой, если разница между двумя последующими взвешиваниями после 30 мин высушивания и 30 мин охлаждения эксикаторе не превышает 0,01 г.
Влажность сырья (X) в процентах вычисляют по формуле:
= ![]() ,
где
,
где
- масса бюкса до высушивания
![]() - масса бюкса
после высушивания
- масса бюкса
после высушивания
Х - влажность сырья [2].
|
№ бюкса |
m пустого бюкса, г |
m до высушивания, г |
m после первого высушивания, г |
m после второго высушивания, г |
|
1 |
28, 420 |
31, 435 |
31, 160 |
31,150 |
|
2 |
32, 680 |
35, 685 |
35, 380 |
35, 370 |
m=31, 435 - 28, 420 = 3, 015
![]() = 31, 150 - 28, 420
= 2, 73
= 31, 150 - 28, 420
= 2, 73
X (1) = ![]() =
=
![]() =
9, 45 %=35, 685 - 32, 680 = 3, 005
=
9, 45 %=35, 685 - 32, 680 = 3, 005
![]() = 35, 370 - 32, 680
= 2, 69
= 35, 370 - 32, 680
= 2, 69
X (2) = ![]() =
=
![]() =
10, 48 %
=
10, 48 %
![]() =
= ![]() =9,
965 %
=9,
965 %
2.4 Определение золы общей
Около 1 г препарата или 3-5 г измельченного лекарственного растительного сырья (точная навеска) поместили в предварительно прокаленный и точно взвешенный фарфоровый тигель, равномерно распределяя вещество по дну тигля. Затем тигель осторожно нагрели, давая сначала веществу сгореть или улетучиться при возможно более низкой температуре. Сжигание оставшихся частиц угля провели при возможно более низко температуре; после того как уголь сгорел почти полностью, увеличили пламя.
Прокаливание вели при слабом красном калении (около 500 град. С) до постоянной массы, избегая сплавления золы и спекания ее со стенками тигля. По окончании прокаливания тигель охладили в эксикаторе и взвесили.
Золу определяют по формуле:
= ![]() ,
где
,
где
![]() - масса пустого
тигля
- масса пустого
тигля
![]() -масса тигля с
навеской
-масса тигля с
навеской
![]() - масса тигля
после третьего высушивания
- масса тигля
после третьего высушивания
|
m тигля без навески |
36, 535 |
|
m тигля с навеской до прокаливания, г |
39, 54 |
|
|
37, 315 |
|
|
36, 909 |
|
|
36, 859 |
= ![]() =
=
![]() =
11, 99%
=
11, 99%
2.5 Качественные реакции
Кровохлебка лекарственная относится к растениям,
содержащим дубильные вещества.

2.5.1 Экстракция дубильных веществ из сырья
Для проведения экстракции дубильных веществ
взяли 5г измельченного сырья и поместили в колбу вместимостью 250мл. Залили 100
мл кипящей воды и прокипятили на плитке в течение 5 минут; профильтровали
полученное извлечение через складчатый фильтр и использовали его для проведения
качественных реакций [4].
.5.2 Качественное определение дубильных веществ в растительном сырье
а) Качественная реакция с желатином

К 1 - 3 мл извлечения добавили 2-3 капли 1% раствора желатина в 10% раствор натрия хлорида [4].
►При добавлении желатина раствор помутнел,
что свидетельствует об образовании желатинатов.
б) Реакция с калия бихроматом

К 1 - 3 мл извлечения добавили 3 - 5 капель 5% раствора калия бихромата [4].
► При добавлении бихромата калия раствор потемнел, что свидетельствует о наличии таннидов.
в) Реакция со свинцом основным уксуснокислым
К 2 - 3 мл извлечения добавили раствор свинца основного уксуснокислого [4].
►При добавлении свинца основного уксуснокислого образовался осадок, что свидетельствует о наличии таннидов.
г) Реакция с реактивом Фолина-Дениса (смесь
фосфомолибденовой и фосфовольфрамовой кислот)

К 3 мл извлечения добавили 3-5 капель реактива Фолина-Дениса и небольшое количество кристаллического натрия карбоната [4].
►При добавлении реактива образовалась молибденовая синь, что свидетельствует о наличии таннидов.
д) Реакция с солями железа (III)

К 1 - 3 мл извлечения добавили 3 капли 1% раствора железоаммонийных квасцов [4].
►При добавлении железоаммонийных квасцов раствор окрасился в черно-синий цвет, что свидетельствует о наличии гидролизуемых дубильных веществ.
е) Реакция с нитритом натрия в кислой среде
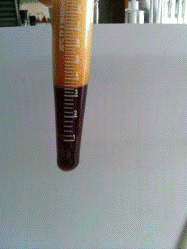
К 2 мл извлечения прибавили несколько кристалликов натрия нитрита и 0,5 мл хлористоводородной кислоты [4].
►Образовалось красное окрашивание, что свидетельствует о наличии гидролизуемых дубильных веществ.
ж) Реакция с раствором ванилина в кислой среде:

К 1 мл извлечения прибавили несколько капель раствора ванилина в кислой среде [4].
►Раствор окрасился в красный цвет, что
свидетельствует о наличии дубильных веществ.
.6 Количественное определение
. Около 2 г (точная навеска) измельченного сырья, просеянного сквозь сито с диаметром отверстий 3 мм, поместили в коническую колбу вместимостью 500 мл, залили 250 мл нагретой до кипения воды, взвесили колбу на электронных весах и кипятили с обратным воздушным холодильником на электрической плитке с закрытой спиралью 30 мин. при периодическом перемешивании.
. Жидкость охладили до комнатной температуры, колбу вновь взвесили, недостающий вес восполнили водой и процедили около 100 мл извлечения в коническую колбу вместимостью 200-250 мл через вату так, чтобы частицы сырья не попали в колбу.
. Затем отобрали 25 мл полученного извлечения в другую коническую колбу вместимостью 750 - 1000 мл, прибавили 500 мл воды, 25 мл индигосульфокислоты и титровали при постоянном перемешивании раствором калия перманганата (0,02 моль/л) до золотисто-желтого окрашивания.
. Параллельно провели контрольный опыт. Взяли 25
мл индигосульфокислоты, прибавили 525 мл воды и титровали калия перманганатом
(0,02 моль/л) до золотисто-желтого окрашивания.


Переход цвета раствора до и после титрования
. Содержание дубильных веществ Х в процентах в
пересчете на абсолютно-сухое сырье вычислили по формуле:
Х=![]() ,
где
,
где
- объем раствора калия перманганата (0,02 моль/л), израсходованного на титрование извлечения, мл;- объем раствора калия перманганата (0,02 моль/л), израсходованного на титрование в контрольном опыте, в мл;
,004157 - количество дубильных веществ, соответствующее 1мл раствора калия перманганата (0,02 моль/л) в пересчете на танин, г;- масса сырья, г;- потеря в массе при высушивании сырья, %;
- общий объем извлечения, мл;
- объем извлечения, взятого для титрования, мл.
реакции. Титрование ведут медленно, при сильном разбавлении экстракта
(Почему?), до появления золотисто-желтого окрашивания [2].
|
V - объем титранта, мл |
17 |
|
|
10 |
|
М - масса сырья, г |
2, 001 |
|
W - потеря в массе при высушивании, % |
9, 965 |
Х=![]()
Выводы к главе 2 (экспериментальная часть)
Исследованы микроскопические признаки корней и корневищ кровохлебки лекарственной в соответствии с требованиями ФС 42-1082-76
Проведен микроскопический анализ корней и корневищ кровохлебки лекарственной, результаты которого могут служить микроскопическими признаками при определении подлинности сырья.
Проведен фармакогностический анализ корней и корневищ кровохлебки лекарственной, который включил в себя следующие показатели:
а) определение влажности корней и корневищ кровохлебки лекарственной, показатель которой при подсчете средней арифметической составил 9, 965%
б) определение общей золы, показатель которой в результате подсчета составил 5, 62%
. Основываясь на результатах проведенного
фармакогностического анализа корней и корневищ кровохлебки лекарственной, можно
сделать вывод о том, что данное растение соответствует требованиям,
предъявляемым к лекарственному растительному сырью.
Заключение
Представители семейства Розоцветные (Rosaceae) относятся к одним из самых многочисленных и повсеместно распространенных растений. Кроме многообразия видов, этому семейству свойственно и разнообразие химического состава у отдельных представителей. Поскольку применение того или иного растения зависит от его химического состава, растения семейства Розоцветных обладают явным преимуществом.
Лекарственные растения этого семейства применяются при лечении самых разнообразных заболеваний совершенно различной этиологии: артериальная гипертензия, аритмии, простудные заболевания, ангина, геморрой, гинекологические заболевания, атеросклероз, мочекаменная болезнь, нарушения обмена веществ, злокачественные новообразования, малокровие, подагра, кишечные расстройства, ревматизм, эпилепсия, язвенная болезнь, поражения кожи, энтериты, гастриты, колиты, стоматиты, фурункулез.
Вещества, которые содержатся в лекарственных растениях, ближе человеческому организму, так как являются природными; они благоприятно влияют на здоровье без выраженных побочных эффектов, быстро метаболизируются и выводятся из организма.
Изучив лекарственные растения семейства
Розоцветных было установлено, что лекарственные растения, рассмотренные в
работе, содержат большое количество биологически активных веществ, благодаря
чему и оказывают свое специфическое действие.
Список использованной литературы
Варлих В.К. Лекарственные растения России / В.К. Варлих - Равновесие, 2005.-672 с.
Государственная фармакопея РФ - 11-е издание - М.: Научный центр экспертизы средств медицинского применения, 1987, том 1.
Государственная фармакопея РФ - 11-е издание - М.: Научный центр экспертизы средств медицинского применения, 1987, том 2
Гринкевич Н.И. Химический анализ лекарственных растений / Н.И. Гринкевич, Л.Н.Сафронич - М: Высшая школа, 1982.-176 с.
Гришина Е.И Фармакогнозия / Е.И.Гришина, И.С. Погодин, Е.А. Лукша - Омск:, 2008. - 1067 с.
Ильина Т.А. Лекарственные растения России / Т.А. Ильина - Эскмо, 2006. - 192 с.
Лавренов В.К. Современная энциклопедия лекарственных трав / В.К. Лавренов, Г.В. Лавренова - Нева, 2009.- 272 с.
Муравьева Д.А. Фармакогнозия: учебник / Д.А. Муравьев, И.А. Самылина, Г.П. Яковлев - М: Медицина, 2002.- 652 с.
Пронченко Г.Е. Лекарственные растительные средства / Г.Е. Пронченко, И.А. Арзамасцев, А.П.Самылиной - М.: ГЭОТАР - МЕД, 2002. - 288 с.
Путырский И.Н., Универсальная энциклопедия лекарственных растений / И.Н. Путырский, В.Н.Прохоров - Книжный дом, 2000.- 656 с.
Яковлева Г.П. Лекарственное сырье растительного и животного происхождения. Фармакогнозия: учебное пособие / Г.П. Яковлева. - СПб.: СпецЛит, 2006. - 845 с.