Материал: Лаба КЭФ
ПРАКТИЧЕСКИЕ РАБОТЫ
Работа 1. Изучение влияния кислотности водного раствора на ионное состояние молекулы рифабутина методом капиллярного электрофореза
Рифабутин – полусинтетический антибиотик, обладающий широким спектром антибактериального действия, активный в отношении многих грамположительных и грамотрицательных бактерий, в том числе в отношении
M. tuberculosis.
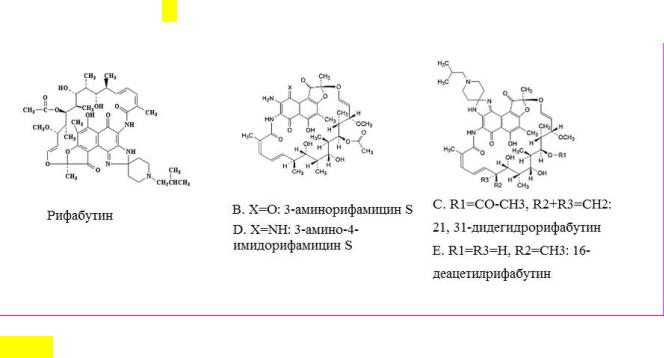
Химическая формула молекулы рифабутина и его родственных примесей представлена на рис.1.
Рис. 1. Химическая формула молекулы РБ и его родственных примесей
Молекула рифабутина имеет несколько центров ионизации, что определяет ее электрофоретическое поведение. Изменение заряда частицы рифабутина при изменении кислотности среды влияет на скорость миграции частицы в капилляре. Константы кислотности молекулы рифабутина составляют: рКа1 = 4,0-5,0, рКа2 = 6,5-7,5 и рКа3 = 9,7-11.
В сильнокислой среде электрофоретическая подвижность частицы рифабутина остается постоянной и не изменяется до достижения значения рН
≈ 4. В данной области рН РБ существует в виде дикатиона (рКа азота имидазольной группы - 4,0-5,0). При дальнейшем повышении рН (диапазон рН от 4 до 8) происходит депротонирование азота имидазольной группы. Это приводит к уменьшению положительного заряда катиона рифабутина,
следствием этого является уменьшение его электрофоретической подвижности. При рН около 8 электрофоретическая подвижность частицы совпадает со скоростью ЭОП: в этой области происходит отщепление протона от гидроксильной группы в остатке нафталина (рКа=6,5-7,5) и образуется цвиттер-ион рифабутина. Далее, по мере увеличения щелочности раствора, на частице рифабутина появляется и увеличивается отрицательный заряд. В этой области рН происходит депротонирование азота пиперидиновой группы молекулы (рКа=9,7-11).
Цель лабораторной работы: изучить зависимость электрофоретического поведения молекулы антибиотика рифабутина от кислотности ведущего электролита, используя метод капиллярного электрофореза.
Для этого следует получить электрофореграммы рифабутина при различных значениях рН ведущего электролита и сделать выводы о знаке заряда соответствующих ионных форм молекулы.
Используемое оборудование и условия КЭ
Оборудование. В эксперименте по КЭ используется система капиллярного электрофореза «Капель 105М» («Люмэкс», Россия), оборудованная спектрофотометрическим детектором и кварцевым капилляром (внутренний диаметр 75 мм, эффективная длина 50 см, общая длина 60 см). Применяется программное обеспечение «Эльфоран» («Люмэкс», Россия).
Для измерения рН растворов используют рН-метр со стеклянным универсальным электродом.
Растворы центрифугируют с использованием лабораторной центрифуги
MiniSpin, Eppendorf.
Весы аналитические.
Посуда: колбы мерные, 100 мл и 25 мл; стаканчики стеклянные, 25 мл; пипетки и дозаторы, пластиковые пробирки 1,5 мл, флаконы стеклянные пенициллиновые.
Реагенты и растворы:
Растворы для промывки капилляра: 1н HCl и 0,5 н NaOH
Рабочий раствор рифабутина в спирте этиловом (5 мг в мл). 0,1% водный раствор ДМСО – метка ЭОП
Сухие соли для приготовления ведущих электролитов: NaH2PO4· H2O и Na2HPO4 · 2H2O.
Условия КЭ: капилляр термостатировать при 25°С;
напряжение, подаваемое на капилляр +20 кВ;
длина волны детектирования 214 нм;
ввод пробы гидродинамический (30 мБар, 5 секунд).
Выполнение работы
Промывка и кондиционирование капилляра
Включают прибор. После автотестирования прибора управляющей программой задают температуру термостата 25°С. Перед началом работы проводят промывку капилляра последовательно водой, 1н HCl, водой, 0,5 н NaOH, водой. Длительность каждой промывки - 5 минут. Для этого по 500
мкл каждого из растворов отбирают в отдельную пробирку, используя дозатор. После этого от пробирок ножницами отрезают крышки и устанавливают пробирки с растворами в карусель автосемплера прибора в соответствии со следующим порядком:
Слева: в гнездо 6 – пробирка в раствором 1н HCl, в гнездо 7 – пробирка с дистиллированной водой, в гнездо 8 – пробирка с раствором 0,5 н NaOH.
Справа: в гнездо 7 – пробирка с дистиллированной водой, в гнезда 8 и 9
вставляют пустые пробирки для слива.
После составления программы промывки, запускают ее и приступают к приготовлению растворов ведущих электролитов.
Приготовление буферных растворов для заполнения капилляра
Для заполнения капилляра необходимо приготовить четыре фосфатных буферных раствора (ведущий электролит) с различной кислотностью и одинаковой молярной концентрацией – 0,05М. Кислотность растворов должна лежать в интервале значения от рН 4 до рН 9,5. В двух мерных колбах объемом по 100 мл готовят два водных раствора с концентрациями 0,05 М из солей: NaH2PO4· H2O и Na2HPO4 · 2H2O. Необходимые для приготовления растворов навески солей взвешивают в сухих пенициллиновых флаконах на аналитических весах. После перенесения навесок в колбы объем колб до меток доводят дистиллированной водой и содержимое колб хорошо перемешивают.
Измеряют рН приготовленных растворов, используя рН-метр, и полученные значения записывают на колбах. Растворы с нужными значениями рН готовят в стеклянных стаканчиках, смешивая на магнитной мешалке два приготовленных раствора, и следят за кислотностью смешиваемого раствора с помощью рН-метра. Стремятся к тому, чтобы в итоге иметь четыре раствора,
кислотность которых приблизительно соответствовала следующим значениям рН: 4,7; 5,6; 8,0: 9,5. При необходимости до нужного значения рН смешиваемого на магнитной мешалке раствора можно довести растворами
NaOH (0,5M) или HCl (1M), добавляя их аккуратно по каплям.
Перед заполнения ими капилляр все буферные растворы следует дегазировать центрифугированием. Для этого каждым из четырех приготовленных растворов заполняют по 3 пробирки. Объем растворов в каждой пробирке –
500 мкл. Следует точно дозатором отмерять объем растворов для того, чтоб центрифуга была заполнена равномерно. Все пробирки устанавливают в центрифугу, соблюдая симметрию их расстановки на центрифужной
платформе. Далее включают программу центрифугирования при 12000
об/мин, 5 мин.
После окончания программы три пробирки с первым из растворов (самый щелочной) устанавливают в карусель автосемплера установки КЭ: две слева
(в 9 и 10 гнездо), одну справа в 10 гнездо.
Приготовление анализируемой пробы рифабутина и проведение КЭ
В пробирку дозатором вносят 10 мкл рабочего раствора рифабутина и 10 мкл
0,1% водного раствора ДМСО. Добавляют 480 мкл дистиллированной воды
(так, чтоб общий объем раствора в пробирке соответствовал 500 мкл) и
тщательно перемешивают полученный раствор в пробирке, предварительно закрыв ее крышкой. Далее ножницами отрезают крышку от пробирки с пробой и пробирку вставляют в гнездо «1» левого отделения автосемплера прибора «Капель».
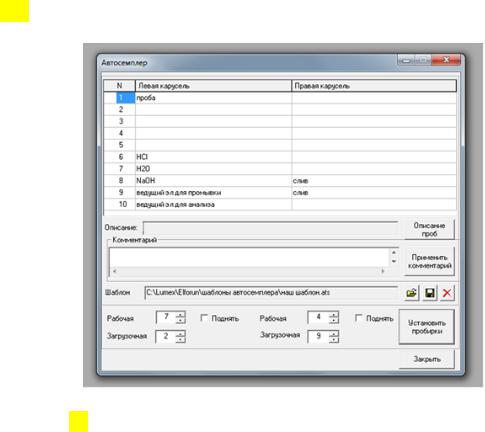
После того, как все необходимые для кондиционирования капилляра и проведения анализа растворы установлены в устройство автосемплера,
заполнение автосемплера должно соответствовать схеме, представленной на рис___.
Рис.___Схема установки пробирок в автосемплер системы КЭ