Материал: Комментарии к слайдам
СЛАЙД 17
Механизм действия гидрофильного гормона на клетку-мишень,
обладающую рецептором – ионным каналом
Второй тип рецепторов, воспринимающих воздействие гидрофильных гормонов на клетки-мишени – это так называемые «рецепторы – ионные каналы». Рецепторы этого типа являются белками, имеющими четыре трансмембранных фрагмента. Соединение молекулы гормона с таким рецептором приводит к открытию трансмембранных ионных каналов, благодаря чему ионы электролитов по градиенту концентрации могут поступать в протоплазму клетки. С одной стороны это может приводить к деполяризации клеточной мембраны (так, например, происходит с постсинаптической мембраной клеток скелетной мышцы при передаче сигнала с нервного моторного волокна на мышцу), а с другой – ионы электролитов (например, Са++) могут активировать серин-тирозиновые киназы или фосфолипазы, и за счет их ферментативного действия на внутриклеточные белки и липиды вызывать изменение клеточного метаболизма.
СЛАЙД 18
Механизм действия гидрофильного гормона на клетку-мишень,
обладающую рецептором, сопряженным с G-белком
Третий тип рецепторов, воспринимающих воздействие гидрофильных гормонов на клетки-мишени, определяется как «рецепторы, сопряженные с G-белками» (сокращенно – GPCR – “G-protein coupled receptors”).
С помощью G-рецепторов на исполнительный клеточный аппарат передаются сигналы, возбуждаемые нейропередатчиками и нейротрансмиттерами (адреналин, норадреналин, ацетилхолин, серотонин, гистамин и др.), гормонами и опиоидами (адренокортикотропин, соматостатин, вазопрессин, ангиотензин, гонадотропин, некоторые факторы роста и нейропептиды и др.). Кроме того, G-рецепторы обеспечивают передачу химических сигналов, воспринимаемых вкусовыми и обонятельными рецепторами.
G-рецепторы, равно как и большинство мембранных рецепторов, состоят из трех частей: внеклеточная часть, часть рецептора, погруженная в мембрану клетки и внутриклеточная часть, контактирующая с G-белком. При этом внутримембранная часть рецептора – это полипептидная цепочка, пересекающая мембрану семь раз.
Функцией G-белков является открытие ионных каналов (т.е. изменение концентрации ионов электролитов в протоплазме клеток-мишеней) и активация белков-посредников (внутриклеточных мессенджеров). В результате с одной стороны происходит активация соответствующих ферментных систем клетки (протеинкиназ, протеинфосфатаз, фосфолипаз), а с другой, фосфорилированные белки, обладающие мощной ферментативной активностью, приобретают возможность проникнуть в ядро клетки и там фосфорилировать и активировать белки, участвующие в транскрипции генов и мРНК. В конечном итоге, метаболизм клетки меняется как за счет ферментативных превращений внутриклеточных белков, так и благодаря биосинтезу новых белков.
СЛАЙД 19
Основные пути нарушения функции желез внутренней секреции
В дополнение к материалу, представленному на кадре 11, следует указать следующие пути нарушения функции желез внутренней секреции:
1. Непосредственное повреждение ткани эндокринной железы патогенным агентом.
Наиболее частым фактором, непосредственно повреждающим железы внутренней секреции, являются сосудистые расстройства. Так, например, изменение интенсивности секреции гормонов передней долей гипофиза нередко возникают при длительном спазме сосудов, питающих эту железу. Сахарный диабет часто развивается в результате атеросклеротических изменений в артериях pancreas. Тромбоз артерий надпочечников или кровоизлияния в их ткань приводят к проявлениям той или иной степени выраженности их недостаточности и т.д.
Расстройства функции эндокринных желез могут быть вызваны инфекционным агентом (например, тиреоидиты – воспаления щитовидной железы, имеющие инфекционную природу; сахарный диабет – в результате инфицирования организма вирусом Коксаки и др.).
Важным фактором, повреждающим эти железы, являются опухоли. Одни опухоли оказывают на ткань желез деструктирующее действие, что ведет к их гипофункции. Другие, имеющие железистое строение, свойственное данной железе (аденомы), являются гормонопродуцирующими и обладают высокой, зачастую не контролируемой инкреторной активностью и тем самым резко повышают содержание данного гормона в крови. К таким опухолям относится, например, инсулома, которая продуцирует инсулин и вызывает у больного периодическое возникновение состояния гипогликемической комы. Гормонопродуцирующей опухолью является феохромоцитома - новообразование из хромаффинной ткани, которая периодически выбрасывает в кровоток огромные количества адреналина, вызывая высочайшие по уровню артериального давления гипертонические кризы.
Воспалительные процессы, поражающие эндокринные железы, угнетают их функцию и могут вызвать серьезные гормональные дисфункции, как бывает, например, при воспалениях яичников.
К факторам непосредственного повреждения ткани эндокринных желез относятся и их механические травмы.
2. Очень частым фактором развития эндокринных расстройств является нарушение нормального влияния эндокринных желез друг на друга, которое может быть как непосредственным, так и опосредованным – через включение промежуточных механизмов.
К первому типу таких расстройств принадлежат эндокринные дисфункции, вызванные изменениями регулирующего влияния гипоталамо-гипофизарной системы. Как известно, гипофиз выделяет ряд гормонов, стимулирующих деятельность других желез внутренней секреции, в частности, щитовидной железы, надпочечников, половых желез. Вместе с тем, активность гипофиза находится в тесной зависимости от выработки гипоталамусом рилизинг-факторов, вызывающих усиление выработки гипофизом этих гормонов. Таким образом, гипоталамо-гипофизарная система является регулятором деятельности всей эндокринной системы, и нарушение этой регуляции неизбежно повлечет за собой изменение деятельности и других желез внутренней секреции.
Второй тип расстройств, возникающих на этом пути, заключается в том, что, например, усиление функции одной из эндокринных желез вызывает в организме такие изменения, которые инициируют изменение деятельности другой железы внутренней секреции, что может в дальнейшем привести к расстройству ее функции. Характерным примером в этом отношении является возникновение сахарного диабета при гиперпродукции передней долей гипофиза соматотропина. Последний является ингибитором гексокиназы – ключевого фермента процесса углеводного обмена, под воздействием которого осуществляется фосфорилирование глюкозы. Этот фермент активируется инсулином. В условиях подавления активности гексокиназы соматотропином возникает компенсаторная гиперфункция -клеток Лангергансовых островков поджелудочной железы, в процессе которой инсулярный аппарат pancreas истощается, что и ведет к развитию абсолютного вторичного сахарного диабета.
3. Третий путь – нейрогенный. Деятельность желез внутренней секреции, как, впрочем, и других органов, находится под контролем регуляторных центров нервной системы. Нарушения этой регуляции, равно как и возникновение патологических состояний в различных отделах ЦНС, может вызвать и расстройство деятельности желез внутренней секреции. Так, например, считается, что приблизительно у 80% больных базедовой болезнью причиной развития заболевания является психическая травма или длительное невротическое состояние. Хроническое нервное напряжение играет чрезвычайно важную роль в развитии сахарного диабета и т.д. Эти неврогенные влияния в основном реализуются через изменение интенсивности секреции рилизинг-факторов гипоталамусом.
4. Четвертый путь расстройств деятельности желез внутренней секреции связан с наследственным фактором.
Как уже указывалось в презентации, посвященной патофизиологии углеводного обмена и этиологии и патогенезу сахарного диабета, в возникновении этого заболевания наследственный фактор играет исключительно важную роль. При хромосомных болезнях (синдромы Кляйнфельтера, Шерешевского-Тернера, связанные с патологией половых хромосом) отмечается гипофункция надпочечников и половых желез, развитие организма по интерсексуальному типу и др.
Таковы общие пути развития расстройств деятельности эндокринной системы.
СЛАЙД 21
Гормоны гипофиза
Гипофиз - нижний мозговой придаток, расположенный на основании черепа в гипофизарной ямке турецкого седла, состоит из двух долей: передней – железистой (аденогипофиз) и задней – нейроглиального происхождения (нейрогипофиз). Аденогипофиз в свою очередь подразделяется на три части: бугорную, дистальную и промежуточную.
В аденогипофизе вырабатываются следующие гормоны:
Соматотропин (соматотропный гормон). Его еще называют гормоном роста. Он оказывает на организм общее анаболическое действие: усиливает синтез белка из аминокислот (путем влияния на объединение рибосом в полисомы, где осуществляется белковый синтез), стимулирует рост и развитие скелета и мышц, а также влияет на углеводный и жировой обмен. Соматотропин обладает видовой специфичностью: для человека активным является лишь гормон, полученный из гипофиза или человека, или человекообразных обезьян.
Кортикотропин (адренокортикотропный гормон). Этот гормон активирует выработку глюкокортикоидов, минералокортикоидов и андрогенов в коре надпочечников и стимулирует выброс адреналина их мозговым слоем. В связи с влиянием его на выброс адреналина, его еще называют адренокортикотропином. Он также мобилизует жиры из жировых депо, способствует окислению жиров, усиливает кетогенез, способствует накоплению гликогена в клетках мышечной ткани. Кортикотропин действует на меланофоры (пигментные клетки) аналогично меланотропину, но значительно слабее.
Тиротропин (тиреотропный гормон). Он активирует функцию щитовидной железы, стимулирует гиперплазию ее железистой ткани и синтез тиреоидных гормонов.
Гонадотропины (гонадотропные гормоны) являются стимуляторами функции половых желез. К гонадотропинам относятся:
- Фоллитропин (фолликулостимулирующий гормон). У женщин он активирует развитие фолликулов яичника, способствует превращению первичных яичниковых фолликулов в везикулярные. У мужчин фоллитропин активизирует сперматогенез. У обоих полов он увеличивает объем половых клеток.
- Лютотропин (лютеинизирующий гормон) способствует овуляции и развитию желтого тела в яичниках.
- Лактотропин (лактотропный гормон). Он активизирует функцию желтого тела, однако, его главным физиологическим эффектом является влияние на молочные железы – стимуляция образования молока и процесса лактации.
Меланотропин (меланотропный, меланофорный гормон) действует на пигментные клетки (меланофоры), стимулирует образование в них пигмента. Этот гормон образуется в промежуточной части аденогипофиза. Следует отметить, что у человека промежуточная (или средняя) доля гипофиза развита слабо и часто в учебниках и руководствах по эндокринологии ее не выделяют, а выработку меланотропина относят к функциям аденогипофиза. Однако, кроме меланотропина в этой доле вырабатывается гормон липотропин, влияющий на липидный обмен, и кортикотропин-подобный иммунный пептид.
Задняя доля гипофиза – нейрогипофиз не обладает самостоятельной секреторной активностью. Специфической составной ее частью являются накопительные нейросекреторные тельца (тельца Герринга), в которых скапливается нейросекрет. Гомоны нейрогипофиза - вазопрессин и окситоцин образуются в супраоптических и паравентрикулярных ядрах передней части гипоталамуса. Продуцируемый в этих ядрах нейросекрет поступает по супраоптическому гипофизарному пути в нейрогипофиз и накапливается в тельцах Герринга.
Вазопрессин стимулирует реабсорбцию воды в почечных канальцах и тем самым способствует уменьшению диуреза. Регуляция секреции вазопрессина осуществляется через тканевые осморецепторы, которые возбуждаются в ответ на изменение осмотического давления в тканях, и баро- и волюмрецепторы, заложенные в крупных кровеносных сосудах и реагирующих на изменение артериального давления и ОЦК. Вазопрессин называют также антидиуретическим гормоном (АДГ).
Окситоцин стимулирует мышцу матки и тем самым - родовую деятельность, регулирует лактацию.
Таковы основные эффекты гормонов гипофиза.
Функция гипофиза находится под контролем гипоталамуса. Вазопрессин и окситоцин вырабатываются непосредственно в ядрах гипоталамуса и накапливаются в нейрогипофизе. Активность аденогипофиза также определяется гипоталамусом. Опыты с повреждением и электрическим раздражением гипоталамической области показали, что функцию аденогипофиза контролирует медиобазальная часть гипоталамуса, где вырабатываются рилизинг-факторы. Здесь же находятся и рецепторы для соответствующих “тропных” гормонов гипофиза. Иными словами, гипоталамическая регуляция функций аденогипофиза осуществляется по принципу и прямой, и обратной связи. Рилизинг - факторы высвобождаются в кровь.
К настоящему времени выделены рилизинг-факторы по отношению ко всем гормонам аденогипофиза. По отношению к некоторым гормонам аденогипофиза выделены рилизинг - ингибирующие гормоны, то есть гипоталамические факторы, угнетающие выработку гормонов в аденогипофизе. Так, соматотропин рилизинг гормон представлен двумя гипоталамическими факторами - стимулирующим и тормозящим секрецию соматотропина: соматолиберином и соматостатином.
Меланотропин-рилизинг-гормон также представлен двумя гипоталамическими факторами: меланолиберином и меланостатином.
СЛАЙД 22
Гормоны надпочечников
Корковый слой надпочечников выделяет гормоны, относящиеся к двум группам: минералокортикоиды и глюкокортикоиды.
Минералокортикоиды, главным из которых является альдостерон, влияют на водно-солевой обмен за счет реабсорбции натрия клетками кортикальных собирательных канальцев почки. При этом, переход натрия в клетки почечных канальцев осуществляется пассивно, по градиенту концентрации, а в кровь – против градиента концентрации и сопровождается затратой энергии. Схема транспорта натрия приводится ниже. Из нее следует, что существует два пути транспортировки: быстрый и медленный. Быстрый путь (секунды, минуты) реализуется после контакта молекулы альдостерона с его рецептором. Связывание с рецептором активирует фосфолипазу С и, через несколько внутриклеточных посредников – мессенджеров, приводит к увеличению концентрации внутриклеточного кальция, что, в свою очередь, включает каскад фосфорилирования и активацию K/Na насоса (активация фермента K/Na – АТФазы). На каждую молекулу АТФ K/Na насос способен переносить против градиента концентрации через мембрану клетки три иона Na и вводить в клетку два иона К. Именно таким способом и происходит реабсорбция Na и выведение К.
Медленный или геномный путь реабсорбции Na (часы и дни) так же начинает свое действие с контакта молекулы альдостерона с его рецептором (ядерным рецептором). Комплекс гормон – рецептор транспортируется в ядро клетки и взаимодействует там с сайтами связывания. Через синтез мРНК и соответствующего белка этот процесс завершается образованием новых K/Na насосов и включением их в клеточную мембрану. Активация K/Na насосов осуществляется по уже описанному «быстрому» пути реабсорбции натрия.
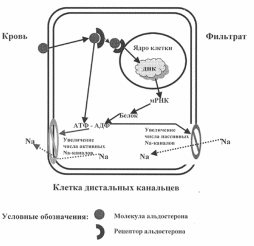
Механизм реабсорбции натрия под влиянием альдостерона
Реабсорбция натрия сопровождается задержкой в организме воды, а также ведет к повышению чувствительности гладкомышечных элементов сосудистой стенки к прессорному влиянию катехоламинов. Таким образом, альдостерон участвует в регуляции уровня артериального давления
Действие на организм глюкокортикоидов отличается чрезвычайным многообразием. Они оказывают влияние на синтез и активность ряда ферментов и важные звенья углеводного, жирового и белкового обмена: способствуют распаду гликогена до глюкозы, стимулируют процессы глюконеогенеза, тормозят липолиз и мобилизацию жира из депо, обладают антианаболическим и катаболическим действием (то есть тормозят синтез и стимулируют распад белков).
Мозговое вещество надпочечников секретирует адреналин, являющийся, в том числе, – и нейромедиатором и оказывающий влияние на многие функции и системы организма, прежде всего, – на сердечно-сосудистую систему.
Без надпочечников организм жить не может. Следует, однако, заметить, что это утверждение относится только к корковому слою надпочечников, поскольку катехоламины (в том числе и адреналин) продуцируются не только мозговым слоем надпочечников, но и хромаффинной тканью, в большом количестве имеющейся в организме, и симпатическими нервными окончаниями.
СЛАЙД 25
Гипер - и гипопродукция соматотропина
Гипофизарный гигантизм и акромегалия
Эти заболевания развиваются или вследствие возникновения эозинофильной аденомы гипофиза (то есть гормонопродуцирующей опухоли, состоящей из эозинофильных гипофизарных клеток), что ведет к избыточной продукции соматотропина, или вследствие избыточной продукции гипоталамусом соматолиберина, который в свою очередь стимулирует секрецию гипофизом соматотропина.
Если указанные изменения происходят в раннем возрасте, когда еще не прекратился рост длинных трубчатых костей, возникает состояние, получившее название гипофизарного гигантизма и выражающееся в общем увеличении размеров и массы тела. Это заболевание встречается преимущественно у мальчиков, достигая своего пика в препубертатном и пубертатном периодах. Такие больные имеют очень высокий рост (свыше двух метров) и большую по массе мускулатуру (поскольку соматотропин обладает общим анаболическим действием, в основе которого лежит усиление синтеза белка). Однако хотя у гигантов мышечная масса увеличена, тем не менее, физически они слабы, что связано, во-первых, с увеличенной тяжестью костей, а во-вторых, со снижением у них уровня энергетического обмена. Последнее, вероятнее всего, происходит потому, что у таких больных имеется та или иная степень инсулярной недостаточности (из-за ингибиции соматотропином гексокиназы, последующей гиперфункции и истощения - клеток Лангергансовых островков pancreas), что снижает энергообразование. Помимо увеличения скелета и мышц, у гигантов отмечается и спланхномегалия, то есть увеличение размеров внутренних органов.
При гигантизме часто встречается ослабление функции половых желез (гипогонадизм), что, по-видимому, связано со сдавление эозинофильной аденомой клеток передней доли гипофиза, ответственных за выработку гонадотропинов. По той же причине может наблюдаться гипофункция и других желез внутренней секреции: щитовидной, надпочечников.
При гигантизме также наблюдается ослабление иммунной защиты организма и, вследствие этого, повышенная чувствительность к инфекционному фактору.
В том случае, если усиление продукции соматотропина развивается в зрелом возрасте, то есть у лиц с завершившемся физиологическим ростом, возникает заболевание, впервые описанное Пьером Мари в 1886 году и получившее название акромегалия. Поскольку в зрелом возрасте диафизарный рост костей уже не возможен из окостенения эпифизарных хрящей, клинические проявления акромегалии будут отличными от таковых при гигантизме. Характерным для данного заболевания является непропорциональное изменение скелета: происходит увеличение черепа, костей и стоп, что обусловлено периостальным ростом этих костей. Одновременно увеличиваются внутренние органы, язык, уши, становится увеличенным и грубым лицо. Кожа утолщена, собирается в складки. Как и при гигантизме, происходит угнетение функции некоторых желез внутренней секреции вследствие нарушения выработки соответствующих “тропных” гормонов гипофиза. Следует заметить, что акромегалия той или иной степени нередко сопровождает такое физиологическое состояние, как беременность, вследствие достаточно глубокой перестройки в этот период эндокринного статуса организма женщины. После родов явления акромегалии практически всегда бесследно исчезают.
Лечение гигантизма и акромегалии должно быть направлено на торможение продукции соматотропина, подавление роста или разрушение аденомы, нормализацию функций эндокринной системы. Основной метод лечения – рентгенотерапия гипофизарной области, возможна криодеструкция опухоли.
Гипофизарный нанизм
Это состояние возникает при гипофункции эозинофильных клеток передней доли гипофиза и определяется или снижением выработки соматолиберина, или усилением секреции соматостатина гипоталамусом.
Гипофизарный нанизм (гипофизарная карликовость) характеризуется маленьким (до 120 см) ростом. О возможности наличия этого состояния говорят в том случае, если при развитии ребенка его рост на 20 – 25% отстает от среднего роста, свойственного данной возрастной группе. Телосложение при этом пропорционально на протяжении всей жизни. Кожа в детстве тонкая и нежная, у взрослых – бледная, морщинистая, с желтоватым оттенком. Поскольку черты лица и в зрелом возрасте остаются мелкими и имеющими детский облик, а кожа становится морщинистой, возникает характерная внешность “старообразного юнца”. Из-за “детского” строения гортани голос сохраняется высоким. Мышечная система недоразвита, сила мышц снижена в связи со снижением анаболического эффекта соматотропина и андрогенов. Интеллект обычно не страдает, но отмечается быстрая умственная утомляемость (равно как и физическая). Половая функция у гипофизарных карликов или нарушается в небольшой степени, или не нарушается вообще, в связи с чем эти больные могут иметь потомство. По наследству гипофизарный нанизм не передается.