Материал: Изучение влияния температуры на нефтеокисляющую активность микроорганизмов-кандидатов в ассоциацию-деструктор
Существуют простые и дифференцированные методы окраски. При простой окраске используют какой-либо один краситель (метиленовый синий, фуксин, генциан фиолетовый), прокрашивается вся клетка. При дифференцированной окраске отдельные структуры клетки окрашиваются разными красителями (окраска по Граму, окраска спор). Метод дифференциациальной окраски микробных клеток основан на различии в химическом составе клеточных оболочек. В клетках одних видов микроорганизмов образуется нерастворимое в спирте соединение йода с основным красителем, а у других видов это соединение появляется временно и после обработки спиртом растворяется. Микроорганизмов первой группы называют грамположительными, второй - грамотрицательными [41].
Техника окраски по Граму. На обезжиренное предметное стекло наносят три тонких мазка разных культур микроорганизмов. Мазки высушивают на воздухе, фиксируют над пламенем горелки и окрашивают в течение 1 мин феноловым раствором генциана фиолетового (или кристаллического фиолетового), держа стекло в слегка наклонном положении. Затем краситель сливают и, не промывая препарат водой, наносят на него на 1 мин раствор Люголя. Стекло держат в наклонном положении. Препарат, не промывая водой, обрабатывают 96%-ным спиртом в течение 15-20 с. Промыв водой, препарат окрашивают фуксином в течение 1 мин. Грамположительные микроорганизмы приобретают темно-фиолетовый цвет, а грамотрицательные окрашиваются в цвет дополнительной окраски (фуксина).
За 24-48 часов до исследования тестовую культуру микроорганизма пересевают со среды хранения на скошенный питательный агар. На следующий день из полученной агаровой культуры с использованием стандарта мутности готовят суспензию тестового штамма в стерильном разбавителе с концентрацией 10(9) кл/мл и десятикратные серийные разведения (по 8 разведение включительно).
Для контроля разбавления из 6 и 7 разведения высевают по 0,1 мл (100 мкл) суспензии прямым поверхностным посевом на чашки с питательным агаром. Из каждого разведения делают по три таких посева. После высева пробирки с разведениями немедленно переносятся в холодильник. Чашки с посевами инкубируют в термостате при 37°С в течение 18 - 24 часов.
В день исследования для каждой серии посевов подсчитывают среднее число колоний, выросшее на трех чашках. При правильно выполненном разведении среднее количество колоний, выросших при посеве 0,1 мл суспензии тестового микроорганизма из 6-го разведения, должно составлять около 100 КОЕ/мл. Соотношение полученных средних значений при посеве из 6 и 7 разведений должно быть близко к 10:1.
В случае, если концентрация микроорганизмов в разведениях значительно отклоняется от расчетной и (или) не соблюдена кратность разведения, данный инокулят тестового штамма не пригоден для дальнейшего использования. Подготовку инокулята необходимо повторить [42].
Для показателей, требующих определения количества внесенных микроорганизмов, рассчитывают посевную дозу.
Посевная доза - объем конкретного разведения, содержащий необходимое для посева количество жизнеспособных клеток тестового микроорганизма. Расчет дозы выполняют, основываясь на ранее определенных концентрациях тестового микроорганизма в 6 и 7 разведениях, исходя из требований, что посев на одну чашку не должен превышать 50 - 100 микробных клеток. При правильно выполненном разведении посевная доза составляет 50 - 100 мкл суспензии из 6 разведения [42].
После расчета посевной дозы определяют необходимое количество повторов посевов (не менее 5) исходя из расчета, что суммарное количество колоний на всех чашках на одной среде должно составлять не менее 200 КОЕ/мл.
Приготовленные суспензии можно использовать,
если они были охлаждены сразу же после приготовления и произведения контрольных
высевов и не хранились более 24 часов. Перед исследованием инокулят следует
тщательно перемешивать, чтобы добиться однородности суспензии микроорганизмов.
2.2.3 Определение роста микроорганизмов при различных температурах
Для наблюдения роста микроорганизмов использовали универсальную агаризованную среду МПА. Это связано с тем, что культивирование с целью изучения роста микроорганизмов на твердой питательной среде позволяет характер роста и произвести визуальную оценку.
Посев испытуемых культур производился на чашки
Петри со стерильной питательной средой методом штриха. Чашку Петри разделили на
4 зоны, в одной зоне сеяли одну культуру, так чтобы в результате в одной чашке
вырастали 4 культуры. Далее инокулированные чашки культивировали при
необходимом температурном режиме. Для культивирования при -5°С, чашки Петри
помещали в холодильник предварительно измерив температуру лабораторным
градусником, для культивирования при +20°С чашки помещали в термостат.
Длительность культивирования 24 часа. Для сравнения роста микроорганизмов при
-5°С и +20°С, испытуемые культуры также культивировались при 37°С (Рисунок 2).
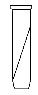
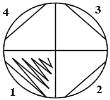
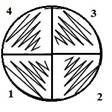
Рисунок 2. Изучение роста микроорганизмов при
температуре +5° С и +20° С
Для изучение роста микроорганизмов при 60° С агаризованную среду следует заменить на жидкую питательную среду МПБ. Температура плавления МПА составляет 50° С, в связи с этим возникают трудности с визуальной оценкой интенсивности роста. Для оценки интенсивности роста используем подсчет общего микробного числа до и после культивирования.
Первым этапом изучения роста микроорганизмов
является активизация культур. Культуры активизировали путем культивирования
испытуемых микроорганизмов в 5 мл МПБ при +30° С 24 часа. Далее из этой
суспензии 1 мл инокулировали в пробирку с 9 мл исходной среды после чего
культивировали при +60° С. Для определения количества клеток внесенных в среду
методом последовательных разведений (методом Коха) со второго и третьего
разведения производился посев на чашки Петри. Далее чашки культивировали 24
часа при +30° С, после чего подсчитывали выросшие колонии и вычисляли КОЕ/мл.
Также ОМЧ определяли после культивирования при +60° С, однако в этом случае на
чашки Петри высевали из нулевого, первого и второго разведения, которые также
культивировали 24 часа при +30° С, после чего подсчитывали выросшие колонии и
вычисляли КОЕ/мл (Рисунок 3).
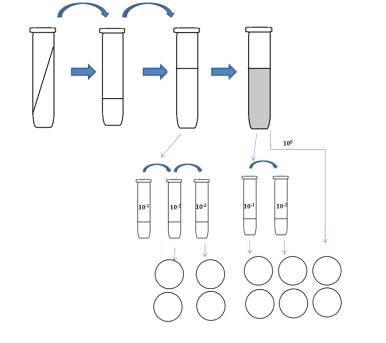
Рисунок 3. Изучение роста микроорганизмов при
температуре +60° С
2.2.4 Определение количества микробных клеток высевом на плотные питательные среды (Метод Коха)
Метод широко применяют для определения численности жизнеспособных клеток в различных естественных субстратах и в лабораторных культурах. В его основе лежит принцип Коха, согласно которому каждая колония является потомством одной клетки. Это позволяет на основании числа колоний, выросших после посева на плотную питательную среду определенного объема исследуемой суспензии, судить об исходном содержании в ней клеток микроорганизмов. Результаты количественного определения микроорганизмов, проведенного по методу Коха, часто выражают не в числе клеток, а в условных, так называемых колониеобразующих единицах.
Определение числа микроорганизмов этим методом включает три этапа: приготовление разведений, посев на плотную среду в чашки Петри и подсчет выросших колоний.
Разведения готовят в стерильной водопроводной воде. Для приготовления разведений стерильную водопроводную воду разливают по 9 мл в сухие стерильные пробирки. Затем 1 мл исследуемой суспензии стерильной пипеткой переносят в пробирку с 9мл стерильной воды - это первое разведение. Для приготовления каждого разведения следует обязательно использовать новую пипетку. Пренебрежение этим правилом приводит к получению ошибочного результата вследствие высокой способности клеток микроорганизмов к сорбции на поверхности стекла.
Полученное разведение тщательно перемешивают новой стерильной пипеткой, несколько раз вбирая в пипетку и выпуская из нее полученную суспензию клеток. Затем той же пипеткой отбирают 1 мл суспензии и переносят во вторую пробирку, получая второе разведение. Таким же образом готовят последующие разведения. Степень разведения зависит от плотности исследуемой популяции микроорганизмов.
Высевать суспензию поверхностным способом. Перед посевом поверхностным способом разливают агаризованную питательную среду в ряд стерильных чашек Петри по 15-20 мл в каждую. Чашки оставляют на горизонтальной поверхности, пока среда не застынет [43].
В чашку Петри с подсушенной средой вносят точно измеренный объем (0,1 мл) соответствующего разведения и распределяют его стеклянным шпателем по поверхности среды. После посева чашки Петри помещают в термостат крышками вниз.
Сроки учета зависят от состава питательной
среды. Количество колонии, выросших на плотной среде подсчитывают и вычисляют
по формуле 1:
M=а*10n/V, (1)
где М - количество клеток в 1 мл; а - среднее
число колоний, выросших после посева из данного разведения; V - объем
суспензии, взятый для посева, мл; 10n - коэффициент разведения.
3. Результаты
исследования и их обсуждение
.1 Выделение и изучение
аборигенных углеводородокисляющих микроорганизмов
Участие микроорганизмов в деградации и трансформации различных ксенобиотиков общепризнано. Углеводороды, в зависимости от степени сложности их молекул, разлагаются микроорганизмами различным образом. Установлено, что лучше всего бактериями усваиваются н-парафины, слабее - циклические и, в меньшей степени, полициклические ароматические углеводороды. Ассимиляция микроорганизмами ароматических углеводородов характерна лишь для отдельных штаммов некоторых видов микроорганизмов и является штаммовым свойством, возникающим в результате длительной адаптации, в связи с чем, при разработке биотехнологий для очистки различных экосистем техногенного происхождения первоначальной задачей является выделение и отбор высокоактивных культур микроорганизмов - деструкторов токсичных органических соединений.
В наших исследованиях для выделения и отбора активных культур микроорганизмов-деструкторов нефти использовались 2 метода:
метод выделения из накопительных культур с нефтью;
поиск активных штаммов - деструкторов органических соединений среди культур, хранящихся в музее кафедры биотехнологии КазНУ им. аль-Фараби.
Характеристика изучаемых 6 проб нефтешлама
(БВН-1, БВН-3, БШС-2, БШН-4, ЗГ-4, БШН(ц)-4) представлена в таблице 1. Для
получения накопительных культур нефтеокисляющих микроорганизмов из
вышеперечисленных проб полигона-накопителя отходов нефтедобычи, в качестве
элективного фактора и единственного источника углерода использовалась нефть с
концентрацией 80% по объему минеральной жидкой среды Е8. Следует отметить, что
элективные условия далеко не всегда оптимальны для роста выделяемых
микроорганизмов, однако они лучше переносятся ими, чем сопутствующими формами.
Таблица 1.
Названия и описание проб образцов, взятых для анализа
|
№ |
Название проб |
Сокращенное название |
Описание |
|
1 |
2 |
3 |
4 |
|
1 |
Буровые сточные воды с нефтью (карта 1) |
БВН-1 |
несмешиваемая двухфазная водно-маслянистая жидкость, темно-коричневого цвета |
|
2 |
Буровые сточные воды (карта 3) |
БВН-3 |
Гомогенная жидкость темно-коричневого цвета |
|
3 |
Буровой шлам «старый» (карта 2) |
БШС-2 |
Твердая фракция грунта, со слабым запахом нефти, отстоявший в течение года на карте № 2 |
|
4 |
Буровой шлам «новый» (карта 4) |
БШН-4 |
Твердая фракция грунта, с резким запахом нефти, собираемый в течение 1-3 месяцев на карте №4 |
На рисунке 4 представлены фотографии получения накопительных нефтеокисляющих культур из проб БВН-1 и БШН-4 полигона накопителя отходов нефтедобычи.
Как видно из рисунка 4, в накопительных суточных
культурах нет видимых изменений ни в цвете среды, ни в консистенции нефти,
тогда как, на 6-7 сутки во всех пробах наблюдаются визуальные признаки развития
накопительных культур, такие как изменение консистенции, цвета среды
культивирования, образование эмульсии капель нефти, накопление хлопьевидного
осадка. Однако, накопительные культуры БВН-1, ЗГ-4 и БШС-2 характеризуются
более обильным образованием осадка, что косвенно свидетельствует о более
интенсивном процессе биодеградации углеводородов нефти микроорганизмами в
условиях отсутствия других источника углерода. Таким образом, из твердых и
жидких фракций нефтешлама полигона-накопителя месторождения «Жанажол» были
получены 5 накопительных нефтеокисляющих культур, обозначенных нами как БВН-1,
БВН-3, БШС-2, БШН-4, ЗГ-4, БШН(ц)-4.

Суточные культуры

Шестисуточные культуры
Рисунок 4. Получение накопительных культур
нефтеокисляющих микроорганизмов из проб БВН-1 и БШН-4
Далее, накопительная нефтеокисляющая культура микроорганизмов пересевалась на плотную среду МПА для получения изолированных колоний углеводородокисляющих микроорганизмов. Затем, доминирующие колонии микроорганизмов отсевались для получения бактериологически чистой культуры угловодородокисляющих микроорганизмов.
В таблице 2 представлены результаты выделения
бактериологически чистых культур нефтеокисляющих микроорганизмов из
накопительных культур, полученных из различных проб полигона-накопителя ТОО
ХимпромсервисАктобе» месторождения «Жанажол».
Таблица 2.
Культуры микроорганизмов, выделенные из различных проб полигона-накопителя ТОО «ХимпромсервисАктобе» месторождения «Жанажол»
|
№ |
Образцы проб |
Накопительная культура |
Всего культур |
Число культур с одной пробы |
Сокращенное название культур микроорганизмов |
|
1 |
Буровые сточные воды с нефтью (карта 1) |
БВН-1 |
1. |
1 |
БВН-1 |
|
2 |
Буровой шлам старый (карта 2) |
БШС-2 |
2. |
1 |
БШС-1 |
|
|
|
|
3. |
2 |
БШС-2 |
|
3 |
Буровой шлам новый (карта 4) |
БШН-4 |
4. |
1 |
БШН-1 |
|
|
|
|
5. |
2 |
БШН-2 |
|
|
|
|
6. |
3 |
БШН-3 |
|
|
|
|
7. |
4 |
БШН-4 |
|
4 |
Буровой шлам с цементом новый (карта 4) |
БШН(ц)-4 |
8. |
1 |
БШН(ц) |
|
5 |
Замазученный грунт (карта 4) |
ЗГ-4 |
9. |
1 |
ЗГ-1 |
|
|
|
|
10. |
2 |
ЗГ-2 |