Материал: ик спектроскоп
Государственное бюджетное образовательное учреждение высшего профессионального образования
«САНКТ-ПЕТЕРБУРГСКАЯ ГОСУДАРСТВЕННАЯ ХИМИКО-ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВа ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ Российской Федерации
КАФЕДРА АНАЛИТИЧЕСКОЙ ХИМИИ
Ю. А. Скорик, А. С. Березин, А. А. Екимов
Методические рекомендации по самостоятельному изучению темы
«ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ»
САНКТ-ПЕТЕРБУРГ «Изд-во СПХФА»
2012
УДК 535.33 М54
Рецензенты:
доц., д.х.н. Булатов А. В. (кафедра аналитической химии СПбГУ), проф., д.х.н. Яковлев И. П. (кафедра органической химии СПХФА)
М54 Методические рекомендации по самостоятельному изучению темы «Инфракрасная спектроскопия»/ сост. : Ю. А. Скорик, А. С. Березин, А. А. Екимов. — СПб. : Изд-во СПХФА, 2012. — 40 с.
ISBN 978-5-8085-0318-2
Методические рекомендации посвящены применению ИК спектроскопии для идентификации органических соединений и предназначены для внеаудиторной самостоятельной работы студентов бакалавриата факультета промышленной технологии лекарств по направлениям химическая технология и биотехнология, а также для студентов фармацевтического факультета СПХФА.
В методических рекомендациях рассмотрены теоретические основы методаИКспектрскопии,приводятсяпримерырешениятиповыхзадач,которые носят ситуационный характер и имеют профессиональную направленность. Используя логику рассуждений обучающих задач, студент самостоятельно учится правильному логическому подходу, необходимому для выполнения самостоятельной работы. Через решение спектральных задач студент получает начальный запас знаний и практических навыков использования ИК спектроскопии в анализе органических соединений.
Рекомендованы методической комиссией факультета промышленной технологии лекарств
ISBN 978-5-8085-0318-2 |
© Санкт-Петербург государственная |
|
химико-фармацевтическая академия, 2012 |
ВВЕДЕНИЕ
В настоящее время инфракрасная (ИК) спектроскопия является одним из основных методов исследования веществ различной химической природы, в том числе и лекарственных субстанций.
Впервые метод стал фармакопейным с 1968 г (ГФ X), где он был рекомендован для контроля качества трех лекарственных веществ: фторотана, оксациллина и метициллина, а в разделе «Общие методы физикохимического, химического и биологического исследования» фармакопеи помещен материал, касающийся вопросов теоретического и практического использования ИК спектроскопии в анализе. Со времени выхода десятого издания фармакопеи число препаратов, при исследовании которых рекомендуется данный метод, значительно выросло, что можно проследить на примере дополнений к фармакопее, издаваемых ежегодно, и отдельно выпускаемых фармакопейных статьях. Так, Международная фармакопея (2008) рекомендует этот метод в анализе половины описанных в ней лекарственных веществ.
ИК спектроскопия занимает важное место в исследовании молекулярной структуры химических соединений, так как любая молекула имеет свой, только ей присущий ИК спектр, состоящий из набора полос поглощения разной частоты и интенсивности. Этот метод широко используется для установления структуры новых биологически активных веществ, получаемых путем химического синтеза или выделяемых из природных объектов (животное или растительное сырье, продукты жизнедеятельности микроорганизмов); при испытании на подлинность и определении доброкачественности лекарственных средств; в контроле технологических процессов в промышленном производстве лекарственных субстанций; для изучения кинетики химических реакций; для выявления природы межмолекулярных взаимодействий. В ряде случаев метод может использоваться для количественного анализа. Достоинством ИК спектроскопии является возможность исследования практически любого неорганического или органического вещества в любом агрегатном состоянии — газе, жидкости, растворах, кристаллах или аморфной фазе.
3
1. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ИНФРАКРАСНОЙ СПЕКТРОСКОПИИ
Молекула может поглощать излучение в результате трех основных процессов; в любом случае она при этом переходит в состояние с более высокой внутренней энергией, причем приращение энергии равно энергии фотона поглощенного излучения (hν). Три типа внутренней энергии квантуются, т. е. энергия может принимать только определенные значения, образуя систему дискретных уровней. Во-первых, молекула вращается вокруг своих различныхосей;находясьнаопределенномуровневращательнойэнергии,молекула может за счет поглощения излучения перейти на более высокий уровень вращательной энергии (вращательные переходы). Во-вторых, атомы или группы атомов в молекуле колеблются друг относительно друга, и энергия этих колебаний также квантуется. Молекула может поглотить дискретное количество энергии и перейти на уровень с более высокой колебательной энергией (колебательные переходы).В-третьих, электроны молекулы могут переходить на болеевысокиеуровниэлектроннойэнергии(электронныепереходы).
ИК спектроскопия — метод исследования, основанный на поглощении веществом инфракрасного излучения, в результате чего происходит усиление колебательных (и отчасти вращательных) движений молекул. Атомы в молекулах никогда не находятся в состоянии покоя, а колеблются относительно каких-то средних положений, поэтому их взаимное расположение периодически меняется. ИК излучение усиливает эти колебания, при этом часть энергии поглощается молекулами, которые переходят из одного колебательного состояния в другое, с более высокой энергией. Именно поэтому ИК спектры называют колебательными.
К инфракрасному относят электромагнитное излучение с длиной волны от 0.8 до 1000 мкм. Энергия, необходимая для возбуждения колебаний атомов в молекуле, соответствует энергии фотона с длиной волны 2.5—25 мкм или волновым числом 400—4000 см-1, т. е. электромагнитному излучению средней инфракрасной области. Области, примыкающие к ней, называются ближней инфракрасной (12500—4000 см-1) и дальней инфракрасной (400—10 см-1). Слова ближний и дальний характеризуют близость к области видимого света.
Процессы, приводящие к появлению аналитического сигнала
ИК спектроскопия дает информацию о частотах колебания связей, так как молекула поглощает инфракрасное излучение с такими частотами, с какими колеблются отдельные связи. Трехатомную молекулу (или трехатомную группировку в составе молекулы) можно представить в виде трех шариков, связанных между собой пружиной (упругой связью),
4
не имеющей массы. В такой системе могут происходить два вида колебаний: валентные и деформационные.
Валентные колебания (ν) — это ритмичные колебания вдоль оси связи, при которых расстояние между колеблющимися атомами увеличивается или уменьшается, но сами атомы остаются на оси валентной связи.
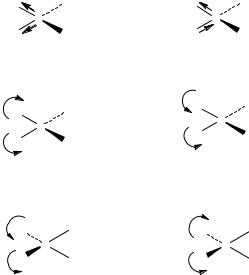
По форме валентные колебания бывают (рис. 1):
•симметричными(vs),еслиобесвязиодновременноудлиняютсяилиукорачиваются, а пары атомов одновременно приближаются или отдаляются;
•асимметричными (vas), если одна из связей укорачивается, а другая — удлиняется, в этом случае приближение и отдаление разных пар атомов происходит не одновременно.
Частота асимметричного колебания всегда выше, чем симметричного.
Деформационные колебания (δ) связаны с изменением валентного угла,
образованного связями у общего атома. Деформационные колебания подраз-
деляются на ножничные, веерные, крутильные, маятниковые (рис. 1). Для возбуждения деформационных колебаний требуется меньшая энергия, чем в случаевалентныхколебанийи,следовательно,ониимеютменьшуючастоту.
|
Валентныеколебания |
H |
H |
C |
C |
H |
H |
симметричные aсимметричные
Деформационные колебания в плоскости
H |
|
H |
|
C |
|
|
C |
|
|
H |
|
H |
|
|
|
|
ножничные маятниковые
Деформационныеколебания внеплоскости
H |
H |
C |
C |
H |
H |
крутильные |
веерные |
Рис. 1. Валентные и деформационные колебания метиленовой группы
5