Контрольная работа: Идеальные системы
В
общем случае произвольных температур сумма ![]() может
быть рассчитана только численно. На рис. приведен график cвр
(в единицах k) как функции безразмерной величины
может
быть рассчитана только численно. На рис. приведен график cвр
(в единицах k) как функции безразмерной величины 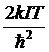 .
.
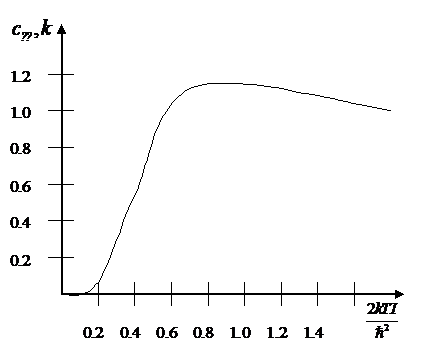
Рис.
2.2
Вращательная
теплоемкость имеет максимум, равный 1,1 при 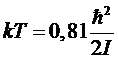 , после
чего асимптотически приближается к классическому значению 1.
, после
чего асимптотически приближается к классическому значению 1.
9. Двухатомный газ. Колебания атомов
Колебательная
часть термодинамических величин газа становится существенной при значительно
более высоких температурах, чем вращательная, потому, что интервалы
колебательной структуры велики по сравнению с интервалами вращательной
структуры. В таблице приведены характерные колебательные температуры 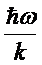 .
.
|
Молекула |
|
|
H2 |
6100 |
|
N2 |
3340 |
|
O2 |
2230 |
|
NO |
2690 |
|
HCl |
4140 |
Мы
будем считать, однако, температуру большой лишь настолько, чтобы были
возбуждены в основном не слишком высокие колебательные уровни. Тогда колебания
можно считать малыми и гармоническими, а уровни энергии определяются обычным
выражением для гармонического осциллятора 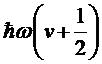 . В
случае ангармонических колебаний выражение для энергии будет значительно
сложнее.
. В
случае ангармонических колебаний выражение для энергии будет значительно
сложнее.
Вычислим
колебательную статистическую сумму
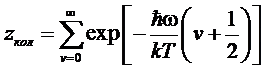 . (*)
. (*)
Хотя при больших числах v колебания будут ангармоническими, но вследствие очень быстрой сходимости ряда суммирование можно распространить до бесконечности.
Сумма
(*) представляет собой геометрическую прогрессию:
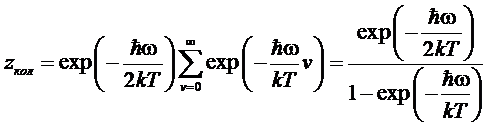 ,
,
откуда
свободная энергия
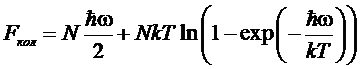 ,
,
энтропия
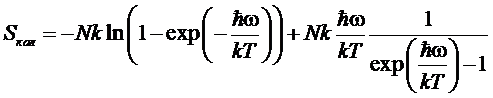 ,
,
энергия
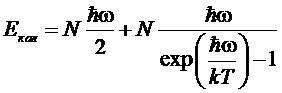 ,
,
и
теплоемкость 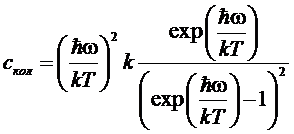 .
.
На
рисунке изображен график зависимости ![]() от
от 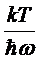 .
.
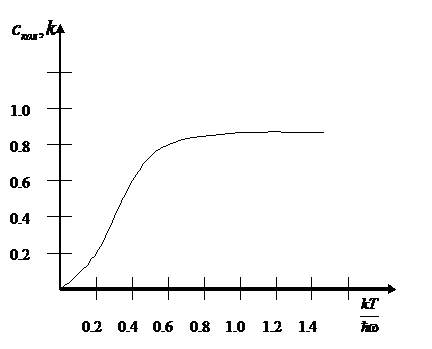
Рис.
2.3
При
низких температурах (![]() ) энтропия и теплоемкость стремятся экспоненциально к
нулю:
) энтропия и теплоемкость стремятся экспоненциально к
нулю:
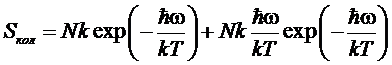 ,
,
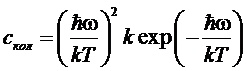 ,
,
а свободная энергия и энергия стремятся к постоянной величине.
При
высоких температурах (![]() ) имеем:
) имеем:
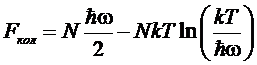 ,
,
чему
соответствует постоянная теплоемкость ![]() .
.
Таким
образом, полная теплоемкость двухатомного газа при температурах ![]() (практически уже при
(практически уже при ![]() ) равна
) равна
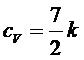 ,
, 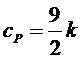 .
.
Многоатомный газ. Свободную энергию многоатомного газа, как и двухатомного газа, можно представить в виде суммы трех частей- поступательной, вращательной и колебательной.
Благодаря большой величине моментов инерции многоатомных молекул (и соответственно, малости их вращательных квантов) их вращение можно всегда можно рассматривать классически. Эффекты квантования вращения могли бы наблюдаться лишь у метана CH4, где они должны появляться при температурах около 50K.
Многоатомная
молекула обладает, в общем случае, тремя вращательными степенями свободы и
большим числом колебательных степеней свободы. Если молекула обладает
какими-либо осями симметрии, то повороты вокруг этих осей совмещают молекулу
саму с собой и сводятся к перестановке одинаковых атомов. Например, если все
атомы в молекуле расположены на одной прямой (линейная молекула), то она
обладает, как и двухатомная молекула, всего двумя вращательными степенями
свободы и одним моментом инерции.
.
Флуктуации. Распределение Гаусса
Статистическое и чисто термодинамическое описание тепловых процессов различаются тем, что из законов статистической физики с неизбежностью вытекает существование флуктуаций. В то же время вероятность сколько-нибудь заметных флуктуаций в системе, содержащей большое число частиц, чрезвычайно мала.
Открытие многочисленных примеров флуктуационных процессов явилось блестящим подтверждением законов статистической физики и послужило одним из важнейших моментов в окончательном утверждении молекулярной теории.
В работах Эйнштейна и Смолуховского было показано, что целый ряд давно известных физических процессов обусловлен явлениями флуктуаций, и была развита комплексная теория этих вопросов, оказавшихся в прекрасном согласии с экспериментами.
Рассмотрим флуктуации в замкнутой системе.
Пусть система находится в состоянии статистического равновесия и имеет энтропию S0. Предположим теперь, что состояние системы изменяется так, что она переходит в неравновесное состояние с энтропией S.
Будем считать, что изменение состояния системы можно характеризовать изменением некоторого внутреннего параметра x, значение которого зависит от состояния всей системы.
В равновесии x = x0. Пример x - плотность ρ газа, находящегося в замкнутом теплоизолированном сосуде. В состоянии равновесия плотность постоянна по всему объему сосуда x0=ρ0=const.
В результате флуктуации система может самопроизвольно перейти в неравновесное состояние с переменной плотностью x= ρ(r).
Энтропия системы будет некоторой функцией параметра x: S=S(x). При этом в состоянии равновесия S0=S(x0) .
Вероятность
застать систему в интервале значений x; x+dx
должна быть пропорциональна статистическому весу (числу микросостояний) и
величине интервала dx:
![]() .
.
Для
изолированной системы верна формула Больцмана
![]()
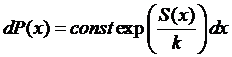
Константа
определяется из условия нормировки:
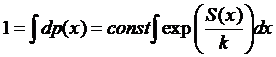
Или
для функции распределения:
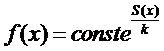 (*)
(*)
Прежде, чем приступить к интегрированию этой функции, надо ответить на вопрос о пределах ее применимости. Все распределения, приведенные выше, неявно подразумевают классичность поведения x. Поэтому надо найти условие, допускающее пренебрежение квантовыми эффектами.
Как
известно из квантовой механики, между квантовыми неопределенностями энергии и
какой-либо величины x имеет место соотношение
![]()
где dx/dt - классическая скорость изменения величины x.
Пусть
τ - время, характеризующее скорость изменения нашей
величины x, которая имеет неравновесное значение. Тогда 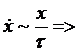
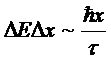
Ясно,
что говорить об определенном значении величины x можно лишь при
условии малости ее квантовой неопределенности ![]()
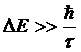
Таким
образом, квантовая неопределенность энергии должно быть велика по сравнению с ![]() . Энтропия системы будет при этом иметь
неопределенность
. Энтропия системы будет при этом иметь
неопределенность
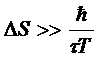
Для
того, чтобы формула (*) имела реальный смысл, необходимо, очевидно, чтобы
кавнтовая неточность энтропии была мала по сравнению с k:
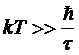 ;
; 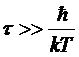
Это и есть искомое условие. При слишком низких температурах или при слишком быстром изменении x (слишком малом τ) флуктуации нельзя рассматривать термодинамически, т.к. на первый план выступают чисто квантовые флуктуации.
Выберем
x так, что энтропия имеет максимум при x = x0 =
0. Поэтому
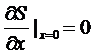 ,
, 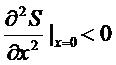
Величина
x при флуктуациях очень мала. Разлагая S(x) в
ряд по степеням x и ограничиваясь членом второго порядка, получим
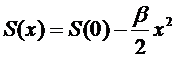
где
β>0.
Тогда получим распределение вероятностей
в виде:
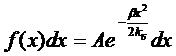
Нормирование
константы A определяется условием
![]()
Хотя выражение для f(x) относится к малым x, но ввиду быстрого убывания подынтегральной функции с увеличением |x| область интегрирования можно распространить на все значения от -∞ до +∞. Произведя интегрирование, получим
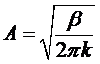 (интеграл
Пуассона).
(интеграл
Пуассона).
Таким
образом, имеем для величины x распределение:
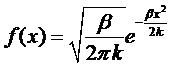 .
.
Эта
формула называется распределение Гаусса. Если обозначить
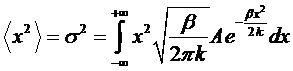 ,
,
то,
беря интеграл, распределение можно записать в виде:
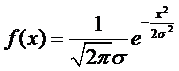 .
.
Функция f(x) имеет тем более острый максимум, чем меньше <x2>.
Отметим, что по известному <x2> можно найти аналогичную величину для любой функции j(x). Ввиду малости x имеем:
<(Dj)2> = 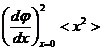
(подразумевается, что функция j(x) мало меняется при значениях x ~ <x2> и что производная dj/dx отлична от нуля при x = 0).
Если
![]() , то распределение Гаусса запишется в виде:
, то распределение Гаусса запишется в виде:
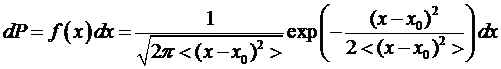 .
.
11.Флуктуации термодинамических величин
Рассчитаем теперь флуктуации конкретных термодинамических величин.
Пусть
ƒ
- любая физическая величина, испытывающая
флуктуации. Флуктуацией величины ƒ называется отклонение ![]() мгновенного
значения этой величины от ее среднего значения. Очевидно, что <Δƒ>
= 0. Поэтому обычно пользуются средним
квадратом флуктуации, т.е. величиной <Δƒ2>. Квадратный корень из этой величины
мгновенного
значения этой величины от ее среднего значения. Очевидно, что <Δƒ>
= 0. Поэтому обычно пользуются средним
квадратом флуктуации, т.е. величиной <Δƒ2>. Квадратный корень из этой величины ![]() называется - среднеквадратичной флуктуацией.
называется - среднеквадратичной флуктуацией.
Усредняя
выражение ![]() , получим
, получим
![]()
Следовательно,
![]() (1)
(1)
Усредним
теперь произведение двух флуктуирующих величин:
![]()
Учитывая,
что <Δƒ>=
<Δg >= 0, получим
![]() (2)
(2)
Формула (1) содержится здесь как частный случай, который получается при g =f.
Величины f и g называются статистически независимыми, если <ΔfΔg> = 0.
Для таких величин
<fg>=<f><g>. (3)
Рассмотрим теперь любую физическую систему, состоящую
из N независимых одинаковых частей. Примером такой системы может служить
идеальный газ, а составных частей - отдельные молекулы. Пусть ft - произвольная аддитивная величина,
характеризующая i-ю подсистему,
например, в приведенном примере - кинетическая энергия i-й молекулы. Тогда в силу предполагаемой аддитивности
соответствующая величина для всей системы будет F = Σƒi,. Выразим средний квадрат флуктуации
величины F через аналогичный квадрат для
величины ƒi
.Очевидно, <F> = Σ<ƒ>i = N<f>,
где индекс i опущен, так как предполагается, что
все составные части системы тождественны. Далее,
![]()
А
так как эти части независимы, то, <ƒi ƒj
>= <ƒi >< ƒj >=(<ƒ>)2. Следовательно,
![]()
Подставляя
эти значения в формулу (1), получим
![]() (4)
(4)
Отсюда
на основании (1)
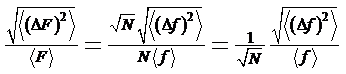 (5)
(5)
Таким
образом, с увеличением N относительная флуктуация величины F
убывает обратно пропорционально ![]() . При
больших величинах N относительные флуктуации ничтожны. Этот вывод
качественно верен и для неаддитивных величин. С ним связана достоверность
термодинамических результатов для больших макроскопических систем.
. При
больших величинах N относительные флуктуации ничтожны. Этот вывод
качественно верен и для неаддитивных величин. С ним связана достоверность
термодинамических результатов для больших макроскопических систем.
В
соответствии со сказанным видим, что в объемах с большим средним числом частиц N
относительные флуктуации малы и труднодоступны наблюдению. Наоборот, при малых N
относительные флуктуации велики. Более общий метод вычисления флуктуации
плотности, применимый также к жидкостям и твердым телам, основан на теореме о
равномерном распределении кинетической энергии по степеням свободы. Рассмотрим
малую часть жидкости или газа, окруженную такой же жидкой или газообразной
средой, температура Т которой поддерживается постоянной (термостатом). С целью
упрощения и наглядности вычислений предположим, что малая часть жидкости или
газа заключена в цилиндр с поршнем. Стенки цилиндра идеально проводят тепло, а
поршень может ходить в нем без трения. Тогда наличие стенок цилиндра и поршня
не будет препятствовать обмену энергией и выравниванию давлений между веществом
в цилиндре и термостатом. Тепловое движение молекул вещества вызовет
броуновское движение поршня. К этому движению поршня мы и применим теорему о
равномерном распределении кинетической энергии по степеням свободы. Поршень
можно рассматривать как гармонический осциллятор, совершающий беспорядочные
тепловые колебания. Среднее значение его потенциальной энергии при смещении на
х из положения равновесия х = 0 равно (1/2) кх2 = (1/2)кТ, где к - жесткость,
соответствующая такому смещению. Если S - площадь поршня, a DV -
изменение объема системы, то DV = Sx. Таким образом, <(ΔV)2 > = <S2x2>=
S2kT/K. Сила, возвращающая поршень в положение равновесия,
будет ![]() , где Р - давление газа или жидкости. Поэтому к = - SdP/dх =S2dP/dV. В
результате получим
, где Р - давление газа или жидкости. Поэтому к = - SdP/dх =S2dP/dV. В
результате получим
 , К
, К