Материал: gina 2018 что нового
GINA 2018: что нового?
21.06.2018
Несмотря на все усилия, предпринимаемые для достижения контроля над бронхиальной астмой (БА), ее распространенность во всем мире, особенно среди детей, растет. По данным Глобальной стратегии по управлению и профилактике БА
(Global Strategy for Asthma Management and Prevention, GINA), в настоящее время
вмире от астмы страдают 300 млн человек. Такая ситуация способствует неуклонному повышению расходов национальных систем здравоохранения, а также росту издержек как самих пациентов, так и их семей. Поэтому ежегодные обновленные отчеты научного комитета GINA не только содержат рекомендации по обучению специалистов, пациентов и их семей методам эффективного контроля
над астмой, но и призваны побудить лидеров национальных систем здравоохранения оптимизировать менеджмент астмы и повысить доступность современной терапии.
В 2018 году отчет традиционно был опубликован после рутинного двухгодичного кумулятивного обзора литературы научным комитетом GINA. Он содержит данные новейших публикаций результатов исследований, адаптированных для применения
вклинической практике.
Оценка БА
Изменения затрагивают концепцию «независимых факторов риска», способствующих обострению заболевания как у взрослых, так и у детей. При этом главным фактором считается неконтролируемая астма. В качестве дополнительного независимого фактора риска добавлена высокая степень бронхиальной обструкции. Основными факторами также считаются наличие ≥1 серьезного обострения за последние 12 мес и эпизоды интубации у пациентов с астмой. Кроме того, риск обострения повышает наличие любого из нижеследующих факторов даже у пациентов с минимально выраженными симптомами БА:
Частое использование короткодействующих бета-агонистов (КБА) (предиктор повышения смертности при использовании >200 доз в месяц).
Неадекватная терапия ингаляционными кортикостероидами (ИКС) (отсутствие
всхеме лечения ИКС, низкая приверженность лечению).
Нарушение техники и режима ингаляций.
Снижение объема форсированного выдоха за 1 секунду (ОФВ1) (≤60%), высокая степень бронхиальной обструкции.
Эозинофилия в мокроте или периферической крови.
Увеличение фракции выдыхаемого оксида азота (FeNO) у взрослых
саллергической БА, принимающих ИКС.
Коморбидность (ожирение, хронический риносинусит, диагностированная пищевая аллергия).
Беременность.
Помимо вышеуказанного вероятность развития обострений повышается при неадекватном употреблении оральных кортикостероидов (ОКС), высоких доз ИКС, а также ингибиторов цитохрома Р450.
В качестве дополнительных факторов риска, способствующих постоянному ограничению воздушного потока, указываются профессиональное облучение, курение, гиперсекреция слизи. Также добавлены недоношенность, низкий вес при рождении, большая прибавка массы тела в младенчестве (den Dekker H.T. et al., 2016).
Из перечня факторов риска были удалены «основные психологические или социальноэкономические проблемы» пациентов, по мнению P.M. Sturdy и соавт. (2012), способствующие обострению БА.
Ступенчатая терапия астмы (изменения в 2018 г.)
Добавлены пояснения, касающиеся раннего применения ИКС, комбинированной терапии ИКС с пролонгированными бета-агонистами (ПБА), а также лечения тяжелой астмы, подтвержденные данными новых исследований.
Шаг 1
Причина, по которой низкие дозы ИКС следует рассматривать для применения у пациентов с легкой астмой (вместо монотерапии КБА), заключается в снижении риска серьезных обострений (Reddel H.K. et al., 2017).
Для многих пациентов первичного звена контроль симптомов БА является лучшим способом снижения обострений. Когда в менеджмент астмы были введены ИКС, частота обострений и смертность снизились, при этом наблюдалось улучшение контроля симптомов и функции легких.
Шаги 3-4
Обширные исследования, посвященные безопасности применения ПБА, показали, что добавление ПБА к ИКС в ингаляторе снижает риск обострений, улучшает симптомы
и функцию легких по сравнению с монотерапией ИКС в аналогичной дозе (Stempel D.A. et al., 2016; Peters S.P. et al., 2016).
Шаг 5 и разделы 3-14
Для пациентов в возрасте ≥12 лет с тяжелой эозинофильной астмой дополнительным средством терапии является подкожное введение бенрализумаба (моноклональное антитело против рецептора интерлейкина-5 – ИЛ-5).
Предменструальная/менструальная астма и астма при беременности
Добавлен новый раздел. Ухудшение симптомов БА у женщин наблюдается в следующих ситуациях:
У 20% женщин – перед менструацией и во время менструации.
У женщин в позднем репродуктивном возрасте, с высоким индексом массы тела (ИМТ) и персистирующей тяжелой астмой; для этой когорты характерны дисменорея, укорочение менструального цикла, увеличение длительности кровотечения, обострение респираторных симптомов после приема ацетилсалициловой кислоты (Sanchez-Ramos J.L. et al., 2017).
Вкачестве дополнительного лечения рекомендованы оральные контрацептивы и/или антагонисты лейкотриеновых рецепторов (АЛТР).
Получены доказательства против отмены ИКС во время беременности:
ИКС уменьшают риск обострений при беременности – уровень доказательности А (Schatz M. et al., 2005; Murphy V.E. et al., 2011).
Отмена ИКС повышает риск обострений при беременности – уровень доказательности А (Murphy V.E. et al., 2006).
FeNO
Добавлено: в силу того что тест становится более доступным во многих странах, разделы, посвященные FeNO, были пересмотрены с учетом новых данных и доказательств, имеющих силу.
Рекомендации, касающиеся стартовой терапии астмы
Низкие дозы ИКС показаны практически всем пациентам с целью снижения рисков обострений и смертности.
Монотерапия КБА возможна только при наличии приступов ≤2 раза в месяц, отсутствии ночных симптомов и факторов риска обострения.
У некурящих пациентов уровень FeNO ≥50 ppb (частиц на 1 млрд) ассоциируется с хорошим краткосрочным ответом на ИКС по влиянию на симптомы БА и функцию легких.
Исследования безопасности применения и снижения риска обострений при длительной терапии ИКС и низком исходном уровне FeNO не проводились.
У пациентов с диагностированной или предполагаемой астмой исходный уровень FeNO может служить аргументом в пользу начала терапии ИКС, однако не может являться причиной для принятия решения об отказе от лечения данными препаратами.
FeNO – ориентированная терапия астмы
Раздел обновлен с учетом новых данных двух отдельных метаанализов (Petsky H.L. et al., 2016; Petsky H.L. et al., 2016) исследований алгоритма достижения контроля астмы, достаточно близким к текущим клиническим рекомендациям и, соответственно, релевантным для сравнения:
Дети/подростки – лечение с учетом результатов определения FeNO ассоциируется со значительно меньшим числом и тяжестью обострений, чем терапия, основанная на текущих рекомендациях.
Взрослые – нет существенной разницы в частоте и тяжести обострений при лечении, учитывающем результаты теста FeNO, по сравнению с лечением, базирующемся на текущих рекомендациях.
В настоящее время FeNO-ориентированная терапия астмы не рекомендована для повсеместного применения.
Для выявления наиболее восприимчивых групп пациентов и оптимальной частоты мониторинга FeNO необходимы дальнейшие исследования.
FeNO у детей в возрасте ≥5 лет с рецидивирующим кашлем и свистящими хрипами
Повышенный уровень FeNO в течение более чем 4 недель после любой острой респираторной инфекции является предиктором манифестирования астмы в школьном возрасте (Singer F., 2013).
Повышенный уровень FeNO в возрасте 4 лет повышает риск развития свистящих хрипов, манифестирования астмы и необходимости применения ИКС в школьном возрасте независимо от клинической истории и наличия специфического иммуноглобулина IgE (Caudri D., 2009).
Последующее наблюдение после обострения астмы
Всем пациентам после обострения необходим мониторинг состояния до нормализации функции легких
Во время выздоровления повышен риск повторного обострения.
Возможность пересмотра терапевтической тактики
Обострения часто представляют собой неудачи в лечении хронической астмы,
с одной стороны, и предоставляют возможности для пересмотра ее менеджмента для каждого конкретного пациента – с другой.
При последующих посещениях необходимо проверить:
понимание пациентом причины обострения его заболевания;
наличие модифицируемых факторов риска (например, курение);
соблюдение пациентом режима терапии и понимание ее цели;
прием КБА только по мере необходимости, а не регулярно;
правильность использования ингалятора и выполнения техники ингаляций;
наличие у пациента письменного плана по достижению контроля над астмой.
Коморбидность БА и хронического обструктивного заболевания легких (ХОЗЛ) – БА-ХОЗЛ-оверлап
Определение «БА-ХОЗЛ-оверлап» не подразумевает наличия отдельной нозологии
Включает пациентов с несколькими различными формами (фенотипами) заболеваний дыхательных путей, вызванных воздействием целого ряда основных факторов.
Постоянное ограничение воздушного потока выявляют:
у некоторых детей с астмой (McGeachie M.J. et al., 2016);
у многих взрослых с БА (Lange P. et al., 2015);
у пациентов, достигших совершеннолетия, с низкой функцией легких
изакономерным ее снижением с течением времени (Lange P. et al., 2015);
у пациентов, достигших совершеннолетия, с нормальной функцией легких
ибыстрым ее снижением с течением времени (Lange P. et al., 2015).
Проблемы терапии пациентов с коморбидностью БА и ХОЗЛ
Малая доказательная база; пациенты с БА-ХОЗЛ-оверлап исключаются из большинства рандомизированных клинических исследований (РКИ).
Необходимость включения ИКС (в качестве временной рекомендации) в схему лечения пациентов с ХОЗЛ и хронической астмой; безопасность данной рекомендации подтверждена хорошо разработанным дизайном исследования «случай – контроль»
(Gershon A.S. et al., 2014).
Дети в возрасте ≤5 лет – ключевые изменения
Шаг 2 (стартовая терапия по достижению контроля) для детей со свистящим дыханием, вызванным частыми вирусными инфекциями и периодическими симптомами астмы:
вначале следует назначить ежедневный прием низких доз ИКС;
можно рассмотреть эпизодический прием ИКС или по необходимости;
уменьшение обострений больше выражено на фоне постоянного приема ИКС или эпизодически высоких доз (Kaiser S.V. et al., 2015);
АЛТР являются еще одним вариантом достижения контроля симптомов.
Шаг 3 (дополнительная терапия по достижению контроля):
вначале необходимо уточнить диагноз, проконтролировать правильность выполнения техники ингаляций, воздействие аллергенов, переносимость
иприверженность терапии;
предпочтительным вариантом является прием ИКС в средних дозах;
еще одной терапевтической опцией для достижения контроля являются низкие дозы ИКС + АЛТР;
предикторами более выраженного кратковременного ответа на умеренные дозы ИКС по сравнению с АЛТР служат уровень эозинофилов периферической крови
иатопия (Fitzpatrick A.M. et al., 2016);
в некоторых странах на выбор варианта терапии может влиять ее стоимость. Схема ступенчатой терапии БА для детей младше 5 лет изображена на рисунке 1.
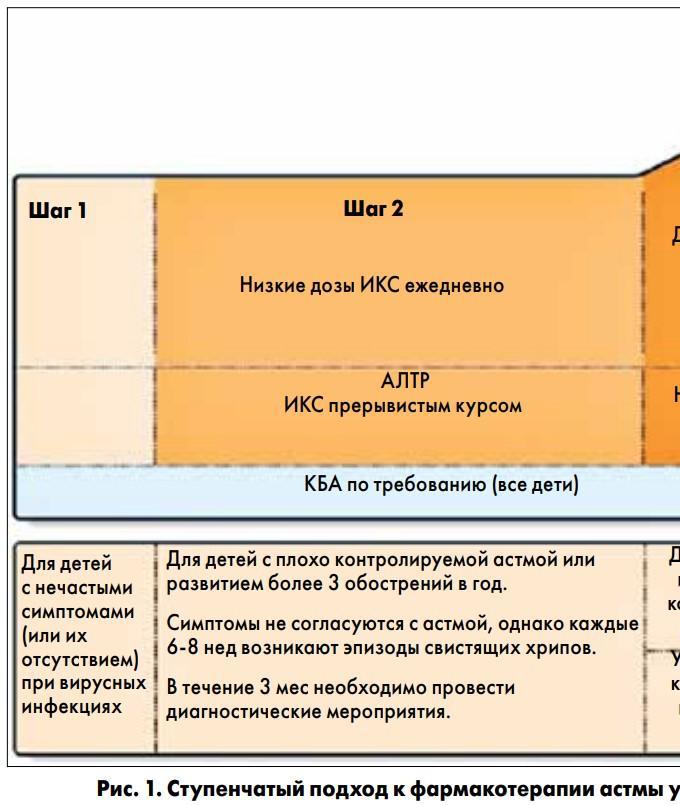
Дозы ИКС, которые используются в педиатрической практике для лечения БА у детей младше 5 лет, отображены в таблице 1.