Материал: Гетерогенный катализ. Основные теории. Применение в нефтехимической промышленности
После конденсации серы образующийся S02 в каталитических реакторах при 250-280°С реагирует с непрореагировавшим H2S по реакции 2. Эта реакция характеризуется небольшим тепловым эффектом, что сильно облегчает поддержание температуры в каталитическом слое. Выше 600°С преимущественно образуется элементная сера S2, при низких температуpax - S8. Реакции 1, 3 и 4 - практически необратимые, реакция 2 - обратимая. Константа ее равновесия равна единице при 500-600°С (для разных форм серы) и растет со снижением температуры. Понижение температуры, повышение давления и отвод продуктов реакции (воды) благоприятно сказываются на конверсии.
В качестве катализаторов второй стадии процесса, т.е. реакции H9S + S02, широко применяли природные бокситы (руды, содержащие смесь гидроксидов алюминия) вследствие их достаточно высокой активности, доступности и низкой стоимости. Их недостатки - быстрая дезактивация и непостоянство состава. Сейчас в качестве катализатора используются оксид алюминия, а именно ɣ-Аl2O3, в виде гранул сферической формы, реже - в форме экструдатов с удельной поверхностью 250-300 м2/г. Иногда применяют TiO2. На тех же катализаторах удаляют и примесные газы CS2 и COS по реакции гидролиза. Дезактивация А12O3 происходит за счет уменьшения удельной поверхности, зауглероживания и сульфатации. Катализатор регенерируют восстановительной обработкой в H2S, взаимодействующем с сульфатом.
В хвостовых газах процесса Клауса содержится 0.5-1.8% H2S + SO2 и 0.04-0.16% COS + CS2. Ранее эти газы сжигали, чем загрязняли атмосферу. Позднее был разработан процесс взаимодействия H2S с SO2 на Аl2O3 при 125-150°С. Преимущество низких температур заключается в том, что они смещают реакцию ниже точки росы серы и позволяют сдвинуть равновесие в сторону серы. Таким образом достигается полная конверсия H2S и SO2. Иногда для очистки хвостовых газов производят поглощение H2S и SO2 в жидкой фазе с реакцией между ними в присутствии гомогенного катализатора (например, Na-coли сульфокислоты) и образованием твердой серы. Есть сведения и о проведении заключительной стадии процесса Клауса в среде жидкой серы.
Каталитическое окисление сероводорода молекулярным кислородом. Было бы удобнее при сероочистке сероводород окислять прямо в серу, а не в SO2. Первая промышленная установка по окислению H2S молекулярным кислородом в серу для переработки газа, содержащего 13-17% H2S, была пущена в 1982 г.
С ростом содержания H2S в исходной смеси по условиям равновесия вероятность образования серы по сравнению с SO2 возрастает. Кинетический и термодинамический анализ, проведенный Т.Г. Алхазовым, показывает, что для достижения высоких степеней превращения H2S в S2 (не менее 99%) должны быть выполнены следующие условия:
отношение величин активности катализатора в реакции Клауса и прямом окислении H2S молекулярным кислородом не должно превышать 0.01;
порядок реакции по кислороду должен быть меньше 1;
реакцию желательно проводить в избытке кислорода.
Если катализатор показывает нулевой порядок реакции по кислороду, то для достижения высокой степени конверсии H2S достаточно стехиометрического количества O2; в противном случае высокая конверсия H2S обеспечивается лишь в избытке кислорода.
При каталитическом окислении H2S до серы образующаяся сера оказывает автокаталитический эффект на реакцию.
По данным ЭПР, сера на поверхности находится в виде нескольких
свободных радикалов разного строения и состава. При окислении серы кислород
реагирует с этими радикалами.
![]()
Появляются три разных сигнала ЭПР, которые можно отнести к
цепочке, состоящей из атомов S; на конце этой цепочки находится один или два
атома кислорода. Восстановление кислорода в SxO2 осуществляется
фрагментами диссоциативно адсорбированного сероводорода.
![]()
При температуре выше 175°С образуется SO2.
![]()
Катализаторами окисления сероводорода в серу могут быть многие пористые твердые тела. Их активность во времени может уменьшаться, проходить через максимум или даже возрастать. Это связано с образованием и отложением в порах элементной серы, проявляющей часто более высокую каталитическую активность, чем исходное твердое тело. Катализаторы, активные в реакции Клауса, обычно малопригодны для селективного окисления сероводорода в серу. На бокситах и А12O3 наблюдаются сравнительно небольшие степени конверсии H2S в серу.
Алхазов изучил ряд катализаторов - оксидов переходных металлов - в окислении H2S до серы при типичных условиях: температуре 200-300°С, объемной скорости 6000 ч-1, содержании H2S 3% и O2 9%. Из простых оксидов более селективными были ТiO2 (рутил), Сг2О3, Fe2O3. Наилучшим среди них оказался Fe2O3, промотированный другими оксидными добавками. Он активен, селективен, обладает высокой механической прочностью. Положительное свойство железного катализатора заключается в его способности проводить окисление сероводорода в элементную серу в присутствии больших количеств углеводородов природного газа, которые при этом не подвергаются каталитическим превращениям.
Разложение сероводорода на элементную серу и
водород. При
температуре выше 1000°С может происходить термическая диссоциация молекулы H2S:
![]()
Применение катализаторов позволяет снизить температуру до 600-800°С. При более низких температурах протекает обратная реакция. Для того чтобы избежать обратной реакции образования H2S, необходима также разработка эффективного быстрого метода отделения водорода от паров серы при высоких температурах.
В ряде работ показано, что в качестве эффективных катализаторов для разложения H2S можно использовать сульфиды переходных металлов. На-пример, на минерале, состоящем из 43.5% Fe2O3, 29.4% Si02, 7.4% Аl2O3, 3.3% Mn304, было осуществлено каталитическое разложение H2S при 00-800°С.
При высоких температурах происходит также разложение
меркаптанов с образованием углеводородов и серы или углеводородов и H2S:
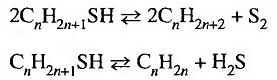
Скорость разложения меркаптанов может быть увеличена в присутствии катализаторов, в качестве которых применяли Аl2O3 и цеолиты. В продуктах реакции обнаруживают серу и сероводород.