Материал: Гетерогенный катализ. Основные теории. Применение в нефтехимической промышленности
3.1 Мультиплетная теория
Мультиплетная теория катализа создает предпосылки для сознательного подбора катализаторов реакций на основе теории строения молекул реагирующих веществ и кристаллических решеток катализаторов. Она позволяет также предсказывать направление процесса.
Мультиплетная теория катализа рассматривает геометрическое и энергетическое соответствие между реагирующими молекулами и атомами твердого тела. На основании этой теории Баландин предлагает метод подбора катализаторов для органических реакций. На поверхности твердого тела реагирующие молекулы образуют различные связи. Наиболее распространены дублетные реакции, при которых компоненты реакции связываются с двумя атомами катализатора. В органических соединениях только определенные группы атомов образуют связи с катализатором. Эти группы в мультиплетной теории названы индексными. Так, для реакции дегидрирования углеводородов индексной группой служит группа СН-СН, а катализаторы этой группы - окислы хрома, ванадия и молибдена. Активность этих соединений объясняется тем, что расстояния между атомами в их кристаллических решетках соответствуют расстояниям между атомами индексной группы. В окислах других металлов, например алюминия и кремния, расстояния между атомами будут уже иными, поэтому они являются менее активными катализаторами, чем первая группа окислов, и реакция на них протекает в менее выгодных условиях, чем в первом случае.
Следствия мультиплетной теории:
. Катализ происходит в монослое на поверхности катализатора.
. Молекулы субстрата ориентированы своими реагирующими группами к поверхности катализатора. Это подверждается очень близкими значениями энергии активации разных соединений в реакциях с одинаковыми индексами.
3.2 Теория активных ансамблей
Активный ансамбль состоит из двух или трех атомов катализатора. Если вещество сильно диспергировано, вероятность возникновения любых ансамблей очень мала. При высокой концентрации возникают ансамбли из большого числа атомов. Для выяснения механизма катализа по методу Кобозева измеряют зависимость удельной активности катализатора от его концентрации на носителе. Удельной активностью катализатора называют увеличение константы скорости реакции, отнесенное к единице веса катализатора.
Теория активных ансамблей была впервые предложена Н. И Кобозевым в 1939 г. Теория активных ансамблей Н.И. Кобозева является теорией катализатора. В ней, как и в мультиплетной теории, считается, что активный центр, ансамбль, состоит обычно из нескольких атомов катализатора. В теории ансамблей принимается, что только строго ограниченное число атомов катализатора может составить каталитически активный ансамбль. Теория рассчитывает это число из экспериментально найденной зависимости возрастания каталитической активности от степени заполнения поверхности носителя каталитическим материалом. В настоящее время теория не ставит своей целью объяснение причины катализа или причины, почему активно то, а не другое число атомов в ансамбле. Не ставит она своей задачей и объяснение избирательности катализа.
Принцип электронной теории катализа для процессов, протекающих при участии катализаторов металлов или их окислов, заключается в том, что свойства этих катализаторов могут влиять на ковалентные или электровалентные связи адсорбированных или ориентированных молекул, вызывая их деформацию, в результате чего будет происходить перестройка связей и образование новых продуктов.
Но данную теорию не стоит пока брать во внимание, так так она
появилась недавно и еще полностью не обосновала себя в той или иной степени.
IV. Применение катализа в нефтехимической промышленности
Важнейшим процессом нефтепереработки является каталитический крекинг. Крекинг углеводородов - наиболее многотоннажный промышленный каталитический процесс. С помощью крекинга из нефти получается жидкое моторное топливо: бензин, дизельное и реактивное топливо. В настоящее время в США - 50% нефти перерабатывается на установках каталитического крекинга.
В 1920-х годах в качестве катализатора крекинга применяли суспензию А1С13 в жидких углеводородах. В 1936 г. в США был запущен первый завод каталитического крекинга на основе предложения Э. Гудри использовать природные глины (монтмориллонит) как катализаторы крекинга. В 1943 г. фирма "Стандард Ойл" (ныне "Экссон-Мобил") ввела в действие производство ТСС (thermofor catalytic cracking) на основе шарикового алюмосиликатного катализатора. В 1949 г. появились первые установки с кипящим слоем микросферического катализатора. Эти установки - процесс FCC (fluid catalytic cracking) - стали главными после перехода промышленности крекинга в 1980-х годах на новое сырье - вакуумный газойль, вместо фракций дизельного топлива.
В 1960-х годах были внедрены цеолитсодержащие катализаторы крекинга. Суммарная мощность установок каталитического крекинга превышает сегодня 650 млн т/год, в том числе в США 265 млн т/год, а единичная мощность - в некоторых установках FCC - более 5 млн т/год. В России суммарная мощность установок каталитического крекинга равна 17 млн т/год. Общий объем производства катализаторов крекинга на всех катализаторных фабриках мира составляет - 450 тыс. т/год.
Технология. Схема промышленной установки приведена на рис.1
Шариковые катализаторы применяют в установках в восходящем потоке. Подогретое в
трубчатой печи нефтяное сырье подают в узел захвата, где оно тонко распыляется
и смешивается с регенерированным катализатором. Сырье (первичные продукты
перегонки нефти - газойль) вместе с катализатором перемещается снизу вверх при
линейных скоростях потока 10-12 м/с. Высота реактора, который представляет
стальную футерованную трубу, обеспечивающая необходимое время контакта сырья с
катализатором, обычно составляет 20-35 м. Поток сырья с катализатором движется
в режиме, близком к режиму идеального вытеснения. Температура процесса 470-570
СС, типичные времена контакта - от 2 до 10 с. При этом на катализаторе
образуется кокс [1-2% (маe.)]. В настоящее время шариковые цеолитсодержащие
катализаторы используют лишь на небольшом количестве заводов. В основном в
процессе FCC применяют микросферические цеолитсодержащие катализаторы.
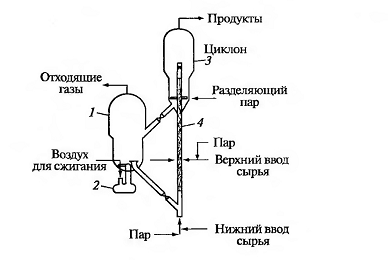
Рис.1. Схема промышленной установки каталитического
крекинга в кипящем слое катализатора:1 - регенератор катализатора, 2 -
подогреватель воздуха, 3 - циклон, 4 - лифт-реактор
Пары продуктов крекинга и непревращенное сырье после отделения катализатора в циклонах (сепараторы) разделяют в ректификационной колонне, из которой в систему возвращается шлам - смесь тяжелых фракций с катализатором. Отработанный катализатор с потоком воздуха поступает в отпарную секцию, где с поверхности катализатора отдувают десорбиро-ванные и увлеченные потоком углеводороды. Обработанный паром катализатор с потоком воздуха поступает в регенератор, где при 670-770°С производится выжигание кокса в кипящем слое. Время регенерации - от 5 до 15 мин. Регенерированный катализатор снова поступает на смешение с сырьем и таким образом цикл замыкается.
Сырьем для каталитического крекинга являются бензиновые фракции нефти, выкипающие при температуре выше 300°С. Для получения автомобильного бензина обычно применяют фракции 85-180°С. Выход и качество бензина зависят от состава сырья, используемого катализатора и режима процесса. Продукты каталитического крекинга разделяют перегонкой на следующие фракции:
. С4 и более легкие углеводороды (пропан-бутановая фракция); углеводороды этой фракции можно использовать как моторное топливо, как бытовой газ и в качестве сырья для алкилирования.
. Легкий крекинг-бензин (т. кип.18-93°С); используют как компонент бензина; с помощи этерификации метанолом октановое число такого бензина можно поднять с 95 до 102.
. Промежуточный крекинг-бензин (т. кип.93-165°С); в целях понижения содержания диолефинов в этой фракции ее необходимо подвергнуть мягкому гидрированию, так как диолефины могут образовать смолообраз-ныс вещества. При этом важно избежать гидрирования моноолефинов, так как иначе октановое число фракции снизится. В целом, октановое число у этой фракции ниже, чем у легкого бензина, и поэтому для улучшения октанового числа ее подвергают каталитическому риформингу (см. разд.10.3). Легкий и промежуточный крекинг-бензины могут выделяться также в виде одной фракции.
. Тяжелый крекинг-бензин (т. кип.150-235°С); из этой фракции можно экстрагировать ароматические углеводороды, а также алканы, которые можно использовать как топливо для реактивных двигателей. Углеводороды этой фракции подвергают гидроочистке для снижения содержания серы в товарном бензине. Снижение содержания серы является в настоящее время основной проблемой в получении бензинов. Другая проблема - как переработать высокоароматическое сырье.
. Фракция с т. кип. выше 235°С; в ней содержится большое количество ароматических и серосодержащих углеводородов. Ее можно подвергнуть гидрообессериванию и деароматизации, а затем использовать в качестве дизельного топлива.
Требования к катализатору. На основании изложенной технологии катализатор крекинга должен отвечать ряду требований:
) обладать высокой активностью и селективностью, т.е. должен обеспечивать значительную степень превращения сырья в высокооктановый бензин;
) должен иметь низкую скорость дезактивации и обладать способностью к полной регенерации без потери активности;
) сохранять стабильность при высокотемпературной регенерации. Кроме того, катализатор не должен образовывать слишком много кокса. Для крекинга в кипящем слое важна также механическая прочность на истирание;
) катализатор должен быть устойчив к отравлению ядами.
Кроме органических соединений азота и серы, содержащихся в нефтях и отравляющих катализатор, в нефтях некоторых месторождений содержатся также металлоорганические соединения Ni, Fe и V, которые отлагаются на поверхности катализатора, отравляют основную реакцию крекинга и способствуют образованию газа и кокса. При регенерации эти металлы катализируют реакцию сгорания кокса до С () 2, а не до СО, что приводит к нежелательным тепловым эффектам. При значительном содержании металлов в сырье приходится подвергать его специальной гидродеметалли-зации на катализаторах гидроочистки. В новых установках каталитического крекинга большое внимание уделяется как тщательной очистке сырья от серо - и азотосодержащих соединений и металлов, так и удалению SO2,NOx,CO из газов регенерации. Цеолитсодержащие катализаторы обладают рядом преимуществ по сравнению с аморфными алюмосиликатами:
) цеолиты отличаются более высокой активностью;
) они обладают исключительно высокой селективностью; при одинаковой степени превращения бензины, полученные на цеолитных катализаторах, отличаются более высоким содержанием олефинов и ароматических углеводородов;
) степень превращения на цеолитах за один проход при том же времени контакта выше, а превращение не сопровождается глубоким крекингом (с образованием газа и кокса);
) стабильность цеолитов выше; цеолитсодержащие катализаторы менее чувствительны к примесям металлов.
4.1 Катализ в переработке природного газа
Состав природного газа. Природный газ состоит, как правило, на 90-98% из метана. Из горючих газов в нем присутствуют также алканы CnH2n+2 Из них основную долю составляют этан и пропан, в меньших количествах - бутаны, пентаны, гексаны и более тяжелые углеводороды. В не-
больших количествах содержится водород, еще реже - СО. Из негорючих газов в природном газе присутствуют N2, Аг, СO2, Н2O, в очень небольших количествах - инертные газы: Не, Ne, Кr, Хе.
В зависимости от исходного состава природные газы делятся на чистые, или сухие, газы, в основном метан, и попутные газы, содержащие, помимо метана, от 1 до 60% других углеводородов. Ценность последних значительно выше, так как из них выделяют другие компоненты. Природные газы являются единственным сырьевым источником промышленного производства гелия. Его выделяют из газов, содержащих не менее 0.25% Не.
Природный газ, поступающий по газопроводу из Тюменской области в Центр, является почти чистым метаном. Он имеет следующий состав (в %): метан - 98.00, этан - 0.71, пропан - 0.20, бутан - 0.05, высшие углеводороды - 0.04, СO2 - 0.10, N2 - 0.90. Газы некоторых месторождений содержат большие количества этана, например, шебелинский газ - 4.0%, а усинский газ - даже 15%. Этан значительно дороже метана и его выделяют из природного газа для последующей переработки.
Применение природного газа является экологически более чистым и энергетически более выгодным топливом, чем нефть или каменный уголь. Поэтому быстрый рост добычи газа в основном обусловлен его применением в электростанциях и других энергетических устройствах для замены мазута и каменного угля. После того как в Москве перешли на газ как на главное топливо, атмосфера в городе значительно улучшилась.
4.2 Каталитическая очистка природного газа от серы
Сера в природном газе. Природный газ месторождений Тюменской и Сахалинской областей, Ставропольского и Краснодарского краев является чистым и содержит лишь малые количества серы (в виде H2S). Однако в га-зе некоторых месторождений имеются большие количества H2S. Например, газ месторождения Лак (Франция) содержит 42.4% H2S, месторождения Эмори (США) - 15.3%. В России в газах всех месторождений Оренбургской области содержится от 2 до 4% H2S, а в газах Астраханской области - от 5.6 до 33% H2S. Много серы в тенгизском газе Казахстана. Содержание H2S закономерно возрастает с ростом глубины залегания, что согласуется с гипотезой о существовании на глубине - 20 км пояса из расплава серы и сульфидов металлов.
Сероводород очень токсичен: уже при концентрации 0.01% может быть вызвана потеря сознания, а пребывание в среде с 0.1% H2S быстро приво-дит к смерти. Поэтому при добыче такого газа должны быть применены особые меры предосторожности. Долгое время по этой причине месторождения сероводородсодержащих газов подвергали консервации. Сейчас многие из них расконсервированы, потому что было признано, что для получения серы такой газ является технологически более удобным и дешевым сырьем, чем серные руды. В США и Канаде большую часть товарной серы получают из серосодержащих природных газов.
Освобождение природного газа от сероводорода осуществляют двумя способами:
) взаимодействием H2S с реагентом или сорбентом с последующей регенерацией сорбентов и утилизацией выделившихся сернистых соединений и 2) превращением H2S в элементную серу (S2 - → S°) с помощью катализа, а также высокой температуры или радиации.
Процесс Клауса. Наиболее распространенным
способом переработки сероводорода в серу является процесс Клауса, впервые
осуществленный в 1890 г. До 20 млн т/год серы в мире производится в процессе
Клауса. Он основан на следующих реакциях:
) H2S + 3/2О2 → SO2 + H2O,
) 2H2S + SO2 ↔ 3S + 2Н20;
протекают также такие реакции:
) H2S + 1/2O2 → S + H2O,
) S + O2 → SO2.
Собственно реакцией Клауса часто называют реакцию 2. Протекают также реакции взаимодействия метана и СO2 с H2S, SO2 и S.
Процесс Клауса разделяют на термическую и каталитическую стадии. Часть H2S сжигают в печи до SО2 + S. Вследствие высокой температуры (1100-1300°С) часть сероводорода в печи разлагается на Н2 + S. Кроме H2S и Н20 в газах имеются также СО2, COS, CS2, СО, Н2, углеводороды.