Материал: Гетерогенный катализ. Основные теории. Применение в нефтехимической промышленности
Гетерогенный катализ. Основные теории. Применение в нефтехимической промышленности
Федеральное агентство по рыболовству
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
"Астраханский государственный технический университет"
Кафедра "Органическая, биологическая
и физколлоидная химия"
Курсовая работа
по физической химии
Гетерогенный катализ. Основные
теории. Применение в нефтехимической промышленности.
Выполнил: студент группы ДХТ-31
Немгеров А.О.
Научный руководитель: доцент, к. х. н.
Летичевская Н.Н.
Астрахань 2012
Содержание
Введение
I. Гетерогенный катализ
II. Катализаторы гетерогенного катализа
2.1 Катализаторы-металлы
2.2 Смешанные катализаторы
2.3 Полифункциональные катализаторы
2.4 Основные требования к катализатору
III. Теории гетерогенного катализа
3.1 Мультиплетная теория
3.2 Теория активных ансамблей
3.3 Электронная теория
IV. Применение катализа в нефтехимической промышленности
4.1 Катализ в переработке природного газа
4.2 Каталитическая очистка природного газа от серы
Введение
КАТАЛИЗ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Термин "катализ" был введён в 1835 году шведским учёным Йёнсом Якобом Берцелиусом.
Катализаторы - вещества, изменяющие скорость химической реакции, которые могут участвовать в реакции, входить в состав промежуточных продуктов, но не входят в состав конечных продуктов реакции и после окончания реакции остаются неизменными.
Катализ бывает гомогенным и гетерогенным (контактным). Гомогенный катализ в включает в себя содержание одной фазы, то есть реагирующего вещества и катализатора. В гетерогенном катализе каталитическая система включает несколько фаз. В нефтепереработке гетерогенный катализ, особенно с твердым катализатором, распространен значительно больше, чем гомогенный. В данной работе будет рассматриваться гетерогенный катализ.
ГЕТЕРОГЕННЫЙ КАТАЛИЗ (контактный катализ), изменение скорости химической реакции при воздействии катализаторов, образующих самостоятельную фазу и отделенных от реагирующих веществ границей раздела.
Применение гетерогенного катализа имеет большое практическое значение и широко внедряется в промышленность. В связи с этим было проведено большое количество исследований для выяснения природы и механизма каталитического процесса на поверхности катализатора. Область применения гетерогенного катализа весьма широка и продолжает расширяться. В связи с заметным повышением стоимости нефти и истощением ее сырьевых ресурсов в недрах Земли ведутся большие исследования по каталитическим процессам химической переработки других горючих ископаемых (уголь, сланцы, природный газ) с целью получения топлив, углеводородов, кислородсодержащих органических соединений и других веществ. Не останавливаясь на других областях применения гетерогенного катализа, на основании изложенного можно сказать, что перспективы применения каталитических процессов чрезвычайно обширны, а их большое значение как прогрессивных промышленных методов бесспорно.
гетерогенный катализ катализатор газ
I. Гетерогенный катализ
В гетерогенном катализе реагирующие вещества и катализатор находятся в разных агрегатных состояниях. Наиболее часто катализатор представляет собой твердое вещество, а реагенты являются газами или жидкостями. Реакция протекает на поверхности катализатора. Следовательно свойства поверхности (площадь, химический состав поверхностного слоя, его структура) существенно влияют на активность катализатора.
Гетерогенный катализ - это каталитические процессы, происходящие па поверхности раздела фаз.
При этом катализатором является твердая фаза, а реагирующими веществами зачастую жидкая или газообразная фаза.
Гетерогенно-каталитические реакции широко применяются в промышленности, чем гомогенные и ферментативные. Это обусловлено тем, что твердые катализаторы легче отделить от жидкой или газообразной фазы, в которой содержатся реагенты. Катализатор действует не всей своей массой, а лишь поверхностными активными центрами. Поэтому скорость такой каталитической реакции уже не будет пропорциональной массе катализатора, как в гомогенном катализе, а зависеть от удельной площади поверхности катализатора. В промышленности применяют катализаторы в виде цилиндров, гранул диаметром несколько миллиметров, а также катализаторы, получаемые нанесением активного агента (платины, палладия) на пористый посей - активированный уголь, кизельгур, силикагель, алюмогель. Количество каталитически активного металла в нанесенном катализаторе не превышает нескольких процентов, что дает возможность экономить драгоценные дефицитные металлы. Из-за очень малых концентраций нанесенного металла на поверхности носителей находятся не микрокристаллы, а небольшие группы атомов, которые Кобозев назвал ансамблями. Он обратил внимание на то, что за увеличением количества нанесенного металла на носителе активность нанесенного катализатора проходит через максимум.
Для повышения активности, термодинамической устойчивости, механической жесткости применяют катализаторы в виде многокомпонентных систем - смешанные и промотированные. Смешанные катализаторы - это смесь двух или нескольких оксидов Al2О3, Сr2О3, СаО и МgO, активность которых является функцией состава. Часто к катализатору добавляют активаторы (промоторы), не имеющих каталитических свойств, но повышающие каталитическую активность катализатора. Например, для железного катализатора для синтеза аммиака нужен промотор оксид алюминия. Он покрывает тонкой пленкой поверхность катализатора и защищает его от рекристаллизации, сохраняя дефекты в поверхностном слое, т.е. удельную активность катализатора.
Во время гетерогенного катализа, как гомогенного, активность
катализатора со временем уменьшается из-за его отравления. Отравление может
быть обратное и необратимое. Соединения, содержащие серу, мышьяк отравляют
необратимо много металлических катализаторов. Следует отметить, что небольшое
количество яда существенно выливает на активность катализатора.
II. Катализаторы гетерогенного катализа
Важно понимать, что катализатор участвует в реакции. Обеспечивая более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. И перейдем к более важной теме это основной выбор промышленного катализатора и основные его типы.
2.1 Катализаторы-металлы
Металлы обычно значительно активнее оксидов и обладают более универсальным каталитическим действием, хотя, как правило, менее селективным. Наиболее универсальны металлы VIII гр. периодической системы, особенно Pt и Pd, катализирующие различные реакции окисления, гидрирования, дегидрирования и т.д. при низких температурах (комнатной и более низких). Каталитическая активность определяется электронной конфигурацией и симметрией d-орбиталей поверхностных атомов. В химическом взаимодействии с молекулами реагирующих на поверхности веществ участвуют только те d-орбитали, которые направлены от поверхности наружу и имеют одинаковую группу симметрии с молекулярными орбиталями реагентов. Участие d-электронов в химической связи металла с адсорбированными молекулами подтверждено методами фотоэлектронной и УФ-спектроскопии для Pt-катализатора. Металлы, находящиеся в конце переходных периодов, имеют в d-оболочке дырки (отсутствие электронов), что облегчает их участие в каталитическом превращении. Металлы, находящиеся в начале периода, обычно образуют прочную связь с молекулами реагентов. Это приводит к образованию фаз (поверхностных или объемных) оксидов, гидридов и т.п. и снижению каталитической активности металла. Так, Ni активен в реакциях гидрирования, а Сu малоактивна. При сплавлении активных металлов VIII группы с неактивными металлами 1б группы каталитическая активность уменьшается вследствие заполнения d-оболочки электронами. Например, для сплавов Cu-Ni падение активности наступает при составе 53% Сu и 47% Ni, когда s-электроны Сu заполняют J-оболочку Ni.
В реакциях с участием Н2 наиболее активны металлы, на поверхности которых происходит его хемосорбция с диссоциацией и низкой энергией связи атомарного водорода. Сплавы Cu-Ni, Au-Pt, Ag-Pd менее активны, чем чистые металлы VIII группы. На чистых металлах 1б группы Н2 не адсорбируется. В промышленности широко применяют мелкодисперсные металлические катализаторы, нанесенные на носители (SiO2, A12O3, алюмосиликаты, активный уголь, кизельгур и др.). Это повышает поверхность катализатора, уменьшает его расход, предохраняет частицы от спекания. По мере уменьшения размера частиц (повышения дисперсности) катализатора его активность в одних реакциях остается неизменной (структурно-нечувствительные или "незатрудненные" реакции), в других реакциях на частицах размером 2-4 нм при общем росте активности наблюдается снижение числа оборотов реакции; это так называемые структурно-чувствительные или "затрудненные" реакции. Так, большинство реакций гидрирования олефинов и ароматических соединений являются структурно-нечувствительными; реакции синтеза NH3, гидрогенолиза связи С-С, окисления, изомеризации и др. структурно-чувствительны. Различие между этими типами гетерогенно-каталитических реакций на металлах объясняют тем, что в первом из них активным центром является каждый атом поверхности, во втором-совокупность нескольких атомов. Разбавление в катализаторе-сплаве активного металла неактивным компонентом не влияет на его активность в структурно-нечувствительных реакциях и приводит к значительному ее снижению в структурно-чувствительных реакциях. Кроме того, в структурно-чувствительных реакциях активность катализатора зависит от выхода на поверхность кристаллических граней, ребер, концентрации дислокаций. Каталитическая активность металлов на носителях изменяется также вследствие их химического взаимодействия с носителем.
2.2 Смешанные катализаторы
В реакциях кислотно-основного типа (крекинг, дегидратация, изомеризация и др.) высокой активностью обладают катализаторы, состоящие из нескольких веществ, - оксиды металлов с различным зарядом катиона, аморфные алюмосиликаты и цеолиты, гетерополикислоты, сульфаты, фосфаты и др. Именно на поверхности смешанных систем легче образуются реакционноспособные заряженные частицы. Например, в алюмосиликатах ион А13+ замещает Si4+ в кремнекислородной решетке; меньший заряд Al3+ по сравнению с Si4+ компенсируется появлением центра Бренстеда Н+. Присоединение образовавшегося Н + к реагентам приводит к возникновению заряженных реакционноспособных частиц, например карбкатионов (СН3СН=СН2 + Н+ - > C3H7+), участвующих далее в катализе. На основных центрах образуются отрицательно заряженные частицы, в реакциях углеводородов-карбанионы.
2.3 Полифункциональные катализаторы
Промышленные каталитические процессы часто проводят на
катализаторах, сочетающих различные функции. Например, превращения
углеводородов в риформинге ускоряются катализаторами, в которых переходные
металлы, главным образом Pt или Ni, комбинируются с кислотным оксидом, например
алюмосиликатом или А12О3, модифицированным фтором. В этом
случае Pt оказывает дегидрирующее действие, а кислотный оксид-изомеризующее.
Катализ протекает вблизи границы раздела фаз или в результате перемещения
активной частицы из одной фазы в другую:
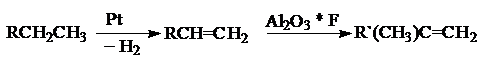
Полифункциональные катализаторы, как правило, состоят из
нескольких фаз, каждая из которых ускоряет одну из стадий сложного процесса.
Более 50 лет назад С.В. Лебедев совместно с сотрудниками подобрал селективный
катализатор синтеза бутадиена из спирта по реакции:
С2Н5ОН - > СН2=СНСН=СН2
+ 2Н2О + Н2
Были выделены стадии процесса: дегидратация, дегидрирование и
конденсация и для каждой из стадий подобран свой катализатор (активная глина,
ZnO и MgO соответственно). В смешанном катализаторе эти компоненты находятся в
соотношении, обеспечивающем максимальный выходбутадиена. Высокоселективные
катализаторы парциального окисления представляют смесь оксидов различных
металлов. Например, для окисления пропилена в акролеин применяют катализатор,
состоящий из оксидов Bi, Mo, Fe, Co и др. В этом катализаторе Bi2
(MoO4) служит для адсорбции и активации пропилена, FеМоО4-для
активации О2, на дефектах кристаллической структуры Fe2
(MoO4) 3 происходит перенос ионов кислорода от центров
его адсорбции к центрам адсорбции олефина, СоМоО4 служит для стабилизации
структуры FeMoO4.
2.4 Основные требования к катализатору
К промышленному катализатору предъявляют следующие требования:
. Катализатор должен быть высокоактивным. Произволительность ка-тализатора для многотоннажных процессов обычно должна быть выше 20 г/л*ч, в противном случае потребовались бы аппараты слишком большого объема или в слишком большом количестве. Наряду с химическим составом для активного катализатора необходимы высокая удельная поверхность и оптимальная пористая структура.
. Катализатор должен быть высокоселективным. В противном случае возрастают расходы на очистку и выделение конечных продуктов. Желательна 100% -я селективность" но она труднодостижима. Заметим, что для получения высокоселективного катализатора высокая удельная поверхность необязательна. Требуемая величина селективности для разных процессов различна; она определяется экономическими соображениями исходя из доли стоимости сырья в цене конечного продукта.
. Катализатор должен обладать достаточной устойчивостью к травлению каталитическими ядами. В том числе желательно минимизировать отложение кокса на поверхности катализатора в органических реакциях, максимально удлинить период работы катализатора до регенерации.
. Катализатор не должен быть чересчур чувствительным к перегревам в экзотермических реакциях. Важно, чтобы перегрев на 50-100°С выше регламентированной температуры процесса не приводил к необратимой потере активности.
. Приготовление катализатора должно быть хорошо воспроизводимым. По составу и структуре вся масса катализатора и каждая гранула в отдельности, должны быть однородными.
. Катализатор должен быть механически прочным таблетки не должны раздавливаться под тяжестью слоя катализатора и разрушаться при свободном падении с высоты, несколько превышающей высоту контактного аппарата. При точечном характере нагрузки на зерно в высоком контактном слое последняя может достигать значительных величин и носить, скорее, раскалывающий, чем раздавливающий характер.
. Катализатор должен иметь высокую механическую прочность на истирание. Особенно высокие требования к прочности на истирание предъявляются к катализатору, работающему в условиях подвижного слоя с циркуляцией или в кипящем слое.
. Катализатор не должен терять активность, селективность или механическую прочность под влиянием процессов, протекающих на его поверхности.
. Продолжительность работы катализатора, независимо от причин, ее определяющих, не должна быть слишком малой. При нормальной промышленной эксплуатации катализатор не должен перегружаться чаще, чем один раз в месяц.
. Желательно, чтобы технологии приготовления и производства катализаторов были не слишком сложными. В их производстве желательно использовать чистые материалы. Примеси в исходном сырье, в том числе примеси в технологической воде, могут сильно уменьшить активность и селективность. В ряде катализаторных производств используют очищенную или даже дистиллированную воду.
. Стоимость катализатора обычно составляет несколько
процентов от стоимости продукта. В некоторых случаях, например для катализаторов
из драгоценных металлов или другого дефицитного сырья, вопрос уменьшения
стоимости является одним из наиболее важных.
III. Теории гетерогенного катализа
В теории гетерогенного катализа постулируется наличие на поверхности катализатора особых участков - активных центров, на которых происходит активация реагирующих молекул и их взаимодействие с образованием продуктов реакций и освобождением активных центров для следующих взаимодействий.