Материал: Фотоповреждение клеток и клеточных структур ультрафиолетовым излучением
.3 Фотоинактивация клеток
Чувствительность клеток к ультрафиолетовой инактивации зависит как от вида клеток и их функционального состояния, так и от параметров облучения - длины волны, интенсивности, времени облучения и т.д.
Видовые различия в чувствительности разных
клеток к УФС излучению (254 нм) отображены в таблице 4. Клетки эукариот более
чувствительны к ультрафиолетовому воздействию, чем клетки микроорганизмов.
Высокая устойчивость некоторых видов к УФ воздействию (грибов, инфузорий)
возможно, связана с полиплоидией, т.е. с многократным дублированием, наличием
нескольких копий ДНК в клетках, а следовательно, с наличием нескольких мишеней.
Таблица 4. Летальные дозы LD90 ультрафиолетового излучения
(254 нм) для разных клеток
|
Летальные дозы LD90 (мДж/см2) |
|
|
Эукариоты (млекопитающие) Бактерии Микрококки Грибы Инфузории Морской жгутиконосец Bodo marina |
1-3 5 (споры: ~10) 50-130 50-90 50-100 1120 |
Обычно делящиеся эпителиальные клетки значительно чувствительней, чем неделящиеся нервные клетки. Наибольшей фоточувствительностью в организме млекопитающих отличаются тимоциты (лимфоциты зобной железы). Но раковые клетки, однако, довольно устойчивы к ультрафиолетовому воздействию, несмотря на то, что они подвержены неконтролируемым делениям.
УФ-чувствительность клеток также зависит от клеточного цикла. В фазе митоза клетки мало чувствительны. Наибольшей фоточувствительностью клетки обладают в фазе G1. В этой фазе наиболее чувствительным компонентом ядра являются ядрышки, в которых синтезируется рибосомная РНК и собираются рибосомные субъединицы. Локальное ультрафиолетовое облучение ядрышек сфокусированным микролучом останавливает митоз. В фазе S, когда происходит копирование ДНК, клетки менее чувствительны к ультрафиолетовому воздействию. Однако, облучение клеток в фазе S вызывает наибольшее число хромосомных повреждений: разрывов, обменов и т.д. Механизм фотоповреждения клеток в фазе G2 отличен от механизма фотоповреждений клеток в фазах G1 и S.
Анаэробные клетки устойчивей к ДНК, чем аэробные. Это, очевидно, обусловлено тем, что митохондрии, участвующие в окислительном обмене, являются важной мишенью ультрафиолетового повреждения клеток. Это подтверждается тем, что УФ-чувствительность аэробных клеток повышается в аноксических условиях.
Кроме гибели клеток ультрафиолетовое излучение вызывает мутации и подавление клеточного деления (пролиферации). Спектр действия обоих эффектов имеет максимум 260 нм, что говорит, что за них ответственно повреждение ДНК, но определенной эффективностью обладает и более длинноволновое излучение. Основным их механизмом, как говорилось выше, является появление тиминовых димеров и другие повреждения ДНК.
Интересно, что малые дозы ультрафиолета не
повреждали клетки, а, наоборот, стимулировали деление. В этом случае спектр
действия соответствовал поглощению света белками, но не ДНК. Возможно, такое
облучение действует через белки, управляющие процессом деления, запускающие
митоз, или снимает ингибирующее действие каких-то белковых факторов.
Сравнение влияния на клетки ультрафиолетового излучения диапазонов UVС, UVB, UVA и видимого света
|
UV-B и UV-C |
UV-A и BC |
|
Повреждения ДНК фотореактивируются видимым светом и подвергаются темновой репарации. |
Повреждения ДНК не репарируются и не фотореактивируются |
|
Нет зависимости от концентрации О2, т.е. синглетный механизм |
Есть зависимость от концентрации О2, т.е триплетный механизм. |
|
Спектры мутаций для этих спектральных областей различаются |
|
Ближний ультрафиолет вызывает похожие эффекты,
но при дозах на 3-5 порядков больших, чем дальний. Сравнение действия ближнего
и дальнего ультрафиолета на клетки (Табл.5) показывает, что в отличие от
диапазона UVA, повреждения ДНК коротковолновым излучением репарируются и
фотореактивируются видимым светом. Эти изменения не зависят от присутствия
кислорода в среде, т.е. происходят по синглетному, а не триплетному механизму.
Различны и спектры вызываемых ими мутаций. Но цитоплазматические структуры
изменяются сходным образом.
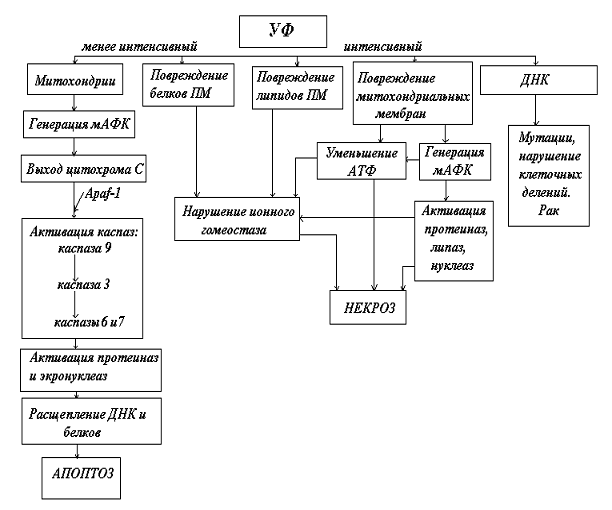
Рис.9. Схема ультрафиолетового повреждения
клетки. В зависимости от интенсивности ультрафиолетовое излучение может вызвать
некроз или апоптоз клеток
Схема повреждений клетки коротковолновым ультрафиолетовым излучением (УФВ и УФС) приведена на рис.9. На ней сравнительно интенсивное облучение (мера интенсивности зависит от вида и состояния клеток), способное существенно повредить клеточную мембрану, индуцировав в ней перекисное окисление липидов, нарушения проницаемости и ионного гомеостаза, приводит к некрозу. Этому способствует повреждение митохондрий и падение синтеза АТФ. Одновременно возникают повреждения ДНК, мутации, нарушения клеточных делений, ведущие к раку. Сравнительно слабое, но продолжительное воздействие, не так существенно повреждающее плазматическую мембрану и производство АТФ, может вызвать апоптоз. Этому способствует генерация вторичных АФК в митохондриях, высвобождение из них цитохрома с и других проапоптозных белков, которые активируют каскад каспаз, протеиназ и нуклеаз. Последние расщепляют клеточные белки и нуклеотиды и осуществляют апоптоз.
Следует рассмотреть подробнее, что происходит при повреждении ДНК. Нам пока далеко не все известно, но данные последних лет выявляют важные детали механизмов, определяющих дальнейшую судьбу клеток. Появление множественных однонитевых разрывов в молекулах ДНК активирует фермент PARP-1 - полимеразу 1 поли(АДФ-рибозы). Этот фермент направляет репаративный комплекс к сайтам повреждения ДНК путем присоединения к ним цепочки из полиадениловых нуклеотидов (поли-А) (Рис.10). Через короткое время цепочка поли-А разбирается. Это требует большого количества NAD и быстро истощает ресурсы АТФ. Большое количество АТФ также потребляется шаперонами, исправляющими конформацию поврежденных белков (heat shock response). Это снижает возможности ионных насосов по поддержанию ионных градиентов и мембранного потенциала.
Нарушения цитоскелета приводят к нарушениям межклеточных контактов, формы и подвижности клеток. В результате повреждения митохондрий из них может высвободиться цитохром с, инициирующий апоптоз. Апоптоз также может запускаться белком p53 (Рис.11), чувствительным к повреждениям ДНК.
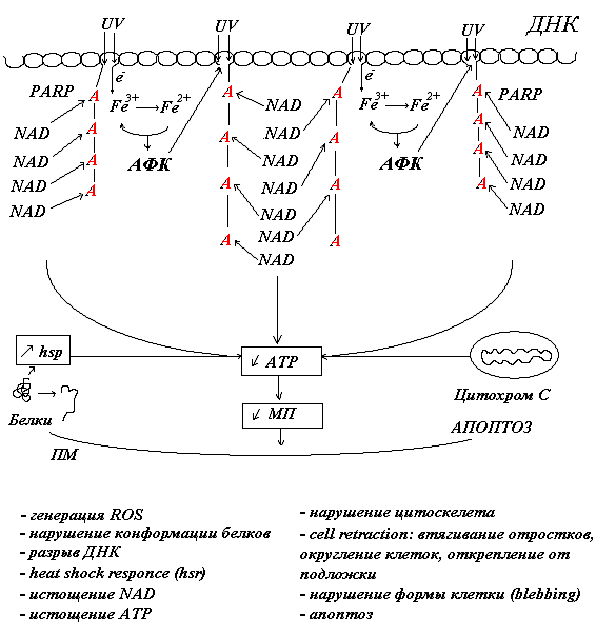
Рис.10. Полиаденилирование ДНК в местах разрывов
цепи белком PARP привлекает к ним репарационный комплекс, но истощает запасы
АТФ. Ниже указан список УФ-индуцированных функциональных нарушений в клетках
Он активирует множество внутриклеточных мишеней,
включая белок р21, приводящий к остановке клеточного цикла, что необходимо
осуществления процессов репарации ДНК. Если повреждения ДНК не удается
репарировать, то поврежденная клетка уничтожается путем Bax-опосредованного
апоптоза. Иногда мутации затрагивают сам белок р53, что случается примерно у 50
% раковых клеток. В этом случае апоптоз не происходит, и клетки неконтролируемо
делятся, приводя к раку.
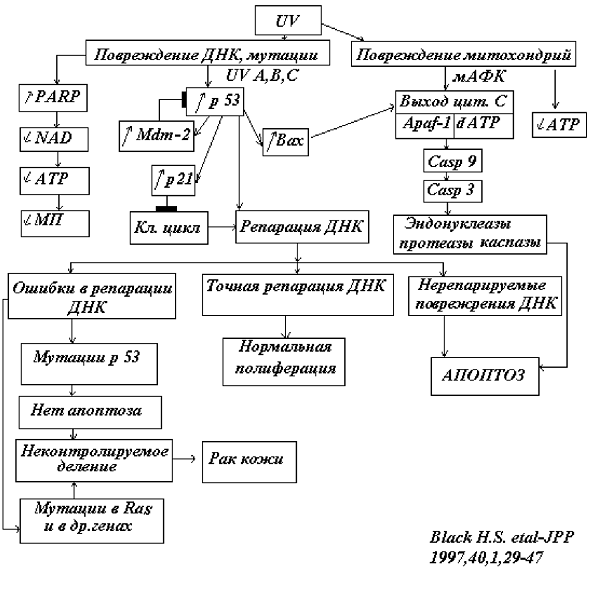
Рис.11. Комплекс изменений в клетках, облученных
коротковолновым ультрафиолетовым излучением
Литература
1. Ремизов А.Н.: Сборник задач по медицинской и биологической физике. - М.: Дрофа, 2011
2. Ремизов А.Н.: Сборник задач по медицинской и биологической физике. - М.: Дрофа, 2011
. Сост. В.А. Тихомирова, А.И. Черноуцан: Физика и биология. - М.: Бюро Квантум, 2011
. А.М. Черныш и др. ; Под ред. В.Ф. Антонова ; Рец.: Каф. биофизики биологического фак. и др.: Биофизика. - М.: Владос, 2010
. А.М. Черныш и др. ; Под ред. В.Ф. Антонова ; Рец.: Каф. биофизики биологического фак. МГУ им. М.В. Ломоносова и др.: Биофизика. - М.: ВЛАДОС, 2010
. Дьяков Ю.Т.: Введение в альгологию и микологию. - М.: МГУ, 2010
. под ред. Ю.А. Ершова: Общая химия ; Биофизическая химия ; Химия биогенных элементов. - М.: Высшая школа, 2010
. Логвиненко А.Г.: Лабораторный практикум по медицинской и биологической физике, медицинской аппаратуре. - Белгород: БелГУ, 2009
. Ремизов А.Н.: Медицинская и биологическая физика. - М.: Высшая школа, 2009
. Титомир Л.И.: Математическое моделирование биоэлектрического генератора сердца. - М.: Наука: Физматлит, 2009
. Чернавский Д.С.: "Белок-машина". - М.: Янус-К, 2009
. БелГУ; Сост.: В.П. Воронов, В.В. Сыщенко, Г.И. Ткаченко; Рец. Г.Н. Положенцев: Концепция современного естествознания. - Белгород: БелГУ, 2008
. Орлов И.В.: Вестибулярная функция. - СПб.: Наука, 2008
. Бернштейн Н.А.: Биомеханика и физиология движений. - М. ; Воронеж: Институт практической психологии : МОДЕК, 2007
. Ремизов А.Н.: Медицинская и биологическая физика. - М.: Высшая школа, 2006
. Сергеев Б. : Как мозг учился думать. - М. : Цитадель, 2005
. Артюхов В.Г.: Биофизика. - Воронеж: ВГУ, 2004
. Авт.: Л.К. Зарембо, Б.М. Болотовский и др.; Сост. В.Н. Руденко: Школьникам о современной физике. - М.: Просвещение, 2010
. Коломийцева И.К.: Радиационная биохимия мембранных липидов. - М.: Наука, 2009
. Ремизов А.Н.: Медицинская и биологическая физика. - М.: Высшая школа, 2007
. Ремизов А.Н.: Сборник задач по медицинской и биологической физике. - М.: Высшая школа, 2007
. Эссаулова И.А.: Руководство к лабораторным работам по медицинской и биологической физике. - М.: Высшая школа, 2007
. Богданов К.Ю.: Физик в гостях у биолога. - М.: Наука, 2006
. Мэрион Дж.Б.: Общая физика с биологическими примерами. - М.: Высшая школа, 2006
. Сергеев Б.Ф.: Ступени эволюции интеллекта. - Л.: Наука, 2006
. Казаков Б.И.: Лаборатория внутри нас. - М.: Знание, 2004
. Романовский Ю.М.: Математическая биофизика. - М.: Наука, 2004
. Сергеев Б.Ф.: Ум хорошо.... - М.: Молодая гвардия, 2004