Материал: Фотоповреждение клеток и клеточных структур ультрафиолетовым излучением
Фотоповреждение клеток и клеточных структур ультрафиолетовым излучением
Контрольная работа
Фотоповреждение
клеток и клеточных структур ультрафиолетовым излучением
Содержание
Введение
. Фотоповреждение нуклеиновых кислот ультрафиолетовым излучением
. Защита клеток от фотоповреждения ДНК
.1 Нуклеотид-эксцизионная репарация повреждений ДНК
.2 Фотореактивация
. Фотоповреждение аминокислот и белков ультрафиолетовым излучением
. Влияние ультрафиолетового излучения на биомембраны
. Действие ультрафиолетового излучения на клетки
.1 Мембранные процессы
.2 Митохондрии
.3 Фотоинактивация клеток
Литература
Введение
В большинстве случаев деструктивным является коротковолновый УФ (< 320 нм), энергия кванта которого сопоставима с энергией различных химических связей. Эффективность более длинноволнового излучения значительно ниже, но он также может влиять на биологические объекты. Этот свет является экологически значимым фактором. В отличие от коротковолнового ультрафиолета, который поглощается озоном в верхних слоях атмосферы, световое излучение с длиной волны более 320 нм достигает поверхности Земли.
1. Фотоповреждение нуклеиновых кислот ультрафиолетовым излучением
фотоповреждение ультрафиолетовый нуклеиновый клетка
После того, как Ф.Гейтсом (1928-1930) и Л. Стадлером и Ф. Угером (1942) было обнаружено соответствие спектров действия летального и мутагенного действия ультрафиолета и спектра поглощения нуклеиновых кислот стало ясно, что фотоповреждение именно нуклеиновых кислот, а не белков или других структур, ответственно за эти эффекты.
Максимумы поглощения ультрафиолетового излучения всех азотистых оснований, входящих в состав ДНК, кроме гуанина, находятся в области 260-265 нм. Гуанин имеет двойную полосу поглощения в этой области с максимумами около 247 и 277 нм. При формировании двойной спирали поглощение уменьшается (гипохромный эффект).
При поглощении ультрафиолетовых квантов с длиной волны около 260 нм азотистые основания нуклеиновых кислот переходят в возбужденное состояние, в котором они могут подвергаться превращениям. При однофотонном возбуждении ДНК могут происходить следующие фотодеструктивные реакции:
- Димеризация пиримидиновых оснований, главным образом, тимина;
- Гидратация азотистых оснований;
- Образование межмолекулярных сшивок ДНК-ДНК, ДНК-белок, белок-белок;
- Одно- или двухнитевые разрывы цепей.
Считается, что образование димеров пиримидиновых оснований, главным образом тимина, ответственно за 70-80 % всех летальных повреждений, индуцируемых в клетках коротковолновым ультрафиолетовым излучением, а пуриновые основания и углеводные группы нуклеиновых кислот значительно менее фоточувствительны.
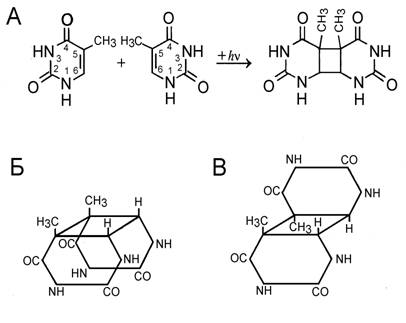
Рис.1. Образование димеров тимина по действием
ультрафиолетового излучения (А) и их пространственная структура. Форма (Б)
образуется между соседними молекулами тимина на одной цепи ДНК; форма (В) -
между разными цепями
Под действием ультрафиолетового излучения в молекуле тимина разрываются двойные связи между 5- и 6-м атомами углерода и образуется квадратное циклобутановое кольцо (Рис. 1А), прочно соединяющее два тимина: Т^Т. При этом возможно образование разных циклобутановых структур, соединяющих тимины, расположенные рядом на одной цепи ДНК (Рис.1Б), или принадлежащие разным ДНК (Рис.1В). Однако, в нативной ДНК два тимина не могут располагаться друг против друга, поскольку по принципу комплементарности напротив тимина должен располагаться аденин. Сближение тиминов, принадлежащих разным цепям ДНК, возможно только при денатурации ДНК и частичном расплетании двойной спирали. В этом случае образование циклобутановых димеров будет закреплять локальную денатурацию. Число образующихся димеров зависит от числа расположенных рядом тиминов в ДНК. Кроме того, образование димеров зависит от длины волны ультрафиолетового излучения.
Спектр действия димеризации тимина близок к суммарному спектру поглощения всех азотистых оснований ДНК. Он имеет максимум при 260 нм (Рис.2, сплошная линия). По-видимому, он обусловлен поглощением квантов не только тимином, но и другими основаниями в ДНК. Это может происходить в результате миграции энергии света от различных оснований, возбужденных ультрафиолетом, на тимин с последующей димеризацией. Механизм миграции энергии между азотистыми основаниям не вполне ясен: ферстеровский индуктивно-резонансный механизм предполагает способностью донора флуоресцировать, а у азотистых оснований время жизни флуоресценции и квантовый выход очень малы. Возможно, более вероятна обменно-резонансная миграция энергии с участием триплетных уровней нуклеотидов, которая происходит безизлучательно, если электронные оболочки находящихся рядом молекул перекрываются. Действительно, исследование спектров фосфоресценции нуклеотидов показало, что энергия триплетных состояний снижается в ряду: Ц > Г > А > Т. Это подтверждает потенциальную возможность миграции энергии от других оснований на тимин. Тушители триплетных состояний, такие как краситель акрихин, снижают димеризацию тимина и защищают вирусы от фотоповреждения ДНК, вероятно, вследствие триплет-триплетного переноса энергии электронного возбуждения с ДНК на краситель.
Тиминовые димеры очень прочны. Они не разрушаются ни при нагревании, ни при действии различных химических агентов. Только сам ультрафиолет способен их разрушить. Спектр действия фоторазрушения димеров тимина (Рис.2, прерывистая линия) существенно отличается от спектра действия их образования (Рис.2, сплошная линия). Эти спектры пересекаются при 254 нм, поэтому при меньших длинах волн более эффективен процесс разрушения димеров, а при больших - образования. Такая разница связана с разными спектрами поглощения димеров и мономеров.
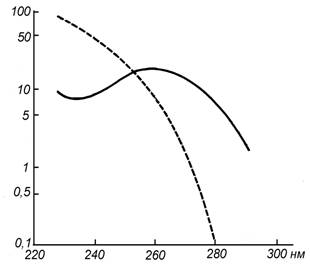
Рис.2. Спектры действия образования (сплошная
линия) и разрушения димеров тимина (прерывистая линия) под действием
ультрафиолетового излучения. По оси ординат отложена эффективность этих
процессов в относительных единицах. (По: Смит, Хэнеуолт, 1972)
Димеры тимина нарушают двухспиральную структуру ДНК. При репликации ДНК или транскрипции ферменты ДНК-полимераза или РНК-полимераза, дойдя до такого структурного дефекта останавливаются и прекращают синтез, а иногда “прочитывают” димер неверно, делая ошибку считывания. В случае репликации это приводит к мутации. Поэтому коротковолновый ультрафиолет является мутагеном и оказывает летальное действие. Но в клетках есть специальные механизмы репарации, устраняющие такие дефекты (см. ниже).
Аналогично димеризации тимина, может происходить димеризация урацила (У^У), цитозина (Ц^Ц) или образование смешанных димеров: (У^Ц; У^Т; Ц^Т). Но эффективность этих процессов ниже, а кроме того образующиеся димеры неустойчивы и в темноте могут мономеризоваться. (Возможно, однако, темновое дезаминирование цитозина в димерах Ц^Ц в результате чего они превращаются в димеры У^У, которые впоследствии мономеризуются, что приводит к мутациям.
Возможны и другие фотоповреждения ДНК.
Фотогидратация - присоединение молекулы воды к пиримидиновым основаниям
(Рис.3). Фотогидраты образуются только в растворах свободных цитозина или
урацила или в однонитевой ДНК или РНК. В двухцепочечной ДНК они не обнаружены.
Этот процесс идет через синглетные возбужденные состояния пиримидинов, т.к.
тушители триплетов (О2) на него не влияют.
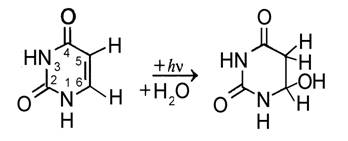
Рис.3. Фотогидратация урацила.
Ультрафиолетовое излучение также может вызывать образование межмолекулярных сшивок ДНК с белками. Сшивки ДНК-белок выявляются по ухудшению экстрагируемости ДНК из облученных клеток, которая восстанавливается после обработки трипсином, разрушающим белки. Фотоакцептором в этом случае могут служить как ДНК, так и белки. При этом группы -SH или -ОН аминокислот серина, тирозина, треонина, цистеина или метионина могут присоединяться к 5 или 6-му атомам углерода в тимине или цитозине (Рис.4). Наибольшей способностью связываться с ДНК обладают цистеин и тирозин.
В образовании сшивок могут также участвовать лизин, аргинин, гистидин и триптофан.
Внутримолекулярные сшивки между двумя
комплементарными нитями ДНК обнаруживаются но неспособности УФ-облучения ДНК
расплетаться на отдельные нити при денатурирующих воздействиях. Они иногда
образуются за счет образования тиминовых димеров Т^Т, формирующих
транс-структуру (Рис.1В). Межмолекулярные сшивки ДНК-ДНК найдены только при
облучении сухих препаратов ДНК, а во влажных и в клетках они не выявлены.
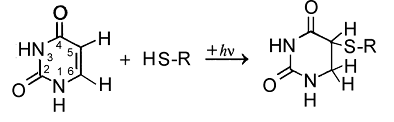
Рис.4. Фотоиндуцированное образование сшивки
между SH-группой цистина, входящего в состав белка (R), и урацилом
При действии коротковолновых УФ фотонов с большой энергией или при высокоинтенсивном лазерном облучении возможны одно- или даже двухнитевые разрывы ДНК, хотя вероятность этих процессов значительно ниже вероятности димеризации тимина.
В последнее время начало исследоваться
биологическое действие вакуумного ультрафиолета с длиной волны 193 нм, энергия
квантов которого столь высока, что способна, возбудив молекулу на высокие
уровни энергии Sо®S2, ионизировать азотистые
основания, оторвав от них электроны. В таблице 1 приведены данные о квантовых
выходах различных фотопродуктов в двухнитевой ДНК при действии коротковолнового
(254 нм) и вакуумного УФ (193 нм).
Таблица 1. Квантовые выходы (х104) различных фотопродуктов в двухнитевой ДНК при действии коротковолнового (254 нм) и вакуумного (193 нм) ультрафиолетового излучения (По данным Г.Б. Завильгельского, 1996)
|
Фотопродукты |
Длина волны облучения, нм |
|
|
|
193 |
254 |
|
Пиримидиновые димеры |
18 |
30 |
|
(6-4)-аддукты |
5 |
1,5 |
|
Фотогидраты |
- |
3 |
|
Однонитевые разрывы |
15 |
0,4 |
|
Двухнитевые разрывы |
0,6 |
0,01 |
|
Потеря азотистых оснований (например, отрыв тимина) |
18 |
0,2 |
|
Межнитевые сшивки |
0,01 |
|
|
Локальные денатурированные участки |
1 |
0,01 |
По этим данным, при действии ультрафиолета с длиной волны 254 нм основную роль в повреждении ДНК играют образование димеров, фотогидратов и 4-6-аддуктов. Более существенные повреждения ДНК (разрывы, сшивки) редки. Но при облучении вакуумным ультрафиолетом их роль, особенно однонитевых разрывов и потери азотистых оснований, резко повышается.
Повреждение нуклеиновых кислот происходит и при двухступенчатом (Sо ® S1 ® S2) возбуждении молекулы мощной лазерной вспышкой, когда поток фотонов столь интенсивен, что за время жизни возбужденного синглетного состояния (1-10 нс) молекула может поглотить ещё один фотон и перейти на второй возбужденный уровень с примерно вдвое большей энергией. При высокой интенсивности лазерного излучения, в принципе, возможны и нелинейные двухквантовые переходы сразу на высокие энергетические уровни в результате одновременного поглощения двух квантов через виртуальное промежуточное состояние. В обоих последних случаях количество двухквантовых фотопродуктов, а следовательно и определяемый ими биологический эффект, быть пропорционально квадрату интенсивности излучения. По данным П.Г. Крюкова и соавторов (1978), процесс фоторазложения (фотолиза) тимина под влиянием высоко интенсивного импульсного пикосекундного лазерного облучения (266 нм, 1012-1013 Вт/см2) происходит по двухступенчатому механизму. Возможно, этот механизм реализуется и в других случаях. Порог наблюдения таких нелинейных эффектов порядка 109 Вт/см2.
Двухступенчатое возбуждение, в отличие от
одноквановых процессов, может привести к ионизации азотистых оснований
нуклеиновых кислот. Катион-радикалы азотистых оснований, образующиеся при
отрыве электрона, играют ключевую роль в формировании разрывов ковалентных
связей в ДНК. Квантовый выход однонитевых разрывов ДНК резко возрастает при
увеличении интенсивности лазерной вспышки, что свидетельствует о наличии порога
двухфотонного поглощения света. Г.Б. Данные о квантовых выходов разных типов
фотоповреждений ДНК при действии низкоинтенсивного и высокоинтенсивного
ультрафиолетового излучения (Табл.2) показывают значительное увеличение выхода
фотопродуктов, требующих образования ион-радикалов азотистых оснований.
Эффективность димеризации пиримидинов, однако, падает при увеличении
интенсивности облучения с 3 до 1·10-3,
вероятно, вследствие опустошения уровня S1 при поглощении второго кванта.
Таблица 2. Квантовые выходы образования фотопродуктов повреждения ДНК при действии низкоинтенсивного (11 Вт/м2) и высокоинтенсивного (l=266 нм; I=4·1013 Вт/м2) импульсного ультрафиолетового излучения с длиной волны 266 нм (Завильгельский, 1996)
|
Фотопродукт |
Низкоинтенсивное излучение |
Высокоинтенсивное излучение |
|
Пиримидиновые димеры |
3·10-3 |
1·10-3 |
|
Однонитевые разрывы |
2·10-5 |
1·10-3 |
|
Межнитевые сшивки |
2·10-6 |
4·10-5 |
В последние годы обнаружено, что длинноволновое ультрафиолетовое облучение (УФА) в области 320-400 нм, не поглощающееся ДНК, также способно повреждать ДНК. Квантовые выходы этих процессов очень малы. Их удается обнаружить только при интенсивностях или дозах облучения, на 2-3 или 5-6 порядков, соответственно. превышающих интенсивности или дозы ультрафиолетового облучения с длиной волны 254 нм. Основными повреждениями ДНК при этом являются пиримидиновые димеры и одноцепочечные разрывы, образующиеся с примерно одинаковым квантовым выходом. Показано, что образование димеров не зависит от присутствия кислорода, мощного тушителя триплетных состояний, а разрывов - зависит. Следовательно, механизмы этих двух видов фотоповреждения ДНК различны: в первом случае процесс, видимо, происходит с синглетных уровней, а во втором - с триплетных. При этом ДНК не является первичным хромофором, так как она не поглощает свет в этой области. Вероятно, ее повреждение опосредовано каким-то эндогенным фотосенсибилизатором.
Ультрафиолетовое облучение нарушает все
известные функции нуклеиновых кислот: способность к репликации и транскрипции у
ДНК вызывает появление мутаций, а следовательно и модификацию белков, структура
которых закодирована в ДНК. Повреждения мРНК и тРНК делают невозможным синтез
белков.
2. Защита клеток от фотоповреждения ДНК