Материал: Фотоповреждение клеток и клеточных структур ультрафиолетовым излучением
В клетках есть ряд специальных систем,
защищающих ДНК от фотоповреждения и репарирующих повреждения ДНК, которые могут
привести к наследуемым генетическим сдвигам.
2.1 Нуклеотид-эксцизионная репарация повреждений
ДНК
Система нуклеотид-эксцизионной репарации устраняет крупные структурные дефекты на одной из нитей ДНК. К наиболее распространенным дефектам такого рода, возникающим под действием ультрафиолетового облучения относятся пиримидиновые димеры, в частности, связанные циклобутановым мостиком димеры тимина (Рис.5).
В клетках есть специальный мультиферментный комплекс, двигающийся по ДНК отыскивающий структурные нарушения двойной спирали ДНК, такие как димеры тимина, и устраняющий повреждения. Механизм его движения и быстрого поиска дефектов пока неизвестен. Поскольку в месте локализации димеров или (6-4)-аддуктов образуется структурный дефект с нарушением комплементарного спаривания оснований двухцепочечной ДНК, то дойдя до такого дефекта, фермент эксинуклеаза делает однонитевые разрывы с двух сторон от дефекта.
У бактерий E.coli эксинуклеаза - это крупный
белковый комплекс, состоящий из трех субъединиц: UvrA
(104 кДа), UvrB (78 кДа) и UvrC
(68 кДа). Он гидролизует пятую межнуклеотидную связь с 3’ стороны перед
дефектным участком и восьмую с 5’ стороны после него. У эукариот аналогичный
расщепляется шестая связь с 3' стороны и двадцать вторая с 5' стороны. Затем
геликаза раскручивает спираль, разрушая водородные связи. При этом удаляется
значительный сегмент ДНК с дефектным участком внутри - 12-13 нуклеотидов у
прокариот и 27-29 нуклеотидов у эукариот, расчищая таким образом свободное
место для дальнейшей работы. Затем ДНК-полимераза I
по принципу комплементарности достраивает недостающие нуклеотиды, и, наконец,
ДНК лигаза соединяет 3'-конец вновь построенной цепочки с 5’-концом старой
цепочки (Рис.5). Эта система, в принципе, очень сходна с РНК-полимеразой,
синтезирующей мРНК.
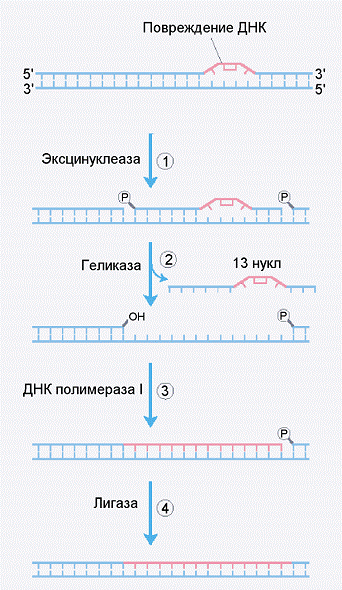
Рис. 5 Нуклеотид-эксцизионная репарация
повреждений ДНК
Система темновой репарации весьма эффективна, она репарирует до 90-98% всех повреждений.
2.2 Фотореактивация
А. Келнер (1949) обнаружил, что ультрафиолетовые повреждения ДНК могут устраняться при последующем облучении более длинноволновым светом в области 350-450 нм с максимумом около 380 нм. Оказалось, что специальный фермент фотолиаза способна разрушать циклобутановые пиримидиновые димеры (вспомним, что на них не действуют ни температура, ни химические воздействия). Этот фермент работает только под действием света, т.е. в электронно-возбужденном состоянии, за счет энергии которого формируются радикалы, разрушающие циклобутановые мостики. Долгое время был неизвестен первичный хромофор, поглощающий свет. Однако, недавно были получены высокоочищенные препараты фермента, которые обладали поглощением света в области, соответствующей спектру действия фотореактивации клеток. Было показано, что фотолиаза содержит два светопоглощающих кофактора. Один из них имеет флавиновую природу. Это флавинадениндинуклеотид, FADH¾. У бактерий E.coli и дрожжей. Второй хромофор - производное фолиевой кислоты N5,N10-метенилтетрагидрофолилполиглутамат (MTHFpolyGlu). Именно он поглощает квант синего света и передает энергию электронного возбуждения на FADH-. Возбужденный флавин *FADH- отдает свой электрон пиримидиновому димеру, становясь радикалом *FADH и превращая последнего в нестабильный радикал. В результате последующих перегруппировок полученный электрон переносится на кислородный атом одного из тиминов, циклобутановая связь разрушается, а лишний электрон снова передается на флавиновый радикал, возвращая его в исходное состояние FADH-. У млекопитающих, включая человека, фотолиаза отсутствует.
3. Фотоповреждение аминокислот и белков
ультрафиолетовым излучением
Как рассмотрено выше, ультрафиолетовое излучение поглощается главным образом аминокислотами триптофаном, тирозином и фенилаланином. Эти аминокислоты высоко чувствительны к повреждающему действию ультрафиолета. Но наибольшей фоточувствительностью к коротковолновому ультрафиолетовому излучению в белках отличаются дисульфидные мостики, разрываемые при поглощении фотона. Это подтверждают данные Табл. 3 о молярных коэффициентах поглощения e, квантовых выходах j и поперечных сечениях фотоинактивации s основных хромофорных групп в белках для УФС излучения с длиной волны 254 нм. Они демонстрируют в 3 раза большую чувствительность (-S-S-) сшивок по сравнению с триптофаном. Фотодеструкция фенилаланина, тирозина, а также пептидных связей намного менее существенна.
При облучении УФВ светом с длиной волны более
280 нм фотоповреждение белков в большей мере обусловлено поглощением триптофана
и тирозина. Основной процесс УФ- модификации ароматических аминокислот -
образование катион-радикалов ·АН+:
АН ![]() АН*
АН*![]() ·АН+
+ e-
·АН+
+ e-
При этом от них отщепляется
электрон, который тут же сольватируется, т.е. покрывается оболочкой из
ориентированных вокруг него диполей воды.
Таблица 3. Фотохимические свойства аминокислот (при lmax=254 нм) (По Смиту и Хэнеуолту, 1972)
|
Соединение |
e, л/моль×см |
j |
s × 1020, см2 |
|
Цистин (-S-S-) Триптофан Фенилаланин Тирозин Пептидные связи |
270 2870 140 320 0,2 |
0,13 0,004 0,013 0,002 0,05 |
13,4 4,4 0,69 0,23 0,004 |
Схема фотопревращений ароматических аминокислот, описанная Д.И. Рощупкиным, представлена на Рис. 6. Радикалы аминокислот неустойчивы и в присутствии кислорода они подвергаются окислению. В результате фенилаланин превращается в тирозин, тирозин - в диоксифенилаланин, а триптофан - в формилкинуренин.
Сольватированные электроны также вступают в
реакцию и сенсибилизируют повреждение аминокислот. Особенно чувствительны к
нему дисульфидные мостики. При взаимодействии с электроном они сначала
превращаются в анион-радикалы, а затем происходит их разрыв с образованием
радикала цистеина:
R-CH2-S-S-CH2-R1 + e-
→ (R-CH2-S·-S-CH2-R1)-
→ R-CH2-S- + ·S-CH2-R1
В присутствии кислорода радикалы цистеина могут
давать цистеинсульфоновую кислоту:
R-CH2-S·-
+ O2 → R-CH2-SO-OH
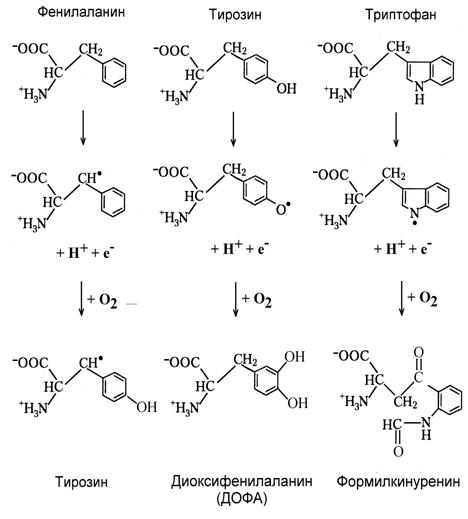
Рис.6. Схема фотопревращений ароматических
аминокислот под действием ультрафиолетового света в присутствие кислорода
Процессы ультрафиолетовой инактивации белков, конечно, сложнее, чем фотопревращения отдельных аминокислот. За первичными фотохимическими процессами следуют темновые реакции, приводящие к изменению конформации, нарушению структуры активного центра и инактивации (Рис.7). Фотоинактивация белков происходит необратимо по одноквантовому механизму с квантовым выходом j порядка 10-3-10-2 (для разных белков). Скорость инактивации линейно зависит от интенсивности света, т.е. подчиняется правилу взаимозаменяемости Бундзена-Роско (I1t1=I2t2). Квантовый выход фотоинактивации белков обычно не зависит от присутствия кислорода О2, т.е. она не связана с процессами окисления.
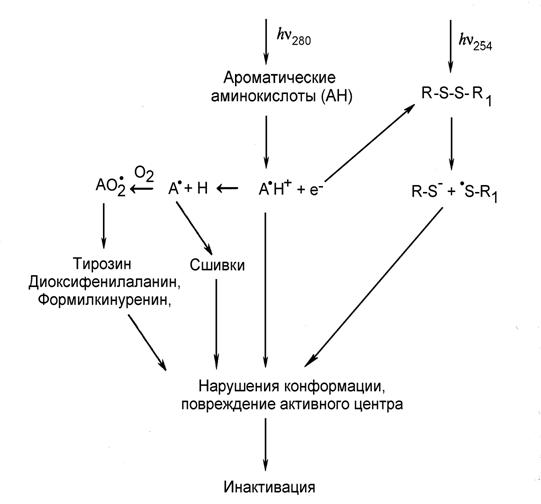
Рис.7. Схема ультрафиолетовой инактивации белков
Спектр действия фотоинактивации белков содержит полосы 250 и 280 нм, свидетельствующие об участии дисульфидных мостиков (цистина) и ароматических аминокислот, особенно триптофана, в этом процессе. При коротковолновом облучении (220-260 нм) преобладает цистиновая инактивация, а при действии более длинных волн (УФБ) - триптофановая. Характер фотоинактивации белка в случае первичного повреждения цистина или триптофана различается. Поэтому говорят о цистиновой или триптофановой инактивации белков. Если поврежденная аминокислота, например, триптофан, входит в состав активного центра белка, то белок теряет активность либо вследствие модификации этой аминокислоты, либо благодаря потере конформационной подвижности. К потере конформационной подвижности и последующей инактивации могут приводить сшивки не только в активном центре, но и в удаленных местах.
Миграция энергии возбуждения в белках может
разобщать в пространстве место поглощения кванта и место повреждения молекулы.
Это увеличивает поперечное сечение фотохимической реакции. В белках возможен
индуктивно-резонансный механизм миграции энергии, т.к. поглощающие и
флуоресцирующие аминокислотные остатки - триптофан, тирозин и фенилаланин -
сближены в белковой глобуле. Направление миграции энергии:
Фен ® Тир ®
Три ®
ионизированный Тир.
Некоторые металлосодержащие белки могут инактивироваться вследствие фотоиндуцированной потери металлического атома.
4. Влияние ультрафиолетового излучения на
биомембраны
Наиболее фоточувствительными молекулами из элементов биомембран являются ненасыщенные жирнокислотные цепи фосфолипидов, содержащие двойные связи, главным образом, остатки олеиновой, Они могут спонтанно окисляться кислородом, но ультрафиолетовое излучение значительно ускоряет этот процесс, инициируя появление свободных радикалов и цепное перекисное окисление липидов. Сами жирные кислоты практически не поглощают свет с длиной волны более 220-230 нм, и он вызывает превращения липидов не прямо, а косвенно. В этом случае ультрафиолетовое излучение сперва поглощается каким-нибудь другим хромофором, который под действием ультрафиолета превращается в свободный радикал, способный инициировать цепное перекисное окисление мембранных липидов. В качестве такого первичного хромофора могут выступать как нелипидные хромофорные группы (порфирины, флавины, триптофан, тирозин или -S-S-мостики в белках), так и собственные продукты окисления липидов, прежде всего гидроперекиси (ROOH). В результате окисления ненасыщенных кислот могут образовываться сопряженные системы двойных связей: диеновые: -СН=СН-СН=СН- (lm »233 нм), триеновые: -СН=СН-СН=СН-СН=СН- (lm »260-280 нм) и др. Чем длиннее цепочка сопряженных связей, тем дальше в красную область смещен спектр поглощения света.
Процессы перекисного окисления липидов (ПОЛ) могут начинаться спонтанно, независимо от облучения. Инициаторами ПОЛ служат свободные радикалы воды или биомолекул, небольшое количество которых всегда образуется в тканях в результате фоновой радиации или некоторых биохимических реакций. Например, при нарушении электронного транспорта в митохондриях электроны могут переноситься не на цитохромы, а прямо на кислород с образованием весьма активного супероксид-аниона О2·¾.
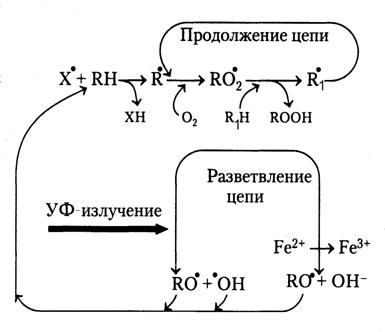
Рис.8. Схема процессов, протекающих при цепном
перекисном окислении липидов
При взаимодействии первичного радикала Х· с молекулой RH приводит к переносу на нее радикального состояния: R· (Рис.8). Его окисление кислородом рождает перекисный радикал ROO·, который, взаимодействуя с другой липидной молекулой R1H, продолжает цепочку, рождая новый радикал R·1, а сам превращается в гидроперекись ROOH. Таким образом, в результате ПОЛ первичная энергия одного радикала приводит к появлению многих новых радикалов и новых молекул перекисей липидов ROOH. Окисление происходит по месту двойных связей в жирных кислотах.
Ультрафиолетовое излучение или двухвалентные ионы железа Fe2+ вызывают разветвление цепи, при котором генерируются два радикальных продукта, способных инициировать появление двух новых цепочек, что резко ускоряет процесс. Цепь ПОЛ может обрываться в результате (а) рекомбинации радикалов или (б) с помощью антиоксидантов, радикалы которых неактивны и не способны продолжать рождение новых радикалов. О цепном характере ультрафиолетового повреждения биомембран свидетельствует аномально высокие квантовые выходы, достигающие 10-100.
Кроме нарушений липидной фазы, ультрафиолетовое излучение вызывает инактивацию мембранных белков в результате разрыва дисульфидных мостиков и фотолиза ароматических аминокислот: триптофана, тирозина и фенилаланина. Также возможна фотодеструкция других важных биомолекул, присутствующих в липидной фазе мембраны или в составе мембранных белков: флавинов, пиридиннуклеотидов, порфиринов, коферментов А, Q и других. Фотоинактивация белков и нуклеиновых кислот, в отличие от фотоокисления липидов, почти не зависит от наличия кислорода.
5. Действие ультрафиолетового излучения на клетки
Главным результатом действия УФ-индуцированного перекисного окисления мембранных липидов является значительное увеличение ионной проницаемости мембран, снижение электрического сопротивления, нарушение барьерных функций, падению трансмембранных ионных градиентов. Эти эффекты являются наиболее ранним проявлением фотоповреждения мембраны. Одновременное повреждение мембранных белков - ионных каналов, транспортных АТФаз, переносчиков различных веществ, рецепторов и адгезионных белков лежит в основе фотоиндуцированных нарушений основных клеточных функций, включая поддержание гомеостаза, межклеточные взаимодействия и т.д. Как следствие, нарушается метаболизм, ингибируются синтезы важных биомолекул, нарушаются функциональные процессы, и развивается смерть.
Например, в облученных ультрафиолетом нервных клетках особенно важную роль играет фотоповреждение Na+,K+-АТФазы и ионных каналов. Так, по данным J.M. Fox, полученным в 1970-х годах, ультрафиолетовое излучение с «белковым» максимумом 280 нм намного сильней повреждает Na+-, чем К+-каналы. Это приводит к уменьшению амплитуды потенциалов действия. Такое облучение также инактивирует Na+,K+-АТФазу необходимую для поддержания градиента ионов Na+ и K+. Сопутствующая деполяризация приводит к учащению потенциалов действия в возбудимых нервных и мышечных клетках, за которым следует так называемый деполяризационный блок, т.е. потеря способности генерировать потенциалы действия.
Ультрафиолетовое излучение с длиной волны 260 нм действовало на нервное волокно иначе: оно не столько меняло мембранный потенциал, сколько повышало порог генерации нервных импульсов и, как следствие, снижало их частоту. Этот эффект мог быть связан с повышением внутриклеточной концентрации ионов Ca2+, от которой зависит порог. Более длинноволновое излучение с максимумами при 313 или 405 нм возбуждало нейронную активность без признаков существенного повреждения. Эти длины волн соответствуют поглощению света цитохромами. Поэтому их воздействие можно связать с влиянием на митохондрии, запасающие Са2+.
Дозы ультрафиолетового излучения, нарушающие
ионную проницаемость биомембран имеют такой же порядок, как и дозы,
инактивирующие нуклеиновые кислоты, и значительно ниже доз, повреждающих белки.
Это указывает на присутствие в клетках двух основных мишеней для повреждающего
действия ультрафиолетового излучения: нуклеиновые кислоты и биомембраны
(цитоплазматическая мембрана и мембраны внутриклеточных органелл).
.2 Митохондрии
При действии ультрафиолета на митохондрии перекисное окисление липидов приводит к неспецифическому увеличению протонной проницаемости митохондриальных мембран, снижению трансмембранного градиента ионов Н+ и разобщению окислительного фосфорилирования. В результате митохондрии теряют способность синтезировать АТФ, что негативно сказывается на различных сторонах жизнедеятельности клеток. На ультраструктурном уровне видно, что митохондрии первыми реагируют на ультрафиолетовое повреждение. Даже небольшие дозы ультрафиолета вызывает их набухание, утрату крист, просветление матрикса.
Вследствие нарушения электронного транспорта по дыхательной цепи в митохондриях происходит непосредственный перенос электронов вместо цитохромов на кислород с образованием супероксид-аниона О·2─ и других активных форм кислорода, названных митохондриальными АФК. Это усиливает повреждение митохондрий. Появление в клетке большого количества свободных радикалов и активных форм кислорода индуцирует комплекс реакций, называемых окислительным стрессом, которые ведут к клеточной смерти. Ультрафиолетовое воздействие на митохондрии является эффективным индуктором одного из основных типов смерти клеток - апоптоза, а также может стимулировать неконтролируемое деление клеток - рак.
Еще одно следствие фотоповреждения митохондрий - высвобождение ионов кальция, запасаемых этими органеллами и высвобождаемых при их повреждении. Появляющиеся в цитозоле ионы кальция могут активировать ферменты - протеиназы, нуклеазы, фосфолипазы - участвующие в процессах некроза и апоптоза.
И наконец, митохондрии при повреждении в
митохондриях открываются специальные высокопроницаемые поры (PTP), через
которые из мембранного пространства выходит цитохром с. Он является индуктором
апоптоза. В комплексе с цитоплазматическим белком Apaf-1,
он активирует протеолитический каспазный каскад, ведущий к смерти клетки:
каспаза 9 ® каспаза 3 ® каспаза 6 и 7 ®
протеиназы, нуклеазы, фосфолипазы ® разрушение белков,
расщепление ДНК- апоптоз.