Материал: Д6901 Митропов ВВ Расчет и сопостановление основных термодин процессов
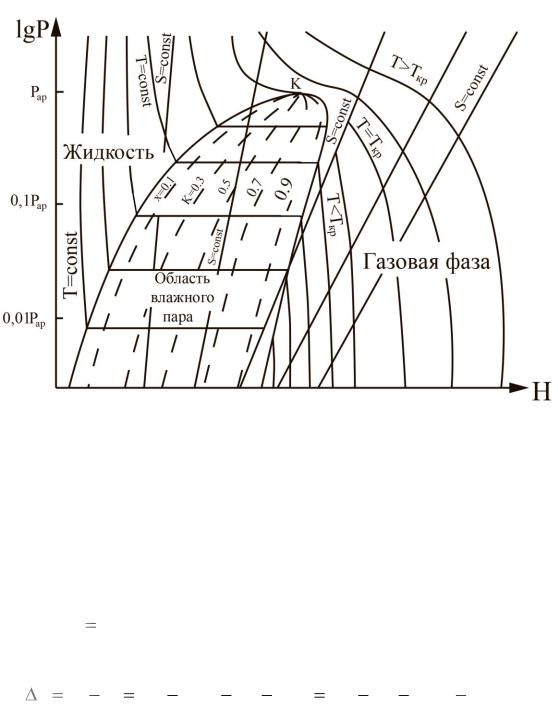
Одно из основных преимуществ диаграммы lg p-h перед тепловой состоит в том, что теплота подогрева жидкости, парообразования, перегрева пара изображается в ней не площадями, а отрезками. Представление разности энтальпий в виде отрезков весьма удобно для расчета и анализа циклов различных машин. Пример диаграммы показан на рис. 9.
Рис. 9. Диаграмма lg p–h
ПРОЦЕССЫ РЕАЛЬНОГО ГАЗА
Изохорный процесс
Процесс, происходящий без изменения объема, называется изохорным ( v const ).
Изменение внутренней энергии
u u2 u1 h2 p2v h1 p1v h2 h1 v p2 p1 .
21
Внешняя работа газа
2
l pdv 0 .
1
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
q |
u l или q |
u . |
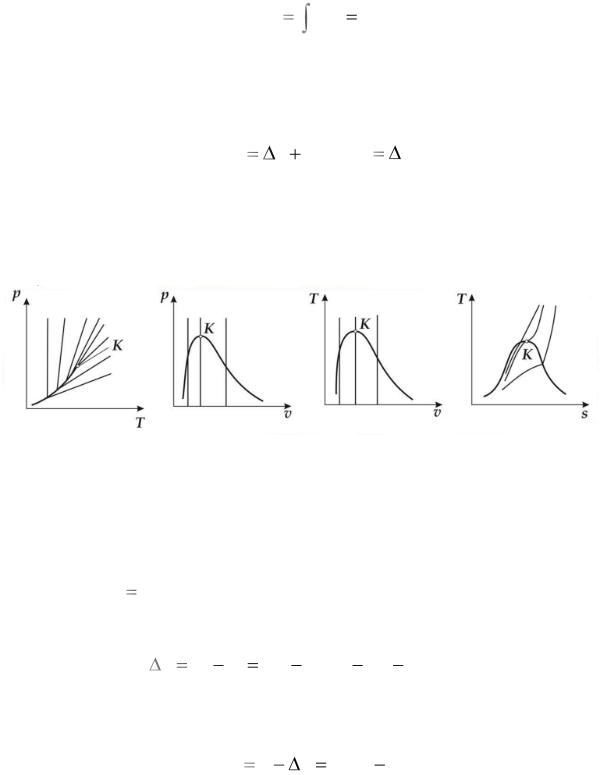
Изображение процесса в координатах p–T, p–v, T–v и T–s
(рис. 10).
Рис. 10. Изохорный процесс
Изобарный процесс
Процесс, происходящий при постоянном давлении, называется изобарным ( p const ).
Изменение внутренней энергии
u u2 u1 |
h2 |
p2v2 |
h1 p1v1 . |
Внешняя работа газа |
|
|
|
l |
q |
u p v2 |
v1 . |
22
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
q h2 h1 .
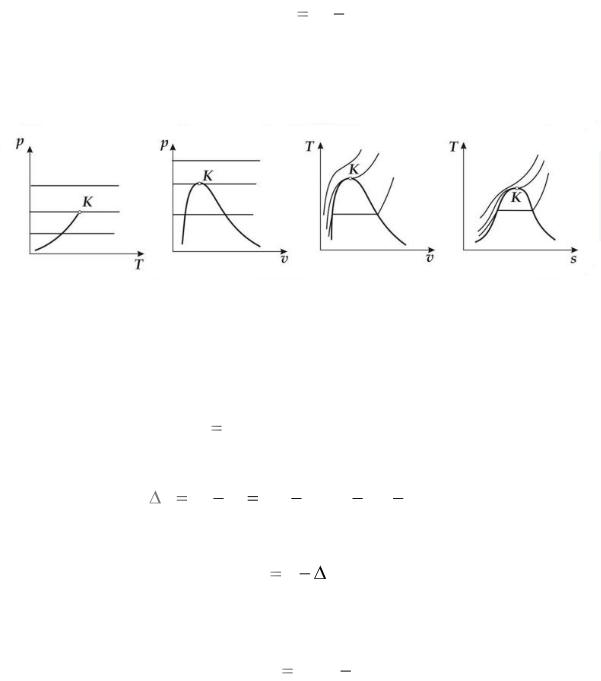
Изображение процесса в координатах p–T, p–v, T–v и T–s
(рис. 11).
Рис. 11. Изобарный процесс
Изотермический процесс
Процесс, происходящий при постоянной температуре, называется изотермическим ( t const ).
Изменение внутренней энергии
u u2 u1 h2 p2v2 |
h1 p1v1 . |
Внешняя работа газа
l q u .
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
q T s2 s1 .
Изображение процесса в координатах p–T, p–v, T–v и T–s
(рис. 12).
23

Рис. 12. Изотермический процесс
Адиабатный процесс
Процесс, происходящий без теплообмена между газом и окру-
жающей средой, называется адиабатным ( dq |
0, s const ). |
|||
Изменение внутренней энергии |
|
|
||
u u2 u1 |
h2 |
p2v2 |
h1 |
p1v1 . |
Внешняя работа газа |
|
|
|
|
l |
q |
u |
u . |
|
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
q 0 .
Изображение процесса в координатах p–T, p–v, T–v и T–s
(рис. 13).
Рис. 13. Адиабатный процесс
24
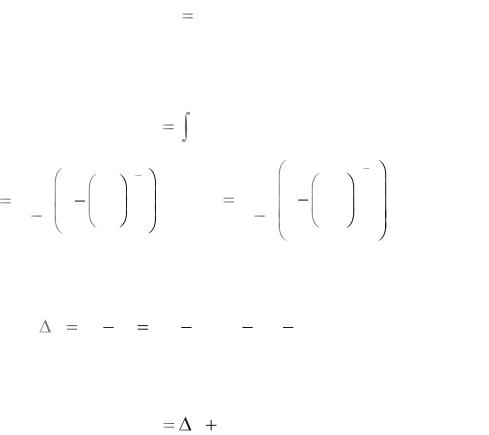
Политропный процесс
Реальные процессы сжатия в газовых двигателях и компрессорах часто не являются ни адиабатными, ни изотермическими, а занимают промежуточное положение между этими двумя видами процессов. Поэтому обычно встречаемые на практике значения показателя n политропного процесса лежат в интервале от 1 до k.
Для любых точек на политропе можно записать уравнение в виде
p1v1n p2v2n .
Внешняя работа газа
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
l |
pdv ; |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
n 1 |
|
|
|
|
|
n 1 |
|
|
p1v1 1 |
|
|
p1v1 1 |
p2 |
|
|
|
|||
l |
|
или l |
. |
||||||||
v1 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
n |
|
|
n 1 |
v2 |
|
n 1 |
p1 |
|
|
|
|||
Изменение внутренней энергии
u u2 u1 h2 p2v2 |
h1 p1v1 . |
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
q u l .
Термодинамические процессы для реальных газов рассчитывают с помощью таблиц или диаграмм рабочих веществ.
25