Материал: Д6901 Митропов ВВ Расчет и сопостановление основных термодин процессов
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
q |
u l |
u 0 , q l . |
Все подведенное тепло превращается в работу
|
q |
l |
T s2 |
|
s1 . |
|
|
|
|
||||
Теплоемкость процесса: |
c |
|
dq |
, |
dT |
0, c |
. |
||||||
|
dT |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
Изменение энтропии в процессе: |
|
|
|
|
|
||||||||
|
|
|
2 |
dq |
1 |
2 |
|
q |
|
|
|||
s s |
2 |
s |
|
|
|
|
|
|
dq |
|
|
; |
|
|
|
|
|
|
|
|
|
|
|||||
|
1 |
|
T |
|
T 1 |
T |
|
|
|||||
|
|
|
1 |
|
|
|
|||||||
s s s R ln |
v2 |
R ln |
p1 |
. |
|
|
|
||||
2 |
1 |
v1 |
|
p2 |
|
|
|
|
|||
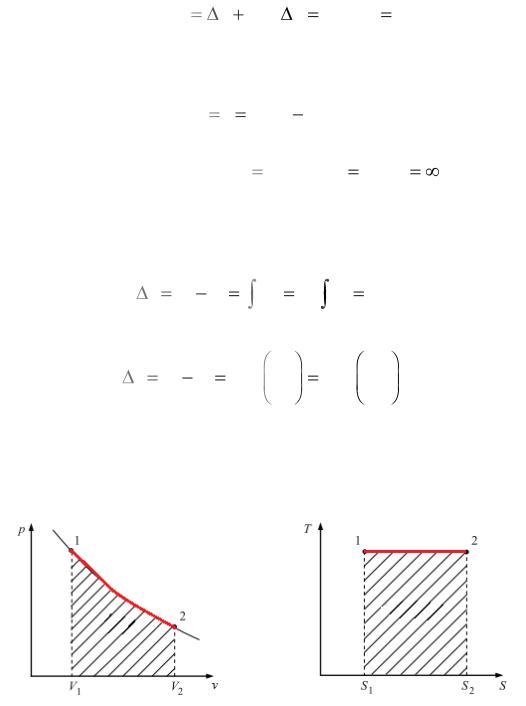
Изображение процесса в рабочей (а) и тепловой (б) диаграммах (рис. 3).
а |
б |
Рис. 3. Изотермический процесс
11
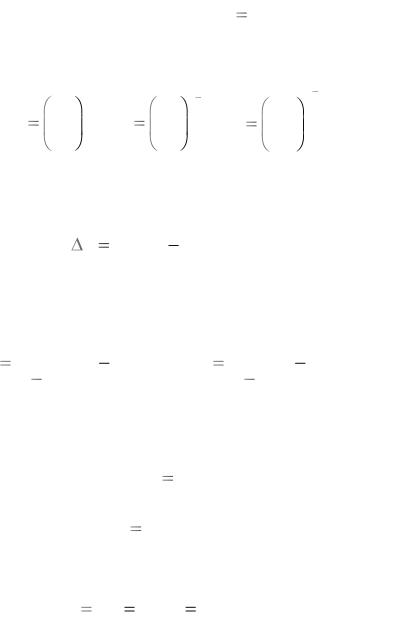
Адиабатный процесс
Процесс, происходящий без теплообмена между газом и окру-
жающей средой, называется адиабатным ( pvk |
const ). |
|
|
|||||||||||||||
Уравнения процесса: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
k |
|
|
|
|
k 1 |
|
|
|
|
|
k |
1 |
|
|
p1 |
|
v2 |
|
T1 |
|
v2 |
|
T1 |
|
p1 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
k |
|
|
|
|
|
|
|
|
; |
|
|
|
|
; |
|
|
|
|
|
. |
|
|
p2 |
|
v1 |
|
T2 |
|
v1 |
|
T2 |
|
p2 |
|||||||
Изменение внутренней энергии
u cvm T2 T1 .
Внешняя работа газа
l |
1 |
|
p1v1 |
p2v2 |
или l |
|
R |
|
T1 |
T2 . |
|
|
|
|
|
||||||
k 1 |
k |
|
|
|||||||
|
|
|
|
|
1 |
|
||||
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
|
|
|
dq |
0. |
|
Теплоемкость процесса: c |
0. |
|
|||
Изменение энтропии в процессе |
|
||||
ds |
dq |
0, |
s const. |
||
|
|
||||
T |
|||||
|
|
|
|||
Изображение процесса в рабочей (а) и тепловой (б) диаграммах (рис. 4).
12
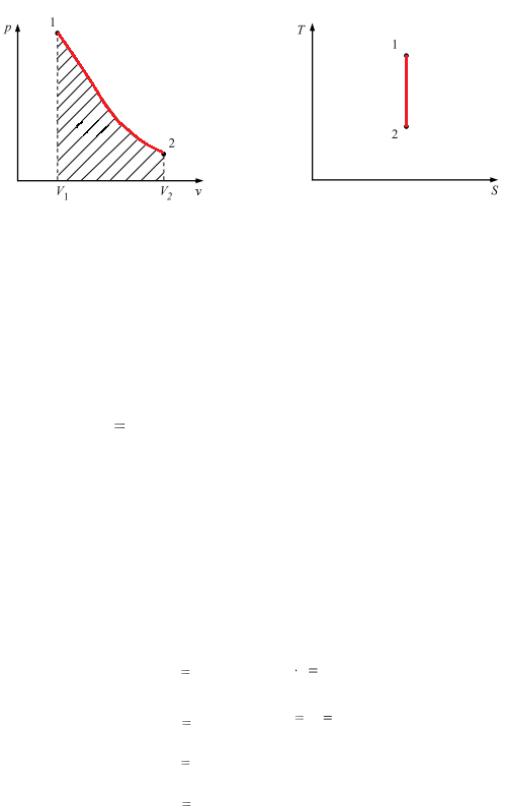
а |
б |
Рис. 4. Адиабатный процесс
Политропный процесс
Политропным называется всякий термодинамический процесс, в котором превращение энергии осуществляется согласно определен-
ному закону ( pvn const ).
Все рассмотренные ранее процессы являются частными случаями политропного.
При некоторых определенных значениях n получаем известные нам процессы (табл. 1).
|
|
|
|
|
|
|
Таблица 1 |
|
|
|
|
|
|
|
|
|
|
Показатель |
|
|
|
Уравнение процесса |
Название процесса |
|
||
политропы |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n = 0 |
pv0 |
const |
p 1 |
const |
Изобарный |
|
||
|
|
|
|
|
|
|
|
|
n = ∞ |
1 |
|
|
p0v 1v |
const |
Изохорный |
|
|
|
|
|
|
|
||||
pn v |
const |
|
||||||
|
|
|
|
|
|
|
||
n = 1 |
pv1 |
const |
|
|
Изотермический |
|
||
|
|
|
|
|
|
|
||
n = k |
pvk |
const |
|
|
Адиабатный |
|
||
|
|
|
|
|
|
|
|
|
13
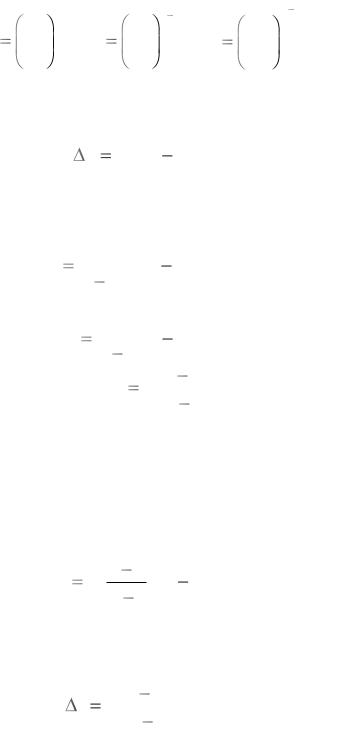
Уравнения процесса:
|
|
|
n |
|
|
|
|
n 1 |
|
|
|
|
|
n 1 |
|
p1 |
|
v2 |
|
T1 |
|
v2 |
|
T1 |
|
p1 |
|
|
|
||
|
|
|
|
|
|
n |
|||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
; |
|
|
|
|
; |
|
|
|
. |
||
p2 |
|
v1 |
|
T2 |
|
v1 |
|
T2 |
|
p2 |
|||||
Изменение внутренней энергии
u cv T2 T1 .
Внешняя работа газа
l |
1 |
|
|
p1v1 |
|
p2v2 ; |
||||
|
|
|
|
|
|
|||||
|
n |
1 |
|
|||||||
|
|
|
|
|
|
|
||||
|
l |
|
R |
|
T1 |
|
T2 . |
|||
|
|
|
|
|
|
|||||
|
n |
|
|
|||||||
|
|
|
1 |
|
|
|
||||
Теплоемкость процесса: |
c |
|
c |
n |
k |
. |
||||
|
|
|
||||||||
|
|
|
|
|
|
|
v |
n |
1 |
|
Теплоемкость может принимать отрицательные значения, ес-
ли 1 < n < k (c < 0).
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
n k
q cv n 1 T2 T1 .
Изменение энтропии в процессе
s c |
n |
k |
ln |
T2 |
. |
|
|
|
|||
v |
n |
1 T |
|||
|
|
1 |
|
||
Изображение процесса в рабочей (а) и тепловой (б) диаграммах (рис. 5).
14
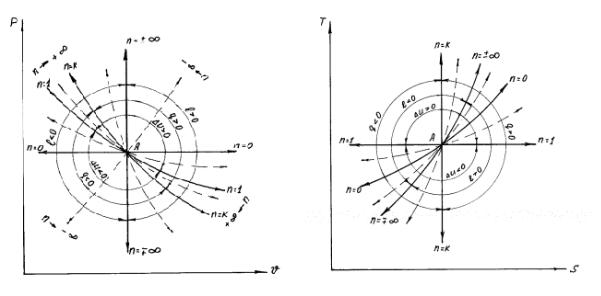
а |
б |
Рис. 5. Изображение политропных процессов
15