Материал: Д6901 Митропов ВВ Расчет и сопостановление основных термодин процессов
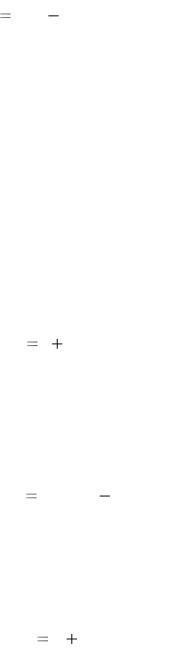
где pизб – избыточное (или манометрическое) давление; pвак – показание вакуумметра (вакуум или разрежение); pбар – атмосферное (или барометрическое) давление.
Соотношение между различными единицами давления:
1 Па = 10 –5 бар = 7,502∙10 –3 мм рт.ст. = 0,102 мм вод.ст.
При измерении давления ртутными приборами их показания необходимо приводить к 0 оС:
p0 p 1 0, 000172t ,
где p0 – показание прибора, приведенное, к 0 оС, мм рт.ст.; p – действительная высота ртутного столба при температуре воздуха t, оС; 0,000172 – коэффициент объемного расширения ртути.
Температура (t, T) – это мера нагретости тела. Температуру можно рассматривать как параметр, одинаковый у частей термодинамической системы, находящихся в состоянии термического равновесия. По действующему стандарту приняты две температурные шкалы – термодинамическая и международная температурная шкала. Отсчеты по каждой из этих шкал можно выразить либо в кельвинах (T, [K]), либо в градусах Цельсия (t, [оС]). Соотношение между температурами, выраженными в кельвинах и градусах Цельсия, имеет вид
Tt 273,15.
Внекоторых странах для измерения температуры применяют шкалу Фаренгейта. Для перевода показаний этой шкалы в градусы Цельсия и обратно служит соотношение
t oC |
5 |
t o F 32 . |
|
9 |
|||
|
|
Энтальпия. В термодинамике во многих случаях применяется не внутренняя энергия, а другой параметр – энтальпия, которая представляет собой
h u pv ,
6

где pv – потенциальная энергия давления, представляет собой работу, которую надо затратить, чтобы ввести рассматриваемое тело с объемом v в среду, имеющую давление p.
Каждая величина, входящая в выражение энтальпии, – параметр состояния, значит, энтальпия – параметр состояния и dh – полный дифференциал. (Полным называется дифференциал, интеграл которого не зависит от пути интегрирования, а определяется только начальным и конечным пределами интегрирования.):
2 2
dh cp dt ;
1 1
h cpm t2 t1 .
Принято считать h = 0 при t = 0 (или T = 0), тогда
h cp |
t0 t . |
Из сказанного вытекает и другое определение энтальпии. Энтальпия – это количество тепла, которое нужно подвести к
телу в изобарном процессе, чтобы перевести его из начального состояния в данное.
Энтропия так же, как и энтальпия, является параметром со-
стояния. |
|
|
|
|
|
|
|
||
Из I закона dq |
cv dT |
pdv . |
|
|
|||||
Поделим обе части на T: |
|
|
|||||||
|
|
|
dq |
|
cv |
dT |
p |
dv . |
|
|
|
|
|
|
|
||||
|
|
|
T |
|
T |
T |
|||
Обозначим |
dq |
ds , |
где под s подразумеваем параметр со- |
||||||
T |
|||||||||
|
|
|
|
|
|
|
|
||
стояния – энтропию.
Энтропия есть мера необратимости протекания термодинамических процессов.
7

ПРОЦЕССЫ ИДЕАЛЬНОГО ГАЗА
Изохорный процесс
Процесс, происходящий без изменения объема, называется изохорным ( v const ).
Уравнение процесса |
|
|
|
|
|
p1 |
|
T1 |
. |
|
|
|
||
|
p2 |
|
T2 |
|
Изменение внутренней энергии
u u2 u1 cvm T2 T1 .
Внешняя работа газа
dl 0, l 0 .
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе:
q u cvm T2 T1
Теплоемкость процесса: c cv . Изменение энтропии в процессе
2 |
dq |
2 |
c dT |
|
T |
|
s s2 s1 |
|
|
v |
cvm ln |
2 |
. |
T |
|
T |
T1 |
|||
1 |
1 |
|
|
Изображение процесса в рабочей (а) и тепловой (б) диаграммах (рис. 1).
8
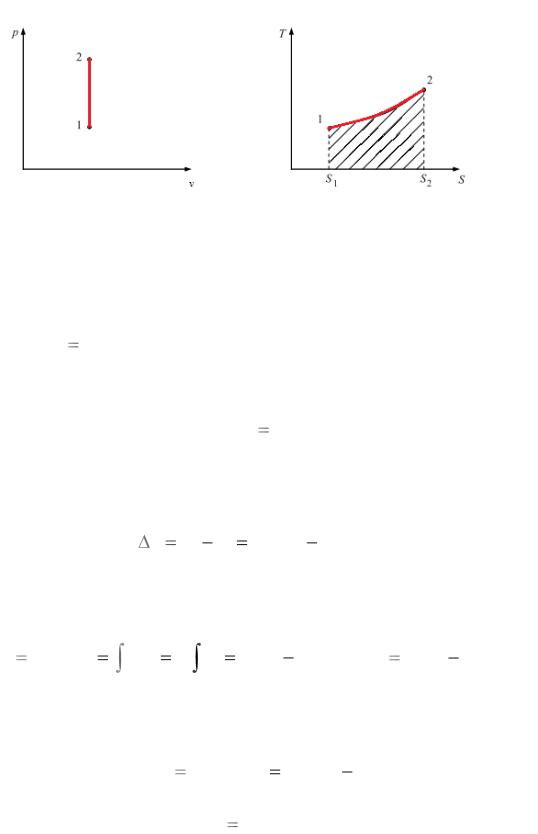
а |
б |
Рис. 1. Изохорный процесс
Изобарный процесс
Процесс, происходящий при постоянном давлении, называется изобарным ( p const ).
Уравнение процесса
v1 |
|
T1 |
. |
|
|
||
v2 |
|
T2 |
|
Изменение внутренней энергии
u u2 u1 cvm T2 T1 .
Внешняя работа газа
2 |
2 |
dl pdv, l |
pdv p dv p v2 v1 или l R T2 T1 . |
1 |
1 |
Количество теплоты, сообщаемое газу или отнимаемое в про-
цессе,
dq cp dT , q cpm T2 T1 .
Теплоемкость процесса: c cp . Изменение энтропии в процессе
9
|
2 |
dq |
2 |
cp dT |
|
|
|
T |
|
s s |
s |
|
|
|
c |
|
ln |
2 |
. |
|
|
|
pm |
|
|||||
2 |
1 |
T |
|
T |
|
|
T1 |
||
|
1 |
1 |
|
|
|
||||
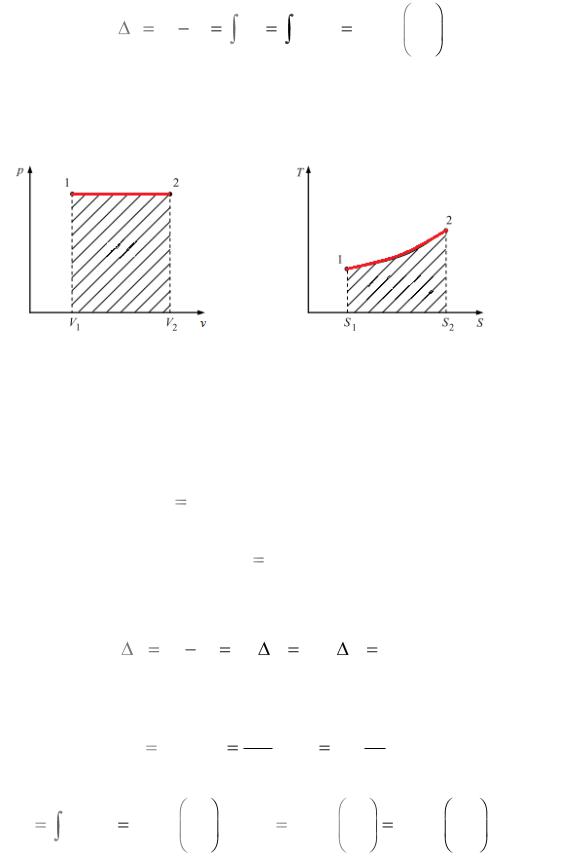
Изображение процесса в рабочей (а) и тепловой (б) диаграммах (рис. 2).
а |
б |
Рис. 2. Изобарный процесс
Изотермический процесс
Процесс, происходящий при постоянной температуре, называется изотермическим (T const ).
Уравнение процесса
p1 |
|
v2 |
. |
|
|
||
p2 |
|
v1 |
|
Изменение внутренней энергии
u u2 u1 cvm T 0, T 0 .
Внешняя работа газа
dl pdv, l RTv , dl RT dvv ,
2
l
1
RT |
dv |
RT ln |
v2 |
или l |
RT ln |
v2 |
RT ln |
p1 |
. |
|
|
|
|
||||||
|
v |
|
v1 |
|
|
v1 |
|
p2 |
|
10