Материал: Болезни, связанные с нарушением фолдинга белка
В результате в их пространственной структуре происходят конформационные перестройки, характерные для прионовых белков.
Известны случаи наследственных форм прионовых болезней, вызванных мутациями в структуре данного белка. Однако возможно и заражение человека прионовыми белками, в результате чего возникает заболевание, приводящее к гибели больного. Так, куру - прионовая болезнь аборигенов Новой Гвинеи, эпидемический характер которой связан с традиционным каннибализмом в этих племенах и передачей инфекционного белка от одной особи к другой. В связи с изменением образа их жизни данное заболевание практически исчезло.
В настоящее время интерес к прионовым болезням возрос в связи с заражением людей прионами при употреблении мясопродуктов, полученных от животных, являющихся носителями прионов, вызывающих «бешенство коров» (болезнь Кройтц-фельдта-Якоба). Несмотря на то, что прионовые белки человека и животных различаются лишь незначительно, долгое время полагали, что существуют межвидовые барьеры на пути передачи болезни. Однако последние данные показали, что эти барьеры не абсолютны, и что существует принципиальная возможность передачи болезни от одного вида другому. Так, в Великобритании к середине1999 г. было зарегистрировано около 40 случаев данного заболевания. Прогноз не исключает развития эпидемии прионовой болезни в ближайшие 10-15 лет.
2.3 Преэклампсия
Преэклампсия - патология беременности, лидирующая среди причин материнской и детской смертности в мире - имеет характеристики, позволяющие отнести этот синдром к заболеваниям, связанным с аномальной структурой белков, таким, как болезнь Альцгеймера или прионные болезни. Сделанное международной группой исследователей открытие, результаты которого опубликованы <#"823707.files/image005.gif">
Рис. 5. Предшественник бета-амилоида
В то же время белок IFI6-16, играющий ключевую роль в регуляции апоптоза (программируемой клеточной гибели), чья аномальная версия также оказалась вовлечена в развитие преэклампсии, ранее не был ассоциирован с болезнями, связанными с нарушением фолдинга белков.
Далее группа Бухимши продолжила исследования в этом направлении, собрав образцы мочи более 600 беременных женщин и проанализировав их с помощью гистологического красителя конго красный (конгорот), применяемого для обнаружения скоплений амилоидных белков. Моча здоровых женщин при соединении с красителем не меняет цвет, а моча, в которой присутствуют белковые клубки, окрашивается красным с разной, в зависимости от выраженности патологии, интенсивностью. В итоге было установлено, что такой метод позволяет с более чем 80-процентной точностью, еще до появления клинических симптомов, диагностировать преэклампсию и даже предсказать тяжесть ее течения и необходимость срочного родоразрешения.
На основании сделанного группой Бухимши открытия уже создан пилотный образец бумажного теста на раннюю диагностику преэклампсии по анализу мочи, проходящий в настоящее время клинические испытания в различных медицинских центрах мира. «Это прекрасная возможность действительно помочь женщинам с помощью простого, дешевого, неинвазивного и очень точного теста», - отметила <#"823707.files/image006.gif">
Рис. 6. Дофамин
Эти
нейроны служат основным компонентом базальных ганглиев, сложных структур в
глубине головного мозга, отвечающих за координацию и тонкую регуляцию движений.
В самом начале заболевания, когда число утраченных дофаминергических нейронов
невелико, мозг работает нормально, но с выходом из строя более половины
специализированных клеток их нехватку организм уже не может компенсировать.
Структуры мозга, отвечающие за движения (таламус, базальные ганглии и кора
головного мозга), перестают работать как единая система, и тогда наступает
ситуация, аналогичная той, что наблюдается в крупном аэропорту при выходе из
строя системы контроля полетов: опоздания, задержки, нестыковки и, наконец,
полный хаос. Больше всего страдают клетки черной субстанции (составная часть
экстрапирамидной системы
<https://ru.wikipedia.org/wiki/%D0%AD%D0%BA%D1%81%D1%82%D1%80%D0%B0%D0%BF%D0%B8%D1%80%D0%B0%D0%BC%D0%B8%D0%B4%D0%BD%D0%B0%D1%8F_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0>,
находящаяся в области четверохолмия среднего мозга
<https://ru.wikipedia.org/wiki/%D0%A1%D1%80%D0%B5%D0%B4%D0%BD%D0%B8%D0%B9_%D0%BC%D0%BE%D0%B7%D0%B3>.
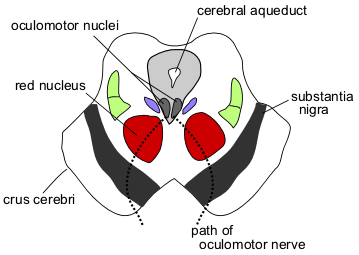
Рис.
7. Мозг. Черная субстанция
Играет
важную роль в регуляции моторной функции, тонуса мышц, осуществлении
статокинетической функции участием во многих вегетативных функциях: дыхании
<https://ru.wikipedia.org/wiki/%D0%94%D1%8B%D1%85%D0%B0%D0%BD%D0%B8%D0%B5>,
сердечной деятельности
<https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%B4%D1%86%D0%B5>,
тонусе кровеносных сосудов
<https://ru.wikipedia.org/wiki/%D0%9C%D1%8B%D1%88%D0%B5%D1%87%D0%BD%D0%BE%D0%B5_%D1%81%D0%BE%D0%BA%D1%80%D0%B0%D1%89%D0%B5%D0%BD%D0%B8%D0%B5>.),
которые контролируют произвольные движения и настроение. Вначале последствия
гибели нейронов в этой области компенсируют другие нейроны, но когда доля
утраченных клеток достигает 50-80%, незатронутые области головного мозга не
справляются с перегрузкой. С этого момента части головного мозга, тоже
вовлеченные в регуляцию двигательной активности, в том числе остальная часть
базального ганглия, таламус и кора головного мозга, перестают работать
согласованно, и движения становятся неконтролируемыми.
.4.1 «Плохие белки»
У многих больных, умерших от паркинсонизма, при вскрытии в черной субстанции обнаруживаются белковые скопления (они называются тельцами Леви по фамилии немецкого патологоанатома, открывшего их в 1912 г.). Аналогичные образования характерны также для болезни Альцгеймера. Являются ли эти кластеры причиной деструктивных изменений или, напротив, выполняют защитные функции, удерживая аномальные, токсичные для нейрона белки от распространения по всей клетке, - не совсем ясно. В любом случае большинство ученых сходятся на том, что выяснение причины кластеризации белков поможет раскрыть тайну болезни Паркинсона.
Рис.
8. Патология чёрной субстанции с потерей клеток, видны Тельца Леви
<https://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D0%BB%D1%8C%D1%86%D0%B0_%D0%9B%D0%B5%D0%B2%D0%B8>.
Если
по тем или иным причинам шаперонная система (Помогает по завершении синтеза
белковой молекулы, сворачивается ей в компактную трехмерную глобулу. Эти же
молекулы вновь упаковывают белки, утратившие должную конфигурацию.) выходит из
строя, то неправильным образом уложенные белки становятся мишенью для так
называемой убиквитин-протеасомной системы. Сначала к белковой молекуле с
аномальной конформацией присоединяется небольшой белок убиквитин (небольшой
консервативный белок
<https://ru.wikipedia.org/wiki/%D0%91%D0%B5%D0%BB%D0%BA%D0%B8>, который у
эукариот
<https://ru.wikipedia.org/wiki/%D0%AD%D1%83%D0%BA%D0%B0%D1%80%D0%B8%D0%BE%D1%82%D1%8B>
присоединяется к белкам.). Вслед за первой убиквитиновой «бусиной»
присоединяется вторая - и так до тех пор, пока на конце обреченной на гибель
белковой молекулы не образуется цепочка (своеобразная «черная метка»). Она
служит сигналом для протеасомы («мусорщика» нервной клетки) к расщеплению
аномального белка на составляющие его аминокислоты.
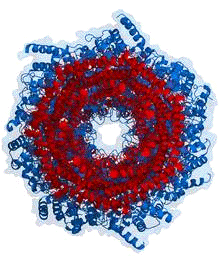
Рис.
8. Протеасома. Вид сверху.
Стало
более или менее ясно, что болезнь Паркинсона развивается в результате нарушений
в работе шаперонной и убиквитин-протеасомной систем. По-видимому, дело обстоит
следующим образом. Какое-то повреждение в нейронах черной субстанции запускает
целый каскад реакций, приводящих к появлению большого количества неправильно
упакованных белков. Они образуют кластеры, что вначале даже дает некоторые
преимущества клетке, поскольку аномальные белки держатся вместе, а не
распространяются по ней, вызывая повреждения. Затем в дело вступают шапероны,
приводящие белки в норму, а те из них, которые исправить не удается,
расщепляются убиквитин-протеасомной системой. Когда аномальных белков
становится слишком много, клеточная «очистительная машина» перестает справляться
с работой, шаперонов не хватает, токсичные белки накапливаются, и в конце
концов нейроны погибают. Эта гипотеза хороша тем, что, по мнению ученых,
объясняет природу обеих форм болезни Паркинсона. Предполагается, что 95%
больных страдают вторичным паркинсонизмом, возникающим в результате сложных
взаимодействий между генетическими и средовыми факторами. Если человек с
предрасположенностью к паркинсонизму попадает в неблагоприятные условия
(например, длительное время находится в контакте с пестицидами), то нейроны
черной субстанции страдают у него в большей степени, чем нейроны людей, не
имеющих предрасположенности, и в них накапливается больше белков с аномальной
конформацией. У 5% остальных больных паркинсонизмом в основе патологии лежат
чисто генетические факторы (первичный паркинсонизм). Результаты исследований,
проведенных за последние восемь лет, указывают на наличие связи между мутациями
в геноме больных и образованием белков с аномальной конформацией или сбоем в
работе защитных механизмов клетки. Это наиболее впечатляющее достижение в
изучении природы болезни Паркинсона за многие годы.
.4.2 Виновник - окружающая среда!?
Гипотеза
о роли в возникновении болезни Паркинсона неблагоприятных внешних факторов
циркулировала в научных кругах не одно десятилетие. Однако подтверждение ей
было получено лишь в начале 1980-х гг., когда Уильям Лангстон (J. William
Langston) из Института по изучению болезни Паркинсона в Саннивейле, шт.
Калифорния, обнаружил, что у молодых наркоманов буквально через несколько дней
после приема одного из синтетических вариантов героина (чайна-уайт) появились
симптомы, характерные для паркинсонизма. Оказалось, что партия наркотика была
загрязнена веществом, губительным для нейронов черной субстанции. После курса
терапии у некоторых из наркоманов контроль над отдельными движениями
восстановился, состояние же большинства не изменилось. В течение следующих
нескольких лет ученые пытались найти другие вещества со сходным действием, и в
2003 г. Национальный институт по изучению влияния окружающей среды на состояние
здоровья выделил на эти работы $20 млн. Сегодня выявлено несколько случаев
развития паркинсонизма в результате длительных контактов человека с различными
пестицидами, гербицидами и фунгицидами. Тимоти Гринэмайер (J. Timothy Greenamyre)
из Университета Эимори показал в опытах на животных, что при контакте с
пестицидом ротеноном, который вырабатывается из натуральных продуктов и часто
применяется в органическом сельском хозяйстве, возможно образование белковых
агрегатов, губительных для дофаминпродуцирующих нейронов и клеточных органелл,
вырабатывающих энергию. Кроме того, у подопытных животных наблюдались
двигательные расстройства. Помимо «провокаторов» паркинсонизма существуют и
вещества, оказывающие противоположное действие. Специалисты полагают, что
некоторым защитным эффектом обладают никотин и кофеин. Но стоит ли беспрерывно
пить кофе или выкуривать по пачке сигарет в день ради призрачной надежды
избежать паркинсонизма? Некоторые пестициды, в том числе изготовленные только
из природных веществ, могут вызывать у животных симптомы, характерные для
болезни Паркинсона.
.4.3 Генетические основы
В 1997 г. Михаэль Полимеропулос (Mihael H. Polymeropoulos) из Национальных институтов здоровья идентифицировал мутацию в гене, кодирующем белок под названием альфа-синуклеин, у членов итальянских и греческих семей, страдавших наследственной формой паркинсонизма. Мутация наследовалась по аутосомно-доминантному типу, т.е. для возникновения болезни было достаточно одной мутантной копии гена (полученной от отца или матери). Мутация в гене альфа-синуклеина встречается крайне редко: доля несущих ее больных составляет лишь 1% от числа всех страдающих паркинсонизмом. Но сам факт обнаружения связи между наличием мутантного белка и болезнью Паркинсона вызвал большой интерес в научных кругах. Отчасти это было связано с тем, что в том же году выяснилось, что альфа-синуклеин (не важно, мутантный или нормальный) относится к категории белков, способных к образованию кластеров. Отсюда напрашивается вывод: разобравшись, каким образом мутация приводит к паркинсонизму, можно раскрыть тайну образования телец Леви в дофаминпродуцирующих клетках черной субстанции при болезни Паркинсона.
Альфа-синуклеин
- это небольшой белок, состоящий всего из 144 аминокислот. Полагают, что он
участвует в обмене сигналами между нейронами. Мутации в его гене приводят к
минимальным изменениям в аминокислотной последовательности белка. В настоящее
время идентифицированы несколько таких мутаций, две из них приводят к единичным
аминокислотным заменам. Опыты на дрозофилах, нематодах и мышах показали, что
если мутантный альфа-синуклеин образуется в нейронах черной субстанции в
больших количествах, то происходит их дегенерация и возникают двигательные
расстройства. Обнаружено также, что мутантные альфа-синуклеины не упаковываются
надлежащим образом и образуют кластеры - тельца Леви. Кроме того, они подавляют
деятельность убиквитин-протеасомной системы и устойчивы к протеасомной
деградации. Недавно обнаружилось, что при наличии в геноме избыточных копий
нормального гена альфа-синуклеина также развивается болезнь Паркинсона. В 1998
г. японские ученые Есикуни Мицуно (Yoshikuni Mizuno) из Университета Джунтендо
и Нобуёси Шимицу (Nobuyoshi Shimizu) из Университета Кейо идентифицировали еще
один ген - он кодирует белок паркин, мутация в котором приводит к
наследственному паркинсонизму, но другого типа. Такая мутация обычно
встречается у людей, заболевших в возрасте до 40 лет, и чем моложе пациент, тем
выше вероятность, что в основе заболевания лежит мутация в гене паркина. Те,
кто получают мутантные копии гена и от отца, и от матери, обязательно
заболевают, но к группе риска относятся и люди, несущие лишь одну копию
мутантного гена. Мутации в гене паркина встречаются чаще, чем в гене
альфа-синуклеина, однако точные цифры неизвестны. В последнее время появились
сообщения об идентификации целого ряда других генов, имеющих отношение к
паркинсонизму.
3)
Лечение Паркинсона сегодня
Врачи
используют два основных подхода к лечению паркинсонизма. У каждого есть свои
преимущества и недостатки, однако оба лишь смягчают симптомы заболевания, не
устраняя его причины.
.1
Лекарственная терапия
Сегодня
применяются лекарственные средства, имитирующие действие дофамина, вещества -
метаболические предшественники дофамина (например, леводопа) и препараты,
блокирующие разрушение дофамина. Кроме того, используются лекарства,
действующие на некоторые недофаминовые системы головного мозга, страдающие при
паркинсонизме, такие, в частности, где нейромедиаторами служат ацетилхолин и
глутамат. Многие из них помогают на начальных стадиях заболевания, но при
длительном приеме вызывают побочные эффекты. Основной из них - непредсказуемые
переходы от нормального состояния к периодам заторможенности, тремора и
ригидности. Кроме того, возникают дискинезии, особенно сильно выраженные у
молодых пациентов.
.2
Стимуляция глубинных структур мозга
В
начале XX века ученые обнаружили, что разрушение небольшого числа клеток
структур мозга, отвечающих за аномальную двигательную активность, уменьшает
тремор. И хотя подобная операция сопровождается мышечной слабостью, больные
предпочитают лечь под нож, чем жить с постоянно трясущимися руками. В 1938 г.
хирурги провели операцию на базальных ганглиях, которая дала положительный
результат. Обнаружилось, что устранение гиперактивных или неправильно
реагирующих на сигнал клеток приводит к нормализации работы остальных отделов
мозга. К несчастью, хирургическое вмешательство не стало решением всех проблем.
Если при этом затрагивались оба полушария или место разрушения подкорковых
структур было выбрано не совсем точно, могли возникнуть такие серьезные
осложнения, как нарушение речи и когнитивных функций. В 1970-х гг.
обнаружилось, что высокочастотная электростимуляция отдельных частей головного
мозга имитирует их разрушение, не вызывая при этом никаких побочных эффектов.
Сегодня методы стимуляции головного мозга в разных вариантах используются для
лечения многих неврологических расстройств (см. статью «Чудеса магнитотерапии»,
«В мире науки», №12, 2003 г.). Больным паркинсонизмом в одну из структур
базального ганглия (бледный шар или субталамическую область) вводят электрод,
подсоединенный к генератору электрических импульсов, который имплантирован в
область грудной клетки. Длительность импульса составляет 90 микросекунд,
амплитуда - три вольта, частота - 185 импульсов в секунду. Генератор подлежит
замене каждые пять лет. После того как разработчики этого метода, Алим Бенабид
(Alim Benabid) и Пьер Поллак (Pierre Pollak) из Гренобльского университета во
Франции, сообщили, что подобная стимуляция приводит к значительному уменьшению
тремора и ригидности, метод вышел на одно из первых мест в лечении
паркинсонизма. Иногда на фоне стимуляции удавалось существенно снизить дозу
принимаемых препаратов и даже вообще обходиться без них. Впрочем, стимуляция
глубинных структур головного мозга не может остановить патологический процесс и
не решает проблем, связанных с утратой когнитивных функций, расстройств речи и
чувства равновесия. Среди нерешенных проблем остается и такая: является ли
бледный шар и субталамическая область оптимальными для подобных воздействий?
Неясно также, какие именно электрические и химические процессы отвечают за
смягчение симптомов. Считалось, что стимуляция глубинных структур мозга
вызывает тот же эффект, что и хирургическое вмешательство, а именно - разрушает
клетки. Однако недавно выяснилось, что эта процедура приводит к повышению
частоты импульсации.