Материал: Болезни, связанные с нарушением фолдинга белка
Болезни, связанные с нарушением фолдинга белка
Содержание
Введение
) Структура и функциональная роль шаперонов в фолдинге белков
.1 Класификация шаперонов
.2 Роль шаперонов в фолдинге белков
.3 Роль шаперонов в защите белков клеток от денатурирующих
воздействий
) Болезни, связанные с нарушением фолдинга белков
.1 Болезнь Альцхаймера
.2 Прионовые болезни
.3 Преэклампсимия
.4 Болезнь Паркинсона
.4.1 «Плохие белки»
.4.2 Виновник-окружающая среда!?
.4.3 Генетические основы
) Лечение Паркинсона сегодня
.1 Лекарственная терапия
.2 Стимуляция глубинных структур мозга
.3 Новые подходы к лечению болезни
Заключение
Список используемой литературы
Введение
В
биохимии и молекулярной биологии фо́лдингом белка (укладкой белка, от англ.
<https://ru.wikipedia.org/wiki/%D0%90%D0%BD%D0%B3%D0%BB%D0%B8%D0%B9%D1%81%D0%BA%D0%B8%D0%B9_%D1%8F%D0%B7%D1%8B%D0%BA>
folding) называют процесс спонтанного сворачивания
полипептидной
<https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D0%BF%D1%82%D0%B8%D0%B4> цепи
в уникальную нативную пространственную структуру (так называемая третичная
структура
<https://ru.wikipedia.org/wiki/%D0%A2%D1%80%D0%B5%D1%82%D0%B8%D1%87%D0%BD%D0%B0%D1%8F_%D1%81%D1%82%D1%80%D1%83%D0%BA%D1%82%D1%83%D1%80%D0%B0>).
 <https://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:Protein_folding.png>
<https://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:Protein_folding.png>
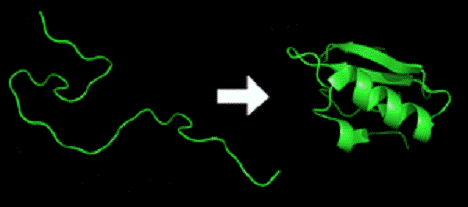
Рис.1.
Переход первичной структуры полипептида (слева) в третичную структуру (справа)
Каждая молекула белка <https://ru.wikipedia.org/wiki/%D0%91%D0%B5%D0%BB%D0%BE%D0%BA> начинает формироваться как полипептид <https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D0%BF%D1%82%D0%B8%D0%B4%D1%8B>, транслируемый <https://ru.wikipedia.org/wiki/%D0%A2%D1%80%D0%B0%D0%BD%D1%81%D0%BB%D1%8F%D1%86%D0%B8%D1%8F_(%D0%B1%D0%B8%D0%BE%D1%85%D0%B8%D0%BC%D0%B8%D1%8F)> из последовательности мРНК <https://ru.wikipedia.org/wiki/%D0%9C%D0%A0%D0%9D%D0%9A> в виде линейной цепочки аминокислот <https://ru.wikipedia.org/wiki/%D0%90%D0%BC%D0%B8%D0%BD%D0%BE%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D1%8B>. У полипептида нет устойчивой трёхмерной структуры (пример в левой части изображения). Однако все аминокислоты в цепочке имеют определённые химические свойства: гидрофобность <https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D1%84%D0%BE%D0%B1%D0%BD%D0%BE%D1%81%D1%82%D1%8C>, гидрофильность <https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D1%84%D0%B8%D0%BB%D1%8C%D0%BD%D0%BE%D1%81%D1%82%D1%8C>, электрический заряд. При взаимодействии аминокислот друг с другом и клеточным окружением получается хорошо определённая трёхмерная структура -конформация <https://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BD%D1%84%D0%BE%D1%80%D0%BC%D0%B0%D1%86%D0%B8%D1%8F>. В результате на внешней поверхности белковой глобулы формируются полости активных центров <https://ru.wikipedia.org/wiki/%D0%90%D0%BA%D1%82%D0%B8%D0%B2%D0%BD%D1%8B%D0%B9_%D1%86%D0%B5%D0%BD%D1%82%D1%80_%D1%84%D0%B5%D1%80%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2>, а также места контактов субъединиц мультимерных белков друг с другом и с биологическими мембранами <https://ru.wikipedia.org/wiki/%D0%9A%D0%BB%D0%B5%D1%82%D0%BE%D1%87%D0%BD%D1%8B%D0%B5_%D0%BC%D0%B5%D0%BC%D0%B1%D1%80%D0%B0%D0%BD%D1%8B>.
В редких случаях нативными могут быть сразу две конформации белка (т. н. конформеры). Они могут сильно различаться, и даже выполнять различные функции. Для этого необходимо, чтобы в разных областях фазового пространства <https://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B7%D0%BE%D0%B2%D0%BE%D0%B5_%D0%BF%D1%80%D0%BE%D1%81%D1%82%D1%80%D0%B0%D0%BD%D1%81%D1%82%D0%B2%D0%BE> белковой молекулы существовали два примерно равных по энергии состояния, каждое из которых будет встречаться в нативной форме с соответствующей вероятностью.
Для стабилизации третичной структуры многие белки в клетке подвергаются посттрансляционной модификации <https://ru.wikipedia.org/wiki/%D0%9F%D0%BE%D1%81%D1%82%D1%82%D1%80%D0%B0%D0%BD%D1%81%D0%BB%D1%8F%D1%86%D0%B8%D0%BE%D0%BD%D0%BD%D0%B0%D1%8F_%D0%BC%D0%BE%D0%B4%D0%B8%D1%84%D0%B8%D0%BA%D0%B0%D1%86%D0%B8%D1%8F>. Весьма часто встречаются дисульфидные мостики <https://ru.wikipedia.org/wiki/%D0%94%D0%B8%D1%81%D1%83%D0%BB%D1%8C%D1%84%D0%B8%D0%B4%D0%BD%D0%B0%D1%8F_%D1%81%D0%B2%D1%8F%D0%B7%D1%8C> между пространственно близкими участками полипептидной цепи.
Для корректной работы белков весьма важна правильная трёхмерная структура. Ошибки сворачивания обычно приводят к образованию неактивного белка с отличающимися свойствами. Считается, что некоторые болезни происходят от накопления в клетках неправильно свёрнутых белков.
В
фолдинге участвуют белки-шапероны
<https://ru.wikipedia.org/wiki/%D0%A8%D0%B0%D0%BF%D0%B5%D1%80%D0%BE%D0%BD%D1%8B>.
И хотя большинство только что синтезированных белков могут сворачиваться и при
отсутствии шаперонов, некоторому меньшинству обязательно требуется их присутствие.
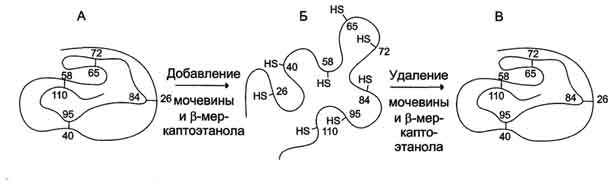
Рис. 2. Денатурация и ренативация рибонуклеазы. А - нативная молекула рибонуклеазы, в третичной структуре которой имеются 4 дисульфидные связи; Б - денатурированная молекула рибонуклеазы; В - нативная молекула рибонуклеазы, в структуре которой вновь образованы 4 дисульфидные связи между теми же остатками цистеина.
фолдин белок паркинсон болезнь
Механизм
сворачивания белков до конца не изучен. Экспериментальное определение
трёхмерной структуры белка часто очень сложно и дорого. Однако аминокислотная
последовательность белка обычно известна. Поэтому учёные пытаются использовать
различные биофизические
<https://ru.wikipedia.org/wiki/%D0%91%D0%B8%D0%BE%D1%84%D0%B8%D0%B7%D0%B8%D0%BA%D0%B0>
методы, чтобы предсказать пространственную структуру белка
<https://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%B5%D0%B4%D1%81%D0%BA%D0%B0%D0%B7%D0%B0%D0%BD%D0%B8%D0%B5_%D1%81%D1%82%D1%80%D1%83%D0%BA%D1%82%D1%83%D1%80%D1%8B_%D0%B1%D0%B5%D0%BB%D0%BA%D0%B0>
из его аминокислотной последовательности.
1) Структура и функциональная роль шаперонов в фолдинге белков
В процессе синтеза полипептидных цепей, транспорта их через мембраны, при сборке олигомерных белков возникают промежуточные нестабильные конформации, склонные к агрегации. На вновь синтезированном полипептиде имеется множество гидрофобных радикалов, которые в трёхмерной структуре спрятаны внутри молекулы. Поэтому на время формирования нативной конформации реакционно-способные аминокислотные остатки одних белков должны быть отделены от таких же групп других белков.
Во всех известных организмах от прокариотов до высших эукариотов обнаружены белки, способные связываться с белками, находящимися в неустойчивом, склонном к агрегации состоянии. Они способны стабилизировать их конформацию, обеспечивая фолдинг белков. Эти белки получили название "шапероны".
. Классификации шаперонов (Ш)
В соответствии с молекулярной массой все шапероны можно разделить на 6 основных групп:
· высокомолекулярные, с молекулярной массой от 100 до 110 кД;
· Ш-90 - с молекулярной массой от 83 до 90 кД;
· Ш-70 - с молекулярной массой от 66 до 78 кД;
· Ш-60;
· Ш-40;
· низкомолекулярные шапероны с молекулярной массой от 15 до 30 кД.
Среди шаперонов различают: конститутивные белки (высокий базальный синтез которых не зависит от стрессовых воздействий на клетки организма), и индуцибельные, синтез которых в нормальных условиях идёт слабо, но при стрессовых воздействиях на клетку резко увеличивается. Индуцибельные шапероны относят к "белкам теплового шока", быстрый синтез которых отмечают практически во всех клетках, которые подвергаются любым стрессовым воздействиям. Название "белки теплового шока" возникло в результате того, что впервые эти белки были обнаружены в клетках, которые подвергались воздействию высокой температуры.
. Роль шаперонов в фолдинге белков
При синтезе белков N-концевая область полипептида синтезируется раньше, чем С-концевая область. Для формирования конформации белка нужна его полная аминокислотная последовательность. Поэтому в период синтеза белка на рибосоме защиту реакционно-способных радикалов (особенно гидрофобных) осуществляют Ш-70.
Ш-70 - высококонсервативный класс белков, который присутствует во всех отделах клетки: цитоплазме, ядре, ЭР, митохондриях. В области карбоксильного конца единственной полипептидной цепи шаперонов есть участок, образованный радикалами аминокислот в форме бороздки. Он способен взаимодействовать с участками белковых молекул и развёрнутых полипептидных цепей длиной в 7-9 аминокислот, обогащённых гидрофобными радикалами. В синтезирующейся полипептидной цепи такие участки встречают примерно через каждые 16 аминокислот.
Фолдинг многих высокомолекулярных белков, имеющих сложную конформацию (например, доменное строение), осуществляется в специальном пространстве, сформированном Ш-60. Ш-60 функционируют в виде олигомернoго комплекса, состоящего из 14 субъединиц (рис. 1-23).
Ш-60 образуют 2 кольца, каждое из которых состоит из 7 субъединиц, соединённых друг с другом. Субъединица Ш-60 состоит из 3 доменов: апикального (верхушечного), промежуточного и экваториального. Верхушечный домен имеет ряд гидрофобных остатков, обращённых в полость кольца, сформированного субъединицами. Экваториальный домен имеет участок связывания с АТФ и обладает АТФ-азной активностью, т.е. способен гидролизовать АТФ до АДФ и Н3РО4.
Шапероновый комплекс имеет высокое сродство к белкам, на поверхности
которых есть элементы, характерные для несвёрнутых молекул (прежде всего
участки, обогащённые гидрофобными радикалами). Попадая в полость шаперонового
комплекса, белок связывается с гидрофобными радикалами апикальных участков
Ш-60. В специфической среде этой полости, в изоляции от других молекул клетки
происходит перебор возможных конформации белка, пока не будет найдена
единственная, энергетически наиболее выгодная конформация.
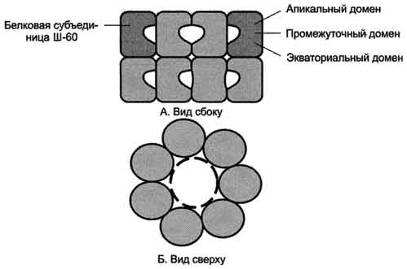
Рис. 3. Структура шаперонового комплекса, состоящего из 14 белковых
молекул Ш-60
Высвобождение белка со сформированной нативной конформацией сопровождается гидролизом АТФ в экваториальном домене. Если белок не приобрёл нативной конформации, то он вступает в повторную связь с шапероновым комплексом. Такой шаперонзависимый фолдинг белков требует затрат большого количества энергии.
Таким образом, синтез и фолдинг белков протекают при участии разных групп шаперонов, препятствующих нежелательным взаимодействиям белков с другими молекулами клетки и сопровождающих их до окончательного формирования нативной структуры (рис. 1-24).
. Роль шаперонов в защите белков клеток от денатурирующих стрессовых воздействий
Шапероны, участвующие в защите клеточных белков от денатурирующих
воздействий, как уже говорилось выше, относят к белкам теплового шока (БТШ) и в
литературе часто обозначают как HSP (от англ, heat shock protein).
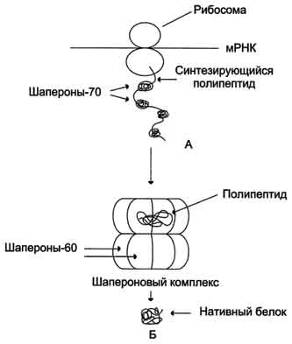
Рис. 4. Участие шаперонов в фолдинге белков. А - участие шаперонов-70 в
предотвращении гидрофобных взаимодействий между участками синтезирующегося
полипептида; Б - формирование нативной конформации белка в шапероновом
комплексе.
При действии различных стрессовых факторов (высокая температура, гипоксия, инфекция, УФО, изменение рН среды, изменение молярности среды, действие токсичных химических веществ, тяжёлых металлов и т.д.) в клетках усиливается синтез БТШ. Имея высокое сродство к гидрофобным участкам частично денатурированных белков, они могут препятствовать их полной денатурации и восстанавливать нативную конформацию белков.
Установлено, что кратковременные стрессовые воздействия увеличивают
выработку БТШ и повышают устойчивость организма к длительным стрессовым
воздействиям. Так, кратковременная ишемия сердечной мышцы в период бега при
умеренных тренировках значительно повышает устойчивость миокарда к длительной
ишемии, вызванной стенокардией или закупоркой сосудов сердца тромбом. В
настоящее время перспективными исследованиями в медицине считают поиски
фармакологических и молекулярно-биологических способов активации синтеза БТШ в
клетках.
2) Болезни, связанные с нарушением фолдинга белков
Лишь небольшая часть теоретически возможных вариантов полипептидных цепей может принимать одну стабильную пространственную структуру. Большинство же таких белков может принимать множество конформаций с примерно одинаковой энергией Гиббса, но с различными свойствами. Первичная структура большинства известных белков, отобранных эволюцией, обеспечивает исключительную стабильность одной конформации.
Однако некоторые растворимые в воде белки при изменении условий могут приобретать конформацию плохо растворимых, способных к агрегации молекул, образующих в клетках фибриллярные отложения, именуемые амилоидом (от лат. amylum - крахмал). Так же как и крахмал, амилоидные отложения выявляют при окраске ткани йодом. Это может происходить:
• при гиперпродукции некоторых белков, в результате чего увеличивается их концентрация в клетке;
• при попадании в клетки или образовании в них белков, способных влиять на конфор-мацию других молекул белка;
• при активации протеолиза нормальных белков организма, с образованием нерастворимых, склонных к агрегации фрагментов;
• в результате точечных мутаций в структуре белка.
В результате отложения амилоида в органах и тканях нарушаются структура и
функция клеток, наблюдают их дегенеративные изменения и разрастание
соединительнотканных или глиальных клеток. Развиваются болезни, называемые
амилоидозами. Для каждого вида амилоидоза характерен определённый тип амилоида.
В настоящее время описано более 15 таких болезней.
2.1 Болезнь Альцхаймера
Болезнь Альцхаймера - наиболее часто отмечаемый β-амилоидоз нервной системы, как правило, поражающий лиц преклонного возраста и характеризующийся прогрессирующим расстройством памяти и полной деградацией личности. В ткани мозга откладывается β-амилоид - белок, образующий нерастворимые фибриллы, нарушающие структуру и функции нервных клеток. β-амилоид - продукт изменения конформации нормального белка организма человека. Он образуется из более крупного предшественника частичным протеолизом и синтезируется во многих тканях. β-Амилоид, в отличие от своего нормального предшественника, содержащего много а-спиральных участков, имеет вторичную β-складчатую структуру, агрегирует с образованием нерастворимых фибрилл, устойчив к действию протеолитических ферментов.
Причины нарушения фолдинга нативных белков в ткани мозга ещё предстоит
выяснить. Возможно, с возрастом уменьшается синтез шаперонов, способных
участвовать в формировании и поддержании нативной конформации белков, или
увеличивается активность протеаз, что приводит к увеличению концентрации
белков, склонных изменять конформацию.
.2 Прионовые болезни
Прионы - особый класс белков, обладающих инфекционными свойствами. Попадая в организм человека или спонтанно возникая в нём, они способны вызывать тяжёлые неизлечимые заболевания ЦНС, называемые прионовыми болезнями. Название «прионы» происходит от аббревиатуры английской фразы proteinaceous infectious particle - белковая инфекционная частица.
Прионовый белок кодируется тем же геном, что и его нормальный аналог, т.е. они имеют идентичную первичную структуру. Однако два белка обладают различной конформацией: прионовый белок характеризуется высоким содержанием β-слоёв, в то время как нормальный белок имеет много а-спиральных участков. Кроме того, прионовый белок обладает устойчивостью к действию протеаз (подкласс гидролаз 3.4., расщепляет пептидные связи в белке и пептидах) и, попадая в ткань мозга или образуясь там спонтанно, способствует превращению нормального белка в прионовый в результате межбелковых взаимодействий. Образуется так называемое «ядро полимеризации», состоящее из агрегированных прионовых белков, к которому способны присоединяться новые молекулы нормального белка.