Материал: Анализ соматических проявлений гибридного дисгенеза у Drosophila melanogaster (на модели признака cubitus interruptus Dominant)
В геноме дрозофилы элемент hobo представлен тремя различными формами: (1) полно- и неполноразмерными элементами; (2) элементами с внутренними делециями и (3) последовательностями, подобными элементу hobo - hRS (hobo-related sequences), которые считаются остатками реликтовых hobo элементов (тех, которые инвазировали группу предшественника группы melanogaster на раннем этапе). Считается, что перемещаться могут все эти последовательности, используя канонический hobo как источник транспозазы. Показано, что некоторые цис-регуляторные элементы hobo способны распознаваться транскрипционными факторами генов развития дрозофилы, что свидетельствует о возможности использования этих последовательностей в качестве материала в процессе эволюции [20].
Считается, что существует 2 класса линий в отношении hobo элемента. Это Н линии, которые содержат 3 т.п.н. полноразмерные элементы и многочисленные их производные меньшего размера. И второй класс - это Е линии, характеризуются отсутствием полноразмерных элементов, однако, имеют некоторое количество их фрагментов. Н линии обычно содержат от 2 до 10 полноразмерных копий hobo на геном, а дефектных элементов 30-75. Гибридный дисгенез наблюдается в реципрокных скрещиваниях Н и Е линий и характеризуется повышенной частотой возникновения мутаций, включая хромосомные перестройки, и редукцию гонад [31]. Структура, распространение в геноме и генетическое поведение этого МГЭ в общих чертах подобны системе Р элемента [28].
.2 Явление и значение атрофии гонад, как
признака гибридного дисгенеза
Активация мобильных элементов в системах гибридного дисгенеза вызывает, среди прочих нарушений, особый вид стерильности гибридов, которая обусловлена недоразвитием гонад [19]. Дисгенная стерильность по-разному проявляется в трех системах гибридного дисгенеза. P-M дисгенез [35] приводит к недоразвитию яичников у гибридных самок и семенников у самцов, в I-R системе [37], не происходит изменения морфологии гонад, но увеличивается количество дефектных яиц и частота гибели эмбрионов (SF-стерильность). Активация hobo элементов в H-E системе гибридного дисгенеза приводит как к недоразвитию гонад у самок и самцов первого поколения, так и к высокому уровню доминантных леталей среди отложенных яиц [28].
Стерильность является следствием потери зародышевых клеток на стадиях раннего эмбриогенеза и личинки. Для P-M гибридного дисгенеза гибель зародышевых клеток значительно усиливается при повышении температуры до 29 °С [22]. Атрофия гонад один из характерных и интенсивно изучаемых аспектов P-M и H-E систем гибридного дисгенеза. GD-стерильность является следствием вымирания клеток в примордиальной зародышевой линии возможно из-за хромосомных разрывов, опосредованных активностью P-элемента [21]. Однако ни кинетика гибели зародышевых клеток, ни число клеток, которые должны быть элиминированы для появления GD-стерильности не известно. Первые признаки стерильности появляются уже у 5-6 часовых эмбрионов. Максимальный уровень гибели клеток наблюдается на личиночной стадии развития, когда зародышевые клетки испытывают экспоненциальный рост, но некоторые умирающие клетки были обнаружены до деления клеток зародышевой линии [36].
Механизм гибели клеток может быть обусловлен разрывами хромосом, имеющими летальный эффект. Следствием этого является отсутствие половых клеток в яичниках и семенниках и общее недоразвитие их у взрослых гибридных самок и самцов. Гибриды могут быть полностью стерильны, если редуцированы обе железы и частично фертильны, если атрофирован один семенник или яичник [30]. Неатрофированные гонады у дисгенных гибридов часто отстают в своем развитии и содержат меньшее число яиц или сперматоцитов по сравнению с недисгенными особями [36].
Степень выраженности гонадной атрофии сильно зависит от температуры, при которой идет развитие гибридов. В отношении Р-М системы атрофия наиболее значительна при 29° С у самок и при 27° С у самцов, а при 24° С и ниже практически отсутствует [24]. Для Н-Е системы характерна наиболее сильная атрофия при 25°С и наименьшая при 29° С [27]. При более низких температурах АГ наблюдается в меньшей степени. Количество и размерность копий Р- и hobo-элементов так же сильно влияют на способность индуцировать гибридный дисгенез, в связи с чем, частота гонадной атрофии может изменяться от нескольких до ста процентов [32].
Сказать точно, в чем заключается адаптивное и /или эволюционное значение синдрома гибридного дисгенеза пока сложно. Предполагается, что атрофия гонад (одно из проявлений синдрома гибридного дисгенеза) является одним из механизмов реализации нескрещиваемости видов и особей из разных популяций и, следовательно, может быть компонентом механизмов видообразования. Примером являются популяции дрозофилы, которые скрещиваясь на границе ареалов дают стерильное потомство. Это объясняется тем, что МГЭ, локализированные в геноме особей данной популяции, обладающей, скажем, Р- или Н-цитотипом, при скрещивании с особями другой популяции (с противоположным цитотипом) дают стерильное потомство[34].
В то же время существует и другая,
противоположная эволюционная функция МГЭ, которая несёт адаптивное значение для
организма. Известно, что при попадании организма в стрессовые условия,
начинается активная транспозиция МГЭ в геноме. В результате перемещений и
встраивания в геномные последовательности, изменяется активность генов,
синтезируемые ими продукты, что влечет за собой каскад реакций, которые
непосредственно влияют на дальнейшее функционирование клеток, органов и
организма в целом. Эти изменения могут быть разнонаправлены, повышать или
снижать адаптивные возможности индивида, но при этом основной их задачей
является увеличение разнообразия особей в популяции. Наиболее приспособленные к
сложившимся стрессовым условиям особи будут иметь шанс выжить и размножиться
[29].
.3 Соматические проявления гибридного дисгенеза
и механизмы их формирования
МГЭ имеют определенную структурную организацию, благодаря которой могут перемещаться в геноме как в пределах одной хромосомы, так и между хромосомами различных клеток и тканей. Как уже было сказано, МГЭ имеют способность увеличивать число копий в геноме хозяина, вызывать мутации в соматических и генеративных тканях, встраиваясь в гены или окрестности генов, служить причиной хромосомных перестроек, влиять на фертильность особей и даже приводить организм к гибели [31]. Возникающие мутации могут не сказываться на жизнеспособности организма, если они возникли в гене, который отвечает, например, за формирование фенотипического признака [19].
Транспозиции МГЭ, способных вызывать синдром гибридного дисгенеза, как было показано в работах некоторых авторов, приводят не только к атрофии гонад, но и к различным мутациям в соматических тканях. В редких случаях мутационные изменения могут иметь адаптивное значение и особи с такими мутациями получают преимущество перед другими сородичами для выживания и оставления потомства. Однако, чаще всего, мутации вредны для организма и приводят к стерильности или гибели особи. Перемещения МГЭ при гибридном дисгенезе у дрозофилы происходят преимущественно в клетках зародышевого пути. Причина различной активности МГЭ в клетках соматических и генеративных тканей подробно изучена у Р-элемента и заключается в особенностях тканеспецифичного сплайсинга транспозазной пре-м-РНК. Однако в ряде работ были описаны случаи перемещения ретротранспозонов в соматических клетках у высших организмов [38].
Что касается транспозонов, существуют единичные данные, прямо или косвенно свидетельствующие о соматической активности этих элементов. Так, например, Коваленко Л.В. в своей работе на тему hobo-элемент как фактор нестабильности генома D. melanogaster в клетках генеративных и соматических тканей получила такие результаты: hobo-элемент способен проявлять транспозиционную активность в клетках соматических тканей. Во-первых, выявлена взаимосвязь между присутствием в геноме активного hobo-элемента и повышением частоты рекомбинаций на клетках крыла Drosophila melanogaster. Во-вторых, с помощью метода FISH, продемонстрировано перемещение hobo-элемента в клетках соматических тканей у Drosophila melanogaster и получена оценка частоты hobo-транспозиций - 3,5x10-2 на сайт, на Х-хромосому [29].
Активность мобильных элементов в P-M и H-E системах гибридного дисгенеза обусловливает мутабильность некоторых нестабильных локусов. В P-M системе наибольшую известность получил локус singed-weak [35], в H-E системе локус vgal [26] и сконструированный маркерный элемент h(w+). Аллель snw обусловлена инсерцией двух дефектных P-элементов и делеция одного или другого из этих элементов в присутствии транспозазы полноразмерных элементов приводит к появлению соответствующих производных аллелей sne и sn(+). Повышенная мутабильность локуса vgal обусловлена активацией дефектных копий hobo в присутствии активных элементов этого семейства. Генетически сконструированный маркерный элемент h(w+) представляет hobo-элемент со встроенным геном mini-white, который определяет оранжевую окраску глаз [23]. Маркерная white линия несет в X-хромосоме два сконструированных элемента h(w+). Это обусловливает оранжевый фенотип цвета глаз, но при эксцизии одного из элементов цвет становится менее выраженным [31]. Линии с нестабильными аллелями широко используются при оценке активности P и hobo-элементов в дисгенных скрещиваниях, и частота мутирования этих аллелей служит дополнительным количественным критерием.
Таким образом, контроль активности мобильных генетических элементов в системах гибридного дисгенеза тесно взаимосвязан с механизмами транспозиций и репарации генетических повреждений. Это обусловливает чувствительность гибридного дисгенеза к действию внешних факторов и его модификацию различным генетическим фоном. Существующие предпосылки позволяют рассматривать синдром гибридного дисгенеза не только как показатель активности некоторых семейств мобильных генетических элементов, но и как целостную генетическую систему, обеспечивающую контроль генетической изменчивости генотипа в неблагоприятных условиях [29].
В целом же, вопрос об активности транспозонов в
соматических клетках D. melanogaster остается открытым. Выявление возможности и
изучение особенностей транспозиций МГЭ в соматических клетках имеет большое
значение, поскольку в ряде работ описан повреждающий эффект соматических
перемещений Р-элемента . Более того, соматические мутации представляют собой
потенциальную угрозу малигнизации клеток [2].
.4 Связь экспрессивности признака cubitus
interruptus Dominant с экспрессией гена ciD
In(4)ciD <#"785969.files/image001.jpg">
Рис. 1. Структура аллеля ciD <#"785969.files/image002.jpg"> Прерванная жилка крыла L4 Рваный край крыла
 Прерванная
жилка крыла L4, L5
Прерванная
жилка крыла L4, L5
 Прерванная
жилка крыла L4, L5 Постериорный край крыла слит с алулой
Прерванная
жилка крыла L4, L5 Постериорный край крыла слит с алулой
 Скручивание
крыла
Скручивание
крыла
 Нормальный
фенотип
Нормальный
фенотип
Рис. 2. Фенотип ciD <#"785969.files/image007.jpg">
Рис. 3. Взаимодействие ciD <#"785969.files/image008.jpg"> а
 b
b


 с
с
 а
а
b 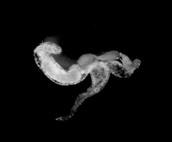
 с
с
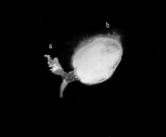
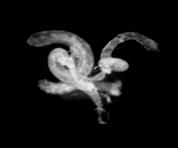
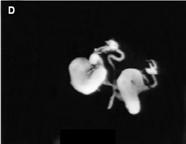
Рис. 4. Атрофия гонад у самок (верхняя строка) и
самцов (нижняя строка) дрозофилы: a - нормальные гонады; b - односторонняя
атрофия гонад; с - двусторонняя атрофия гонад
.3.3. Методика оценки экспрессивности признака сiD
Экспрессивность количественного признака сiD
оценивали по соотношению длины отсутствующего участка жилки к проекции её
полной длины [43]. Измерение осуществляли на фотографиях имаго, выполненных с
помощью стереоскопического микроскопа и цифровой камеры. Обработка фотографий
производилась с помощью программного обеспечения ImageJ, а вычисления -
Homacosoft XQR2. Результат выражался в долях.
.3.4 Методы статистического анализа
Частоту атрофии гонад (АГ) вычисляли как %АГ=%А0 + 1/2% А1 (Marin et al., 2000). Для всех вариантов эксперимента рассчитывали ошибку выборочной доли (Атраментова).
Сравнение выборочных долей проводили при помощи критерия Фишера.
Показатель экпрессивности усредняли в каждом варианте опыта. И для каждого среднего рассчитывали статистическую ошибку.
Сравнение экспрессивности в разных вариантах эксперимента проводили при помощи дисперсионного анализа количественных признаков [18].
Для вычислений использовали программное
обеспечение Microsoft Excel и STATISTICA_8.0.550.
. ОХРАНА ТРУДА И БЕЗОПАСНОСТЬ В ЧРЕЗВЫЧАЙНЫХ
СИТУАЦИЯХ
Охрана труда - это система правовых, социально-экономических, организационно-технических, санитарно-гигиенических и лечебно-профилактических мероприятий и средств, направленных на сохранение жизни, здоровья и трудоспособности человека в процессе трудовой деятельности [5]. Государственная политика в области охраны труда направлена на создание безопасных и здоровых условий труда, предотвращение несчастных случаев и профессиональных заболеваний.
Первостепенным ее принципом является приоритет жизни и здоровья работающих. Реализация принципов и задач охраны труда связана с научным прогнозированием возможных чрезвычайных ситуаций в производственном процессе и выполнение мероприятий, привлечение средств снижающих их уровень риска.
При выполнении научно-исследовательских работ в области генетики в роли потенциального источника опасности могут выступать исследуемые биологические объекты, методы работы с ними, а также результаты исследования. Перед началом выполнения работы со мной был проведен первичный инструктаж [6] по технике безопасности при работе в биологической (генетической) лаборатории. Суть данного инструктажа касалась изложения правил безопасного выполнения работ.
При выполнении данной курсовой работы биологическим объектом, на котором проводилось исследование, являлись различные линии (в том числе и сконструированные в лаборатории, но не генетически модифицированные согласно определению вида Drosophila melanogaster [9]. Данный вид не является напрямую опасным для человека, а также не является переносчиком возбудителей заболеваний человека. Он представляет собой всемирно признанный модельный генетический объект и не значится ни в одном из списков видов, представляющих реальную или потенциальную биологическую угрозу, в законодательной базе Украины [13, 14, 15]. Тем не менее, разведение данного объекта в лабораторных условиях связано с использованием химических реактивов, электроприборов и лабораторной посуды. При выполнении курсовой работы использование упомянутых оборудования и материалов осуществлялось в соответствии с типовыми и местными инструкциями по технике безопасности, разработанным службой охраны труда ХНУ имени В.Н. Каразина и утвержденными в надлежащем порядке [Инструкции по охране труда № 71, № 5; Инструкция о мероприятиях пожарной безопасности в служебных и конторских помещениях (офисах)], а также в соответствии с инструкциями, прилагающимися непосредственно к приборам и расходным материалам.
Так, при работе с данным биологическим объектом (для его наркотизации) используется диэтиловий эфир - химическое соединение, которое входит в список №2 (Прекурсоры, относительно которых устанавливаются контрольные мероприятия) Списка наркотических средств, психотропных веществ и прекурсоров [7]. Все виды работ, требующие использования данного соединения выполнялись под вытяжкой [8].
Поскольку источником электрической безопасности является электрический ток, основными источниками потенциальной опасности в ляаборатории могут стать - электроприборы (термостат, сухо-жаровой шкаф, электроплита, осветители к микроскопам), розетки, выключатели, ПК, поэтому разработаны соответствующие меры защиты согласно нормативным требованиям ГОСТ 14254-69, ГОСТ 14255-69, ПУЭ-87. В лаборатории для обеспечения работы электрооборудования применяется переменный ток, напряжением 220 В. По степени опасности поражения электрическим током данное помещение приравнивается к помещениям без повышенной опасности, согласно ПУЭ-87 [10].