Материал: Анализ метода плазмохимической конверсии HCl в Cl2
Для реакций из таблицы 2.2 кинетические
уравнения были сформированы как:
![]()
+ B ® продукты реакции
(11 - 30, 32 - 35, 38 - 43, 85 - 93)
![]()
+ A ® продукты реакции
(31, 36, 37, 44)
![]()
+ A + A ® продукты реакции
(50, 57, 71)
![]()
A + A + B ® продукты реакции
(45 - 49, 51 - 56, 63, 64, 66 - 70)
![]()
+ B + C ® продукты реакции
(58 - 62, 65, 72 - 76, 77 - 80)
![]()
® продукты реакции (81 - 84)
![]()
Для решения дифференциальных кинетических уравнений был использован метод Гира. Расчеты проводились с использованием готового программного обеспечения.
Константы скорости для реакций электронного
удара 1-10, представленных в таблице 2.2 были рассчитаны по уравнению:
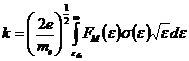 (2.1)
(2.1)
в использованием максвэлловского приближения для
функции распределения электронов по энергиям. Необходимые для расчета сечения
процессов брали из справочной литературы. Температура электронов задавалась
парамеррически как ![]() = 1.5-2.0 эВ, что
является типичными значениями для стационарных разрядов, возбуждаемых при
атмосферном давлении. Константы скоростей реакций 11-80 были взяты из
справочника [9, 10]. Константы скорости гетерогенной рекомбинации оценивались
предположении о первом кинетическом порядке рекомбинации (механизм Или-Ридила)
по формуле
= 1.5-2.0 эВ, что
является типичными значениями для стационарных разрядов, возбуждаемых при
атмосферном давлении. Константы скоростей реакций 11-80 были взяты из
справочника [9, 10]. Константы скорости гетерогенной рекомбинации оценивались
предположении о первом кинетическом порядке рекомбинации (механизм Или-Ридила)
по формуле
![]() (2.2)
(2.2)
где ![]() -
вероятность рекомбинации,
-
вероятность рекомбинации, ![]() - коэффициент
диффузии частиц и
- коэффициент
диффузии частиц и ![]() - эффективная
длина диффузии, определяемая геометрическими параметрами реактора (
- эффективная
длина диффузии, определяемая геометрическими параметрами реактора (![]() ,
,
![]() ).
).
.2 Объект исследований
Объектом исследований служил идеализированный
плазмохимический реактор, состоящий из трех резко разграниченных зон (рис.
2.1).
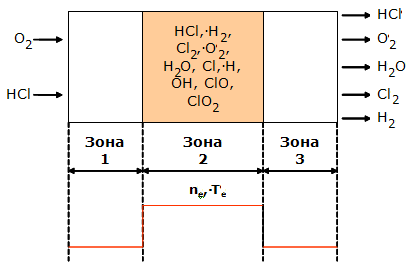
Рис. 2.1. Схема реактора
Исходные реагенты подаются в зону 1, где происходит их смешение. Далее смесь поступает в зону 2, где подвергается воздействию плазмы. Под действием электронных ударов идет образование атомов и радикалов, которые участвуют в различных химических реакциях. Затем газ, содержащий как стабильные, так и нестабильные частицы, поступает в зону 3, где происходит рекомбинация атомов и радикалов до стабильных продуктов. При этом принимались следующие допущения:
1) Профили концентрации и температуры электронов в зоне плазмы являются изотропными;
2) Инициирование химических реакций электронным ударом в зонах 1 и 3 отсутствует;
) Транспорт газа не оказывает влияния на кинетику химических реакций в зоне 2 (малая скорость потока, обеспечивающая tпр > 1 сек)
В таблице 2.3 приведены внешние параметры
процесса, использованные в расчетах.
Таблица 2.3.
Параметры процесса
|
Входные параметры |
|
|
Температура газа: |
300 K |
|
Температура (средняя энергия) электронов: |
2 эВ |
|
Давление: |
1.33´105 Па |
|
Время пребывания газа в зоне 2: |
1-3 sec |
|
Концентрация электронов в плазме: |
задавалась параметрически в диапазоне 106 - 1016 см-3 |
3. Обсуждение результатов
.1 Анализ кинетики плазмохимических процессов в
чистом HCl
При анализе кинетики плазмохимических процессов в чистом хлороводороде кинетическая схема включала в себя 26 реакций, а именно Р1,5,6,11,12,15,22,45,47,49,50,52,54,55,57,58,60,62-64,81,82,85,86,88,89 из таблицы 2.2.
Расчеты показали, что степень превращения (соотношение между концентрациями компонентов в зонах 1 и 3) заметно зависит от концентрации электронов. При малых концентрациях электронов (~107 см-3 , см. рис. 3.1.1) стационарные концентрации продуктов конверсии Cl, H, Cl2 и H2 на несколько порядков величины ниже концентрации молекул хлороводорода. Очевидно, что это связано с низкой скоростью диссоциации HCl электронным ударом. Так как в зоне плазмы имеет место выполнение неравенства [H], [Cl] << [H2], [Cl2], при переходе в зону 3 полная рекомбинация атомов практически не увеличивает концентрацию молекул. При этом концентрация целевого продукта - молекул Cl2 - в 430 раз ниже концентрации HCl, что говорит о пренебрежимо малых степенях превращения. Увеличение концентрации электронов (до ~1016 см-3 , см. рис. 3.1.2) улучшает ситуацию, но не изменяет ее принципиально. Очевидно, что рост концентрации электронов приводит как к росту скорости диссоциации хлороводорода по реакции Р1, так и увеличивает скорости разложения молекулярных продуктов реакции. Поэтому, хотя в зоне плазмы концентрации атомов хлора и водорода имеют один порядок величины с концентрацией HCl, количество H2 и Cl2 в тех же условиях значительно ниже. При переходе в зону 3 концентрации молекулярных компонентов несколько возрастают из-за рекомбинации атомов, однако стационарная концентрация Сl2 все равно остается ниже концентрации HCl в 5 раз. Формально это соответствует степени превращения 28%, однако встает вопрос о методе возбуждения плазмы для достижения такой концентрации электронов. По нашему мнению, даже если такой метод может быть найден и реализован, его суммарная стоимость будет соизмерима с затратами на электролиз.
Рассмотрим подробнее кинетику плазмохимических процессов в хлороводороде при концентрации электронов ~1011 см-3, которая легко достигается в условиях тлеющего или дугового разряда атмосферного давления.
Зона 2. Как видно из рис. 3.1.3, атомы Cl и H
образуются с одинаковой скоростью и имеют приблизительно равные концентрации
вплоть до времени протекания процесса ![]() ~
10-9 сек. Наличие одинакового количества атомов H и Cl объясняется реакцией
взаимодействия HCl c электронами (Р1), а близкими скоростями их гибели в
реакциях Р45, Р52 и Р58. Затем концентрация атомов Cl начинает интенсивно
увеличиваться по отношению к H, и в результате разница между стационарными
концентрациями H и Cl составит примерно 2 порядка величины. Это связано с
эффективным протеканием реакции Р12, которая расходует атомы H и одновременно
генерирует атомы хлора. Немонотонное поведение концентрации H связано с
конкурирующим действием реакций 1 и 12.
~
10-9 сек. Наличие одинакового количества атомов H и Cl объясняется реакцией
взаимодействия HCl c электронами (Р1), а близкими скоростями их гибели в
реакциях Р45, Р52 и Р58. Затем концентрация атомов Cl начинает интенсивно
увеличиваться по отношению к H, и в результате разница между стационарными
концентрациями H и Cl составит примерно 2 порядка величины. Это связано с
эффективным протеканием реакции Р12, которая расходует атомы H и одновременно
генерирует атомы хлора. Немонотонное поведение концентрации H связано с
конкурирующим действием реакций 1 и 12.
Хотя молекулы H2 и Cl2 образуются по одним и тем
же реакциям, таким как Р45 и Р52, концентрация H2 увеличивается быстрее вплоть
до ![]() =
10-4 - 10-3 сек. Дело в том, что молекулы Cl2 эффективно распадаются в Р22, в
том время как по Р12 идет образование молекул H2. Однако при наступлении
стационарного состояния процесса концентрации обоих компонентов выравниваются.
Это результат уменьшения скоростей реакций Р12 и Р22 из-за уменьшения
концентрации атомов H. Исходный реагент НCl незначительно расходуется в Р12, а
его стационарная концентрация определяется балансом между Р1 и Р58. При данном
значении
=
10-4 - 10-3 сек. Дело в том, что молекулы Cl2 эффективно распадаются в Р22, в
том время как по Р12 идет образование молекул H2. Однако при наступлении
стационарного состояния процесса концентрации обоих компонентов выравниваются.
Это результат уменьшения скоростей реакций Р12 и Р22 из-за уменьшения
концентрации атомов H. Исходный реагент НCl незначительно расходуется в Р12, а
его стационарная концентрация определяется балансом между Р1 и Р58. При данном
значении ![]() ,
максимальная концентрация Cl2 достигается после (6 - 8)Ч10-3 с. Тем не менее
HCl остается в качестве основного газообразного компонента, и степень конверсии
HCl в Cl2, при условии, что HCl чистый, ничтожно мала.
,
максимальная концентрация Cl2 достигается после (6 - 8)Ч10-3 с. Тем не менее
HCl остается в качестве основного газообразного компонента, и степень конверсии
HCl в Cl2, при условии, что HCl чистый, ничтожно мала.
Зона 3. Хотя стационарная концентрация атомарного Cl выше чем Cl2, рекомбинация атомов в зоне 3 не обеспечивает увеличения концентрации Cl2. Напротив, концентрация Cl2 слабо уменьшается поскольку эффект Р45 компенсируется реакцией Р22. Кроме того, процесс рекомбинации Cl протекает не только по Р45, но и по реакции Р58, которая не приводит к образованию Cl2. Реакция Р22 обеспечивает быструю гибель атомов H, в то время как высокое время жизни атомов Cl обусловлено их регенерацией по реакции Р12 (реакция Р11 практически не работает из-за высокой пороговой энергии и низкой константы скорости реакции).
Изложенные выше результаты могут быть обобщены в виде следующих положений:
1. Плазма в чистом хлороводороде не обеспечивает степеней конверсии выше 4% при типичных условиях, реализуемых в тлеющем разряде постоянного тока или высокочастотном разряде атмосферного давления.
2. Для повышения степени конверсии необходимо привлекать дополнительные механизмы диссоциации HCl не связанные с электронным ударом. Это позволило бы поддерживать относительно низкие концентрации электронов при высоких скоростях диссоциации HCl, предотвращая тем самым деструкцию целевого продукта - молекулярного хлора - по реакции Р6.
Как показывают литературные данные, одним из
таких механизмов может являться окислительная деструкция HCl в плазме смеси
хлороводорода с кислородом. Действительно, из табл.2.2 можно видеть, что
константа скорости взаимодействия HCl с атомами кислорода (Р13) на два порядка
величины выше константы скорости аналогичного процесса с участием молекул хлора
(Р23). Более того, продуктом Р13 является радикал ОН, который сам является
сильным окислителем и также взаимодействует с HCl по реакции Р14. Таким
образом, можно ожидать, что в такой системе будет происходить преимущественное
разложение HCl с накоплением молекулярного хлора.
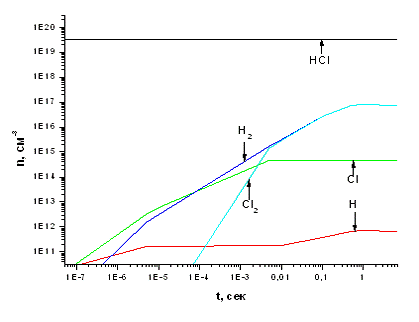
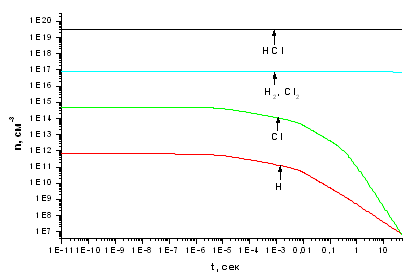
Рис. 3.1.1 Зависимость концентраций компонентов,
участвующих в процессе, от времени при концентрации электронов 1*107 см -3
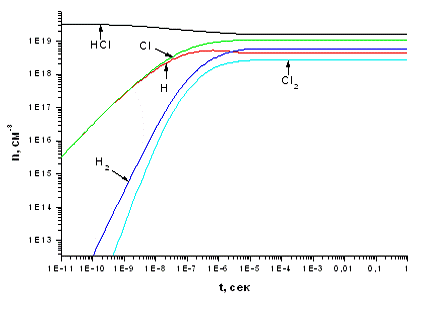
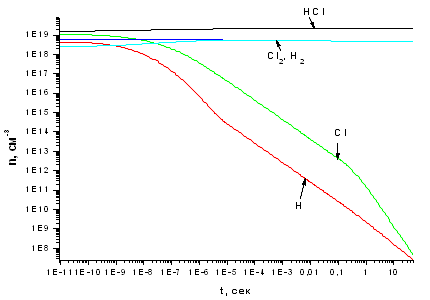
Рис. 3.1.2 Зависимость концентраций компонентов,
участвующих в процессе, от времени при концентрации электронов 1*1016 см -3
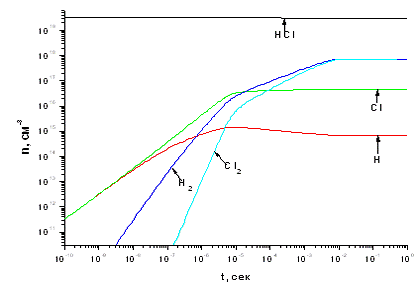
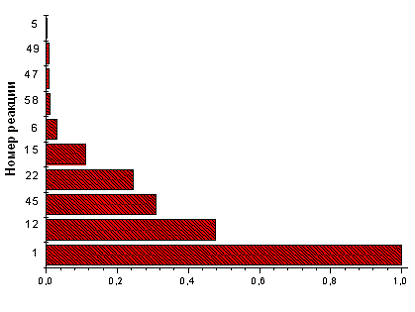
Рис. 3.1.3 Зависимость концентраций компонентов,
участвующих в процессе, от времени и расположение реакций, протекающих в
реакторе, по степени важности при концентрации электронов 1*1011 см -3
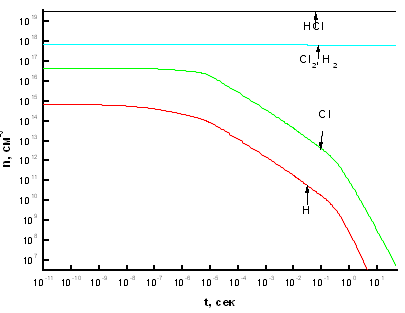
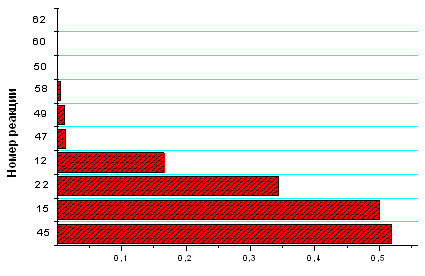
Рис. 3.1.4 Зависимость концентраций компонентов,
участвующих в процессе, от времени и расположение реакций, протекающих на
выходе из реактора, по степени важности при концентрации электронов 1´1011
см -3
.2 Анализ возможности получения хлора методом
окислительной деструкции HCl в плазме смеси HCl+O2
Для определения оптимальных параметров
проведения процесса было проведено исследование зависимости степени превращения
от начального состава смеси HCl+O2 и концентрации электронов. Соответствующие
данные представлены на рис. 3.2.1. Для характеристики степени превращения
использовалось отношение концентраций хлороводорода к хлору, наблюдаемых в зоне
3. Очевидно, что оптимизация процесса направлена на минимизацию этого параметра.
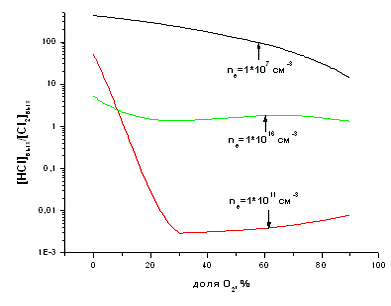
Рис. 3.2.1 График зависимости отношения HCl к
Cl2 на выходе из реактора от доли кислорода в смеси
Низкая степень конверсии при концентрации электронов 107 см-3 объясняется низкими скоростями инициирования химических процессов, и, в первую очередь, низкими скоростями Р1, Р2 и Р3. При ne = 1016 см-3 достигаются значительно более высокие степени превращения, однако лимитирующим фактором служит высокая скорость диссоциации целевого продукта при электронном ударе. Наиболее оптимальный вариант имеет место при ne = 1011 см-3, когда в зоне 3 концентрация целевого продукта примерно в 100 раз превышает концентрацию HCl. Для этих условий зависимость степени превращения от доли кислорода в смеси имеет явно выраженный максимум в области 30% О2.
Рассмотрим подробнее кинетику процесса при концентрации электронов 1011 см-3 и соотношении концентраций исходных компонентов смеси HCl - 70%, O2 - 30%.
1. Как видно из рис. 3.2.1, вплоть до 10-6
- 10-5 сек, кинетика образования Cl2 не проявляет существенных отличий по
сравнению с плазмохимической обработкой чистого HCl. Это связано с тем, что
количество частиц O и OH недостаточно велико и поэтому можно пренебречь
процессами с их участием, в том числе Р13 и Р14. При больших временах воздействия
плазмы на газовую смесь, когда концентрация O и ОH достигает 1011 - 1012 см-3,
влияние реакций Р13 и Р14 ускоряет разрушение молекул HCl и образование атомов
Cl. Одновременно по Р14 идет образование H2O из радикалов OH, являющихся
продуктом Р13. Так же частицы OH задействованы в Р31, Р72-76. Поэтому при
достижении времени возбуждения ![]() > 10-6 - 10-5
сек идет интенсивное накопление Cl, Cl2 и H2O. Это и является основным отличием
разрядов в чистом хлороводороде и в смеси HCl/O2.
> 10-6 - 10-5
сек идет интенсивное накопление Cl, Cl2 и H2O. Это и является основным отличием
разрядов в чистом хлороводороде и в смеси HCl/O2.
2. Из-за влияния реакций Р13 и Р14 концентрация HCl достигает более низких величин, чем в случае с обработкой чистого HCl, и это обеспечивает более высокую степень превращеня HCl в Cl2. Максимальная степень конверсии, характеризуемая максимальными значениями отношения концентраций HCl/Cl2 и HCl/H2O достигается при 30-60% кислорода в смеси. Во всем этом диапазоне кинетика процесса показывает одни и те же закономерности, как это было рассмотрено выше на примере смеси 70% HCl + 30% O2. Смесь 70% HCl + 30% O2 также является предпочтительной по соображениям экономии кислорода и наблюдения близких к максимальным степеней конверсии. Когда доля кислорода в смеси становится ниже 20 - 30% степень конверсии ограничивается быстрым расходованием образующегося атомарного кислорода (фактически, низкой скоростью образования атомарного кислорода при диссоциации О2 электронным ударом) и снижением скоростей процессов R13 и R14. В случае если доля кислорода в смеси превышает 60 - 70%, степень конверсии снижется по сравнению с максимальным значением из-за разлодения молекул хлора по реакциям R23 и R24
. Присутствие кислорода и
кислород-содержащих соединений не оказывает существенного влияния на кинетику
продуктов конверсии в зоне 3. Фактически, аналогично предыдущему случаю,
максимальные стационарные концентрации Cl2 и H2O формируются в зоне 2 и не
изменяются за счет рекомбинации атомов в зоне 3. Высокое время жизни в зоне 3
для Cl и ClO, а также быстрое разрушение атомов O обусловлено влиянием Р23.
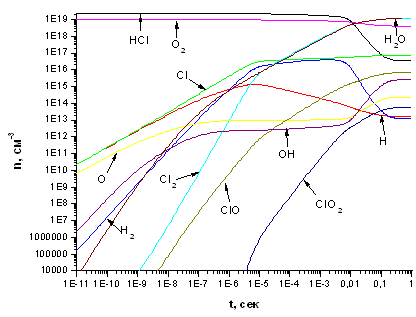
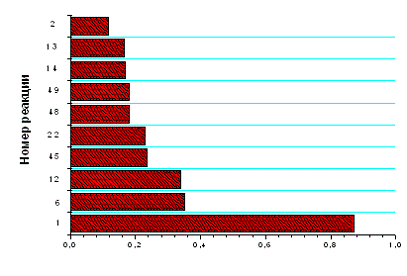
Рис. 3.2.2 Зависимость концентраций компонентов, участвующих в процессе, от времени при концентрации электронов 1*1011 см -3 и степень важности реакций, соотношение HCl:Cl2=70:30
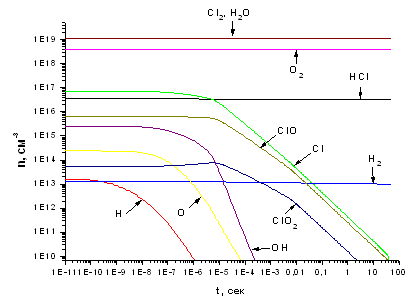
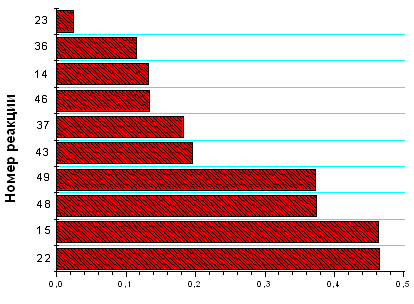
Рис. 3.2.2 Зависимость концентраций компонентов,
участвующих в процессе, от времени и расположение реакций, протекающих на
выходе из реактора, по степени важности при концентрации электронов 1*1011 см
-3