Материал: Анализ метода плазмохимической конверсии HCl в Cl2
В мембранном электролизере протекают те же
химические реакции, что и в диафрагменном электролизере. Вместо пористой
диафрагмы используют катионную мембрану (Рис. 1.2.4.2).
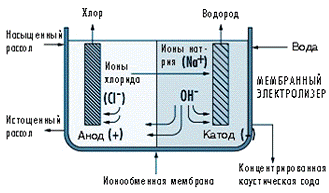
Рис. 1.2.4.2 Схема мембранного электролизера
Мембрана препятствует проникновению ионов хлора в католит, за счет чего непосредственно в электролизере можно получить каустическую соду почти без соли, концентрацией от 30 до 35%. Поскольку исчезает необходимость отделять соль, выпаривание обеспечивает получение 50%-ной коммерческой каустической соды значительно проще и при меньших капиталовложениях и энергозатратах. Поскольку каустическая сода в мембранном процессе значительно большей концентрации, то в качестве катода используют дорогостоящий никель.
Ртутный электролизер состоит из двух
электролитических камер (Рис. 1.2.4.3). В первой камере на аноде протекает
следующая реакция:
Cl- = Cl2 + 2e- (1.2.4.1)
В первой камере на катоде протекает следующая реакция:
+ + Hg + e- = Na*Hg (1.2.4.2)
Рассол затекает по стальному наклонному желобу, покрытому по бокам резиной. Ртуть, являющаяся катодом, протекает под рассолом. Титановые аноды с покрытием подвешены в рассоле для получения хлора, который из электролизной камеры поступает в систему накопления и переработки. Натрий подвергается электролизу и амальгамируется ртутью в первой электролизной камере. Амальгама направляется во вторую электрохимическую камеру, называемую разлагателем амальгамы. Разлагатель амальгамы - это электролизер с графитовым катодом и амальгамой в качестве анода.
В разлагателе амальгамы происходит следующая
реакция:
2Na*Hg + 2H2O = 2NaOH + 2Hg +H2 ↑
(1.2.4.3)
С помощью ртутного электролизера также получают
каустическую соду с концентрацией до 50% на выходе из второй камеры
электролизера [3].
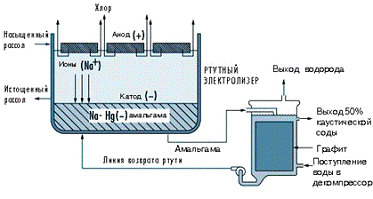
Рис. 1.2.4.3 Схема ртутного электролизера
В 2006, около 84% всего производства хлора около 59 миллионов тонн получали диафрагменным и мембранными методами, и только 13% при помощи ртутных электролизеров.
Сравнение промышленных методов получения хлора
проведено в таблице 1.2.4.1 [6]:
Таблица 1.2.4.1
Сравнение промышленных способов получения хлора
|
Метод получения |
Ртутный |
Диафрагменный |
Мембранный |
|
Рабочая плотность тока (кА/м2) |
8 - 13 |
0,9 - 2,6 |
3 - 5 |
|
Напряжение ячейки (В) |
3,9-4,2 |
2.9 - 3,5 |
3.0 - 3,6 |
|
Концентрация NaOH (%) |
50 |
12 |
33 - 35 |
|
Потребление энергии (кВт*ч/MT Cl2) при плотности тока (кА/м2) |
3360 (10) |
2720 (1,7) |
2650 (5) |
|
Потребление пара (кВт*ч/MT Cl2) при онцентрации NaOH 50% |
0 |
610 |
180 |
Электрохимическое получение хлора - одна из самых больших технологий в мире, которая, однако имеет два существенных недостатка:
1) Электрохимическое производство является вредным и опасным в связи с использованием ртути, выделением водорода в качестве побочного продукта и др. факторов.
2) Электрохимическое производство хлора является очень энергетически интенсивным процессом, потребляющим 2400 миллиардов кВт*ч электроэнергии в год. Это более 60% электроэнергии, потребляемой всей мировой химической промышленностью.
В связи с этим проблема поиска альтернативных
методов получения хлора является очень актуальной.
.3 Плазма: основные понятия и свойства.
Процессы, протекающие в плазме. Применение плазмы
Плазма - состояние вещества, характеризующееся высокой степенью ионизации и равенством концентраций положительных и отрицательных зарядов (квазинейтральностъю). Плазма в стационарном состоянии может существовать только при наличии факторов, восполняющих убыль заряженных частиц. В газовом разряде плазма в стационарном состоянии поддерживается за счёт внешнего электрического поля, энергия которого расходуется на ионизацию газа. Газ в состоянии плазмы находится в следующих видах разряда:
· положительный столб тлеющего и дугового разряда:
· дуговой разряд низкого давления с накаленными электродами:
· отдельные области высокочастотного и сверхвысокочастотного разрядов.
Плазма в общем случае состоит из электронов, ионов и нейтральных частиц - атомов и молекул (радикалов), находящихся как в основном, так и в возбужденных состояниях: вращательных, колебательных, электронных. Концентрация заряженных частиц в плазме достигает 1017 1/см3 и по своей электропроводности плазма приближается к проводникам. Плазму нельзя представлять как механическую смесь компонент, так как все частицы плазмы находятся в непрерывном взаимодействии друг с другом, и плазма в целом обладает рядом специфических свойств, которые вовсе не присущи отдельным её составляющим. Различают изотермическую и неизотермическую плазму.
Изотермической плазме отвечает ионизированный газ при высокой температуре, когда энергии (температуры) всех составляющих плазму частиц равны (Те =Tt =Tg) и все процессы обмена являются равновесными.
Неизотермическая плазма характеризуется тем, что средняя энергия (температура) электронов во много раз превышает энергию ионов и нейтральных частиц (Те"Тi=Tg). Такое состояние реализуется при относительно небольшом выделении джоулевой теплоты за счет высокой теплоемкости газа тяжелых частиц и быстрого уноса теплоты из зоны разряда. Существование неизотермической плазмы поддерживается за счёт внешних факторов, например электромагнитного поля, при этом процессы обмена энергией являются неравновесными. Последнее связано с тем, что электроны, как наиболее легкие из заряженных частиц, преимущественно отбирают энергию внешнего поля, однако в силу своей малой массы не способны эффективно перераспределять ее при столкновениях с "тяжелыми" частицами. Наиболее часто применяется в технологии микроэлектроники один из видов неизотермической плазмы - неравновесная низкотемпературная газоразрядная плазма (ННГП) пониженного давления.
ННГП представляет собой слабо ионизованный газ при давлениях 10-1 - 103 Па со степенью ионизации 10-5 - 10-3. Средняя энергия электронов составляет 1-10 эВ (концентрация электронов 109 - 1012 1/см3), а средняя энергия тяжелых частиц (атомов, молекул и ионов) ниже в среднем на два порядка величины. К внешним (задаваемым) параметрам ННГП относятся тип плазмообразующего газа, его давление и расход газа, ток разряда (в случае ВЧ и СВЧ разрядов - удельная мощность, вкладываемая в разряд), а также геометрия плазмохимического реактора и его конструкционные материалы, находящиеся в контакте с зоной разряда и послесвечения. Количественное описание плазменных процессов требует знания концентраций частиц всех типов, а также их энергетических, пространственных и временных распределений. Одним из определяющих факторов, формирующих стационарное состояние неизотермической плазмы, является кинетика процессов при электронном ударе, которая, в свою очередь, определяется функцией распределения электронов по энергиям (ФРЭЭ). К параметрам, определяющим вид ФРЭЭ. следует отнести приведенную напряженность электрического поля (E/N или Е/Р, где N - общая концентрация нейтральных частиц в реакторе. Р - давление газа), транспортные коэффициенты электронов, а также первичный состав нейтральных частиц. Величина E/N и другие внутренние параметры устанавливаются на уровне, обеспечивающем баланс скоростей образования и гибели заряженных частиц. Таким образом, плазма является сложной самоорганизующейся и самосогласованной системой, в которой внутренние параметры, определяющие кинетику и механизмы плазменных процессов, сами зависят от скоростей и направлений этих процессов.
Под действием электронного удара в плазме протекают различные элементарные процессы взаимодействия электронов с атомами, молекулами или ионами, в результате которых происходит изменение их энергетического или химического состояния. Виды этих процессов представлены в таблице 1.3.1.
В силу того, что энергия электронов существенно превышает энергию тяжелых частиц, именно эти процессы количественно определяют скорости диссоциации, ионизации и электронного возбуждения, которые имеют высокие пороговые энергии. Соударения электронов с молекулами газа делятся на упругие и неупругие. При упругих соударениях происходит перераспределение кинетической энергии взаимодействующих частиц без изменения их внутренней энергии (процесс 1. табл. 1.3.1). Максимальная доля энергии, передаваемой при упругом соударении, пропорциональна отношению масс сталкивающихся частиц:
=2me/M (1.3.1)
где me - масса электрона, М- масса молекулы газа.
Данное выражение справедливо, если молекула газа неподвижна. Если энергией молекул газа пренебречь нельзя по сравнению с энергией электронов, то выражение для X принимает вид:
=2me/M*(1-Eg/E), (1.3.2)
где E и Eg - энергии электрона и
"тяжелой" частицы, соответственно.
Таблица 1.3.1
Типы элементарных процессов
|
Реакция |
Схема реакции |
|
|
1. |
Передача импульса |
AB + e(p1) → AB + e(p2) |
|
2. |
Возбуждение |
AB + e → AB* + e |
|
3а. |
Диссоциативное прилипание |
AB + e → A- + B |
|
3б. |
Образование ионной пары |
AB + e → A- + B+ + e |
|
4 |
Отлипание |
A- + e → A + 2e |
|
5 |
Диссоциация |
AB + e → A + B + e |
|
6 |
Ионизация |
AB + e → AB+ + e |
|
7 |
Диссоциативная ионизация |
AB + e → A+ + B + 2e |
При неупругих столкновениях столкновение электронов с атомами или молекулами сопровождается изменением внутренней энергии или химического состояния последних (процессы 2-7. таблица 1.3.1). Неупругие соударения могут быть первого рода и второго рода. При неупругих соударениях первого рода происходит передача энергии от электронов к атомам или молекулам газа. Неупругие соударения второго рода сопровождаются передачей энергии от возбуждённых атомов или молекул к электронам [7].
Наибольший прогресс в практическом использовании плазмы низкого давления к настоящему времени достигнут в электронной промышленности и прежде всего в микроэлектронике. Здесь плазмохимическими методами решаются задачи нанесения тонких диэлектрических, проводящих и полупроводниковых слоев, создания поверхностной конфигурации интегральных схем путем локального плазменного травления указанных поверхностных слоев, а также очистки поверхностей неорганических материалов от органических веществ, включая удаление резистивных слоев в литографических операциях. Достаточно широко известно применение неравновесной плазмы для поверхностной обработки металлов в машиностроении. В последние 15-20 лет начался интенсивный процесс проникновения плазменных технологических процессов в технологию легкой и текстильной промышленности, хотя реальные достижения здесь еще скромны. Основу этого направления составляет модифицирование поверхностных свойств полимерных (пленочных или тканых) материалов путем обработки в плазме травящих пли полимеризующихся газов. Получаемые разнообразные технологические эффекты чаще всего связаны с приданием поверхностям гидрофильных или гидрофобных свойств. Однако наблюдаются эффекты, которые не могут быть объяснены лишь этими причинами и пока до конца не выяснены. Широкое практическое применение плазмохимических процессов в легкой промышленности тормозится рядом причин, среди которых нужно отметить отсутствие необходимого оборудования, к тому же весьма далекого от традиционно используемого, а также недостаточную изученность устойчивости и потребительской ценности достигаемых эффектов.
Разумеется, три указанных сферы применения
плазмы низкого давления не охватывают всего многообразия ее уже реализуемых
возможностей. Однако физико-химические основы упомянутых в иных плазменных
технологических процессов и способы их технической реализации в достаточной
степени общие [8].
Заключение
Из представленного обзора литературы видно, что существующая технология промышленного получения хлора имеет серьезные недостатки, связанные с негативным действием на окружающую среду, опасностью производства и высокой энергоемкостью. Альтернативой классическим химическим технологиям могут служить плазмохимические технологии. Особенности плазмохимических технологий является то, что в них имеет место неравновесная активация химических реакций (не термически, а электронным ударом), при этом достигаемые степени превращения веществ также могут существенно превышать равновесные.
Целью настоящей работы являлось исследование
возможности плазмохимической конверсии HCl в Cl2. Выбор в качестве исходного
реагента HCl обусловлен тем, что хлороводород является побочным продуктом
многих химических производств, который мало востребован в основном
производстве. В результате большая часть хлороводорода утилизируется в
нейтрализаторах на NaOH.
2. Методическая часть
.1 Инструмент исследований
В качестве основного инструмента исследований
было выбрано моделирование плазмы. Для определения взаимосвязей между входными
параметрами процесса и концентрациями частиц использовалась глобальная
(0-мерная) модель, оперирующая величинами, усредненными по объему реактора. В
ходе анализа литературных данных был составлен набор процессов, протекающих в
плазме чистого хлороводорода и в смесях HCl с кислородом. Этот список включает
93 реакции для частиц в основном состоянии и возбужденных атомов кислорода в
состоянии 1d. Список компонентов и список процессов приведены в таблицах 2.1 и
2.2, соответсвенно.
Таблица 2.1
Реагенты и продукты реакции
|
Компоненты |
|
|
На входе в реактор: |
HCl, O2 |
|
Зона плазмы: |
HCl, O2, O(3p), O(1d), Cl2, Cl, H2, H, H2O, OH, ClO, ClO2 |
|
На выходе из реактора: |
HCl, O2, Cl2, H2, H2O |
Таблица 2.2
Набор процессов для моделирования плазмы
|
Номер реакции |
Реакция |
Константа скорости при T=300 K |
|
|
Реакции электронного удара: |
|
||
|
Р1 |
HCl + e ® H + Cl + e |
Eq.(2) |
|
|
Р2 |
O2 + e ® O(3p) + O(3p) + e |
Eq.(2) |
|
|
Р3 |
O2 + e® O(3p) + O(1d) + e |
Eq.(2) |
|
|
Р4 |
O(3p) + e ® O(1d) + e |
Eq.(2) |
|
|
Р5 |
H2 + e ® H + H + e |
Eq.(2) |
|
|
Р6 |
Cl2 + e ® Cl + Cl + e |
Eq.(2) |
|
|
Р7 |
H2O + e ® H + OH + e |
Eq.(2) |
|
|
Р8 |
OH + e ® O(3p) + H + e |
Eq.(2) |
|
|
Р9 |
ClO + e ® Cl + O(3p) + e |
Eq.(2) |
|
|
Р10 |
ClO2 + e ® ClO + O(3p) + e |
Eq.(2) |
|
|
Реакции взаимодействия атомов и радикалов: |
|
||
|
Р11 |
HCl + Cl ® Cl2 + H |
3.16´10-20 |
|
|
Р12 |
HCl + H ® Cl + H2 |
6.31´10-14 |
|
|
Р13 |
HCl + O(3p) ® OH + Cl |
3.16´10-12 |
|
|
Р14 |
HCl + OH ® H2O + Cl |
1.26´10-11 |
|
|
Р15 |
H2 + Cl ® HCl + H |
3.98´10-14 |
|
|
Р16 |
H2 + O(3p) ® OH + H |
5.01´10-17 |
|
|
Р17 |
H2 + O(1d) ® OH+H |
2.00´10-10 |
|
|
Р18 |
H2 + OH ® H2O + H |
6.31´10-15 |
|
|
Р19 |
H2O + O(3p) ® OH + OH |
3.98´10-24 |
|
|
Р20 |
H2O + O(1d) ® OH + OH |
2.00´10-10 |
|
|
Р21 |
H2O + H ® H2 + OH |
2.51´10-25 |
|
|
Р22 |
Cl2 + H ® HCl + Cl |
6.31´10-12 |
|
|
Р23 |
Cl2 + O(3p) ® ClO + Cl |
7.94´10-14 |
|
|
Р24 |
Cl2 +O(1d) ® ClO + Cl |
1.58´10-10 |
|
|
Р25 |
O2 + H ® O(3p) + OH |
2.51´10-22 |
|
|
Р26 |
O2 + O (1d) ® O(3p) + O2 |
2.51´10-11 |
|
|
Р27 |
O(3p) + O (1d) ® O(3p) + O(3p) |
2.51´10-12 |
|
|
Р28 |
Cl + O(1d) ® Cl + O(3p) |
2.51´10-12 |
|
|
Р29 |
OH + O(3p) ® H + O2 |
5.01´10-11 |
|
|
Р30 |
OH + H ® O(3p) + H2 |
5.01´10-18 |
|
|
Р31 |
OH + OH ® H2O + O(3p) |
6.31´10-13 |
|
|
Р32 |
OH + Cl ® ClO + H |
2.00´10-17 |
|
|
Р33 |
ClO + O(3p) ® O2 + Cl |
3.16´10-12 |
|
|
Р34 |
ClO + O(1d) ® O2+Cl |
3.18´10-11 |
|
|
Р35 |
ClO + Cl ® Cl2 + O |
1.26´10-15 |
|
|
Р36 |
ClO + ClO ® Cl2 + O2 |
1.00´10-12 |
|
|
Р37 |
ClO + ClO ® ClO2 + Cl |
1.58´10-12 |
|
|
Р38 |
ClO + H2 ® HCl + OH |
5.01´10-16 |
|
|
Р39 |
ClO + H ® HCl + O(3p) |
5.11´10-11 |
|
|
Р40 |
ClO + H ® Cl + OH |
2.00´10-13 |
|
|
Р41 |
ClO2 + O(3p) ® ClO + O2 |
1.58´10-12 |
|
|
Р42 |
ClO2 + Cl ® ClO + ClO |
1.58´10-12 |
|
|
Р43 |
ClO2 + Cl ® Cl2 + O2 |
1.58´10-11 |
|
|
Р44 |
ClO2 + ClO2 ® Cl2 + O2 + O2 |
1.58´10-15 |
|
|
Реакции тройного соударения: |
Cl + Cl + HCl ® Cl2 + HCl |
5.21´10-32 |
|
|
Р46 |
Cl + Cl + O2 ® Cl2 + O2 |
5.21´10-32 |
|
|
Р47 |
Cl + Cl + H2 ® Cl2 + H2 |
5.21´10-32 |
|
|
Р48 |
Cl + Cl + H2O ® Cl2 + H2O |
5.21´10-32 |
|
|
Р49 |
Cl + Cl + Cl2 ® Cl2 + Cl2 |
5.21´10-32 |
|
|
Р50 |
Cl + Cl + Cl ® Cl2 + Cl |
5.21´10-32 |
|
|
Р51 |
Cl + Cl + OH ® Cl2 + OH |
5.21´10-32 |
|
|
Р52 |
H + H + HCl ® H2 + HCl |
1.00´10-32 |
|
|
Р53 |
H + H + O2 ® H2 + O2 |
1.00´10-32 |
|
|
Р54 |
H + H + H2 ® H2 + H2 |
1.00´10-32 |
|
|
Р55 |
H + H + Cl2 ® H2 + Cl2 |
1.00´10-32 |
|
|
Р56 |
H + H + H2O ® H2 + H2O |
1.00´10-32 |
|
|
Р57 |
H + H + H ® H2 + H |
1.00´10-32 |
|
|
Р58 |
H + Cl + HCl ® HCl + HCl |
5.13´10-32 |
|
|
Р59 |
H + Cl + O2 ® HCl + O2 |
5.13´10-32 |
|
|
Р60 |
H + Cl + H2 ® HCl + H2 |
5.13´10-32 |
|
|
Р61 |
H + Cl + H2O ® HCl + H2O |
5.13´10-32 |
|
|
Р62 |
H + Cl + Cl2 ® HCl + Cl2 |
5.13´10-32 |
|
|
Р63 |
H + Cl + Cl® HCl +Cl |
5.13´10-32 |
|
|
Р64 |
H + Cl + H ® HCl + H |
5.13´10-32 |
|
|
Р65 |
H + Cl + OH ® HCl + OH |
5.13´10-32 |
|
|
Р66 |
O(3p) + O(3p) + O2 ® O2 + O2 |
1.20´10-32 |
|
|
Р67 |
O(3p) + O(3p) + HCl ® O2 + HCl |
1.20´10-32 |
|
|
Р68 |
O(3p) + O(3p) + Cl2 ® O2 + Cl2 |
1.20´10-32 |
|
|
Р69 |
O(3p) + O(3p) + H2 ® O2 + H2 |
1.20´10-32 |
|
|
Р70 |
O(3p) + O(3p) + H2O(3p) ® O2 + H2O |
1.20´10-32 |
|
|
Р71 |
O(3p) + O(3p) + O(3p) ® O2 + O(1d) |
1.20´10-32 |
|
|
Р72 |
H + OH + HCl ® H2O + HCl |
1.26´10-31 |
|
|
Р73 |
H + OH + H2 ® H2O + H2 |
1.26´10-31 |
|
|
Р74 |
H + OH + O2 ® H2O + O2 |
1.26´10-31 |
|
|
Р75 |
H + OH + H2O ® H2O + H2O |
1.26´10-31 |
|
|
Р76 |
H + OH + Cl2 ® H2O + Cl2 |
1.26´10-31 |
|
|
Р77 |
Cl + O(3p) + HCl ® ClO + HCl |
1.00´10-32 |
|
|
Р78 |
Cl + O(3p) + O2 ® ClO + O2 |
1.00´10-32 |
|
|
Р79 |
Cl + O(3p) + H2 ® ClO + H2 |
1.00´10-32 |
|
|
Р80 |
Cl + O(3p) + H2O ® ClO + H2O |
1.00´10-32 |
|
|
Гетерогенные реакции: |
|
||
|
Р81 |
Cl ® Cl(s) |
1.00´10-2 |
|
|
Р82 |
H ® H(s) |
2.00´10-2 |
|
|
Р83 |
O(3p) ® O(s) |
1.00´10-2 |
|
|
Р84 |
O(1d) ® O(3p) |
1 |
|
|
Р85 |
Cl + Cl(s) ® Cl2 |
1.00´10-7 |
|
|
Р86 |
H + Cl(s) ® HCl |
1.00´10-7 |
|
|
Р87 |
O(3p) + Cl(s) ® ClO |
1.00´10-7 |
|
|
Р88 |
Cl + H(s) ® HCl |
1.00´10-7 |
|
|
Р89 |
H + H(s) ® H2 |
1.00´10-7 |
|
|
Р90 |
O(3p) + H(s) ® OH |
1.00´10-7 |
|
|
Р91 |
Cl + O(s) ® ClO |
1.00´10-7 |
|
|
Р92 |
H + O(s) ® OH |
1.00´10-7 |
|
|
Р93 |
O(3p) + O(s) ® O2 |
1.00´10-7 |
|