Материал: Анализ метода плазмохимической конверсии HCl в Cl2
Анализ метода плазмохимической конверсии HCl в Cl2
Федеральное агентство по образованию Российской Федерации
ГОУВПО
"Ивановский государственный химико-технологическиий университет"
Кафедра
ТП и МЭТ
Квалификационная работа бакалавра
Анализ
метода плазмохимической конверсии HCl в Cl2
Студент гр. 4/10:
Филимонов В.Г.
Руководитель:
Ефремов А.М.
Иваново 2008
Аннотация
В данной работе рассмотрены основные лабораторные и промышленные методы получения хлора, определены достоинства и недостатки отдельных методов. Проведен анализ кинетики плазмохимических процессов, определены основные механизмы конверсии. Показана возможность получения хлора методом окислительной деструкции HCl в условиях плазмы. Подобраны оптимальные параметры проведения процесса.
Объем квалификационной работы бакалавра 44 страницы, включая 13 рисунков, 5 таблиц и список используемых источников из 9 наименований.
хлор плазма конверсия окислительный
Содержание
Введение
. Литературный обзор
.1 Применение хлора
.2 Методы получения хлора
.2.1 Лабораторные методы получения хлора
.2.2 Основы электролиза
.2.3 Устройство электролизера
.2.4 Промышленные способы получения хлора
.3 Плазма: основные понятия и свойства. Процессы, протекающие в плазме. Применение плазмы
Заключение
. Методическая часть
.1 Инструмент исследований
.2 Объект исследований
. Обсуждение результатов
.1 Анализ кинетики плазмохимических процессов в чистом HCl
.2 Анализ возможности получения хлора методом окислительной деструкции HCl в плазме смеси HCl+O2
Основные выводы по работе
Список
используемой литературы
Введение
В наши дни хлор нашел широкое применение во многих отраслях хозяйства и промышленности. Он может применяться как в чистом виде так и в составе более сложных соединений. А так же использоваться на промежуточных стадиях производства каких-либо соединений. В промышленности хлор, главным образом, получают электролизом водного раствора NaCl. Электрохимическое получение хлора является одной из самых больших технологий в мире, однако она имеет существенных недостатка:
1. В технологии используются вредные и опасные вещества;
2. Колоссальные затраты электроэнергии.
Этот недостатки делают необходимимым разработку новой, альтернативной методики получения хлора.
В настоящее время одним из развивающихся направлений в науке являются плазмохимические технологии, которые имеют ряд преимуществ перед электрохимическими методами.
Целью настоящей работы являлось исследование
возможности плазмохимической конверсии HCl в Cl2.
1. Литературный обзор
.1 Применение хлора
Хлор представляет собой зеленовато-желтый газ с резким раздражающим запахом, состоящий из двухатомных молекул.
При обычном давлении он затвердевает при -101°С и сжижается при -34°С.
Плотность газообразного хлора при нормальных условиях составляет 3,214 кг/м3, то есть он примерно в 2,5 раза тяжелее воздуха и вследствие этого скапливается в низких участках местности, подвалах, колодцах, тоннелях. Газ растворим в воде: в одном объеме воды растворяется около двух его объемов.
Образующийся желтоватый раствор часто называют хлорной водой. Химическая активность его очень велика - он образует соединения почти со всеми химическими элементами.
Поэтому применение его разнообразно.
Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:
1. В производстве поливинилхлорида,
пластикатов, синтетического каучука, из которых изготавливают: изоляцию для
проводов, оконный профиль, упаковочные материалы, одежду и обувь, линолеум и
грампластинки, лаки, аппаратуру и пенопласты, игрушки, детали приборов,
строительные материалы. Поливинилхлорид производят полимеризацией винилхлорида,
который чаще всего получают, обрабатывая ацетилен хлористым водородом:
HC ≡ CH + HCl → CH2 =
CHCl (1.1.1)
2. Отбеливающие свойства хлора известны с давних времен, хотя не сам хлор "отбеливает", а атомарный кислород, который образуется при распаде хлорноватистой кислоты:
+ H2O → HCI + HCIO → 2HCI + O•
(1.1.2)
Этот способ отбеливания тканей, бумаги, картона используется уже несколько веков.
3. Производство хлорорганических инсектицидов - веществ, убивающих вредных для посевов насекомых, но безопасные для растений. На получение средств защиты растений расходуется значительная часть производимого хлора. Один из самых важных инсектицидов - гексахлорциклогексан (часто называемый гексахлораном). Это вещество впервые синтезировано еще в 1825 году Фарадеем, но практическое применение нашло только через 100 с лишним лет - в 30-х годах нашего столетия.
4. Использовался как оружие массового поражения и в производстве других отравляющих веществ массового поражения: иприт, фосген. Иприт был впервые использован как оружие массового поражения в 1915 году немецкими войсками в бельгийском городке Ипр, отсюда и название - "иприт".
5. Для обеззараживания воды (хлорирования) применяют хлор, двуокись хлора, хлорамин и хлорную известь. Наиболее распространённый способ обеззараживания питьевой воды основан на способности свободного хлора и его соединений угнетать ферментные системы микроорганизмов, катализирующие окислительно-восстановительные процессы.
. В химическом производстве для производства соляной кислоты, хлорной извести, бертолетовой соли, хлоридов металлов, ядов, лекарств, удобрений.
7. В металлургии для производства чистых металлов: титана, олова, тантала, ниобия.
8. Как индикатор солнечных нейтрино в хлор-аргонных детекторах [1].
Более наглядно масштабы применения хлора
представлены на рис. 1.1.1:
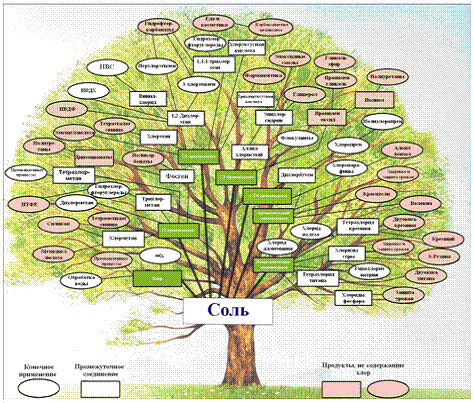
Рис. 1.1.1 Масштабы применения хлора
.2 Методы получения хлора
.2.1 Лабораторные методы получения хлора
В лабораторных условиях хлор получают действием
различных окислителей на соляную кислоту, например:
МnО2 + 4НСl = МnСl2 + Сl2↑ + 2Н2О
(1.2.1.1)
Еще более эффективно окисление проводится такими
окислителями, как РbО2, КМnО4, КСlO3, К2Сr2О7 [2]. Или перманганатом калия на
соляную кислоту [1]:
KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑
+8H2O (1.2.1.2)
Так же хлор можно получить термическим
разложением хлорида меди:
CuCl2 = 2CuCl + Cl2↑ (1.2.1.3)
Однако в промышленных масштабах хлор получают
электрохимическим способом. В результате электролиза раствора соли получают
хлор и каустическую соду. Чаще всего используют хлорид натрия NaCl, однакотакже
можно применять хлорид калия KCl [3].
2NaCl + 2H2O = Cl2 ↑ + 2NaOH
+H2 ↑ (1.2.1.4)
В основе электрохимической технологии лежит
процесс электролиза водного раствора NaCl .
.2.2 Основы электролиза
Электролиз - совокупность электрохимических
окислительно-восстановительных процессов, происходящих при прохождении
электрического тока через электролит с погруженными в него электродами. На
катоде катионы восстанавливаются в ионы более низкой степени окисления или в
атомы, например:
Feі+ + e- = FeІ+ (1.2.2.1)
СuІ+ + 2е- = Сu (1.2.2.2)
Нейтральные молекулы могут участвовать в
превращениях на катоде непосредственно или реагировать с продуктами катодного
процесса, которые рассматриваются в этом случае как промежуточные вещества
электролиза. На аноде происходит окисление ионов или молекул, поступающих из
объема электролита или принадлежащих материалу анода; в последнем случае анод
растворяется или окисляется. Например:
OH- + 4e- = 2H2O + O2 (1.2.2.3)+ + 3OH- +H2O =
CrO42- + 5H+ + 3e- (1.2.2.4)
Электролиз включает два процесса: миграцию реагирующих частиц под действием электрического поля к поверхности электрода и переход заряда с частицы на электрод или с электрода на частицу. Миграция ионов определяется их подвижностью и числами переноса. Процесс переноса нескольких электрических зарядов осуществляется, как правило, в виде последовательности одноэлектронных реакций, то есть постадийно, с образованием промежуточных частиц (ионов или радикалов), которые иногда существуют некоторое время на электроде в адсорбированном состоянии.
Скорости электродных реакций зависят от состава и концентрации электролита, материала электродов, электродного потенциала, температуры, гидродинамических условий. Мерой скорости служит плотность тока - количество переносимых электрических зарядов через единицу площади поверхности электрода в единицу времени. Количество образующихся при электролизе продуктов определяется законами Фарадея [4]. Согласно 1-му закону, масса вещества т, прореагировавшего в процессе электролиза, прямо пропорциональна силе тока I и времени электролиза t, то есть количеству пропущенного электричества Q = I*t (предполагается, что I не зависит от t; в противном случае масса т пропорциональна t1∫t2J*dt, где t1 и t2 - моменты включения и выключения тока). Согласно 2-му закону, для разных электродных процессов при одинаковом количестве пропущенного электричества Q массы прореагировавших веществ относятся друг к другу так же, как эквиваленты химические этих веществ. Оба закона Фарадея объединяются одним уравнением:
=(1/F)*Q*M/z , (1.2.2.5)
где M - молярная масса вещества, участвующего в электролизе, z - число элементарных зарядов, соответствующее превращению одной молекулы этого вещества, 1/F - коэффициент пропорциональности, общий для всех веществ, F - постоянная Фарадея, равная 96484,56 Кл/моль [5].
Для выделения 1 грамм-эквивалента вещества на электроде необходимо количество электричества, равное 26,8 А* ч. Если на каждом из электродов одновременно образуется несколько продуктов в результате ряда электрохимических реакций, доля тока (в %), идущая на образование продукта одной из реакций, называется выходом данного продукта по току.
В электродном процессе участвуют вещества,
требующие для переноса заряда наименьшего электрического потенциала. Это могут
быть не те вещества, которые обуславливают перенос электричества в объеме
раствора. Например, при электролизе водного раствора NaCl в миграции участвуют
ионы Na+ и Сl-, однако на твердых катодах ионы Na+ не разряжаются, а протекает
энергетически более выгодный процесс разряда протонированных молекул воды [4]:
Н3О+ + е- = 1/2H2 + Н2О (1.2.2.6)
В промышленности процесс электролиза проводится
в специальных аппаратах - электролизерах.
1.2.3 Устройство электролизера
Конструкция промышленных аппаратов для проведения электролитических процессов определяется характером процесса. В гидрометаллургии и гальванотехнике используют преимущественно так называемые ящичные электролизеры, представляющие собой открытую емкость с электролитом, в которой размещают чередующиеся катоды и аноды, соединенные соответственно с отрицательным и положительным полюсами источника постоянного тока. Для изготовления анодов применяют графит, углеграфитовые материалы, платину, оксиды железа, свинца, никеля, свинец и его сплавы; используют малоизнашивающиеся титановые аноды с активным покрытием из смеси оксидов рутения и титана (оксидные рутениево-титановые аноды), а также из платины и ее сплавов. Для катодов в большинстве электролизеров применяют сталь, в том числе с различными защитными покрытиями с учетом агрессивности электролита и продуктов электролиза, температуры и других условий процесса. Некоторые электролизеры работают в условиях высоких давлений, например: разложение воды ведется под давлением до 4 МПа. В современных электролизерах широко применяют пластичные массы, стекло и стеклопластики, керамику.
Во многих электрохимических производствах требуется разделение катодного и анодного пространств, которое осуществляют с помощью диафрагм, проницаемых для ионов, но затрудняющих механическое смешение и диффузию. При этом достигается разделение жидких и газообразных продуктов, образующихся на электродах или в объеме раствора, предотвращается участие исходных, промежуточных и конечных продуктов электролиза в реакциях на электроде противоположного знака и в приэлектродном пространстве. В пористых диафрагмах через микропоры переносятся как катионы, так и анионы в количествах, соответствующих числам переноса. В ионообменных диафрагмах (мембранах) происходит перенос либо только катионов, либо анионов, в зависимости от природы входящих в их состав ионогенных групп. При синтезе сильных окислителей используют обычно бездиафрагменные электролизеры, но в раствор электролита добавляют К2Сr2О7. В процессе электролиз на катоде образуется пористая хромит-хроматная пленка, выполняющая функции диафрагмы. При получении хлора используют катод в виде стальной сетки, на которую наносят слой асбеста, играющий роль диафрагмы. В процессе электролиза рассол подают в анодную камеру, а из анодной камеры выводят раствор NaOH.
Электролизер, применяемый для получения магния, алюминия, щелочных и щелочно-земельных металлов, представляет собой футерованную огнеупорным материалом ванну, на дне которой находится расплавленный металл, служащий катодом, аноды же в виде блоков располагают над слоем жидкого металла. В процессах мембранного получения хлора, в электросинтезе используют электролизеры фильтр-прессного типа, собранные из отдельных рам, между которыми помещены ионообменные мембраны.
По характеру подключения к источнику питания
различают монополярные и биполярные электролизеры (рис. 1.2.3.1). Монополярный
электролизер состоит из одной электролитической ячейки с электродами одной
полярности, каждый из которых может состоять из нескольких элементов,
включенных параллельно в цепь тока. Биполярный электролизер имеет большое число
ячеек (до 100-160), включенных последовательно в цепь тока, причем каждый
электрод, за исключением двух крайних, работает одной стороной как катод, а
другой как анод. Монополярные электролизеры обычно рассчитаны на большой ток и
малые напряжения, биполярные - на сравнительно небольшой ток и высокие
напряжения. Современные электролизеры допускают высокую токовую нагрузку:
монополярные до 400-500 кА, биполярные эквивалентную 1600 кА [4].
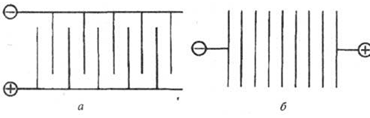
Рис. 1.2.3.1 Виды электролизеров по характеру
подключения к источнику питания
.2.4 Промышленные способы получения хлора
В настоящее время хлор вырабатывается тремя электрохимическими методами, два из которых представляют собой электролиз с твердым катодом: диафрагменный и мембранный методы. Третий метод - электролиз с жидким ртутным катодом. В ряду электрохимических методов производства самым легким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути [1].
Для новых производственных мощностей предпочитают использовать мембранный процесс, поскольку он более экономичен, более безопасен для окружающей среды и дает возможность получить конечный продукт более высокого качества.
В технологии с использованием диафрагменного
электролизера солевой рассол подают в первую камеру (рис. 1.2.4.1), в которой
установлен титановый анод с покрытием из солей рутения и других металлов. У
верхней пластиковой стенки электролизера скапливается тепло и влажный
газообразный хлор, получаемый на аноде.
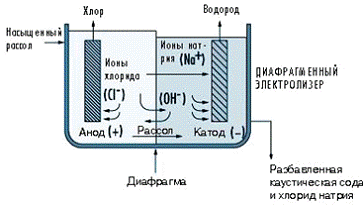
Рис. 1.2.4.1 Схема диафрагменного электролизера
С помощью всасывающего насоса хлор подают в коллектор для дальнейшей обработки, состоящей из процесса охлаждения, сушки и сжатия газа. Воду и не вступивший в реакцию рассол отводят через пористый диафрагменный сепаратор в камеру, где расположен катод и где в результате взаимодействия воды и стального катода образуется гидрохлорид натрия (каустическая сода) и водород. Диафрагма разделяет хлор, полученный в анодной камере, и гидрохлорид натрия, полученный на катоде. Эти два вещества, вступая в соединение, образуют хлорную известь или хлорат натрия. Чаще всего диафрагму изготавливают из асбеста и фторполимера. При производстве хлора в диафрагменных электролизерах слабый раствор гидроокиси натрия содержит не вступившую в реакцию соль. Следовательно, для получения каустической соды нужной концентрации требуется дополнительный процесс выпаривания и удаление большей части соли, чтобы получить каустическую соду стандартного качества.