Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО
тема 23. аміни. амінокислоти. білки
Добування амінокислот
Основний спосіб добування амінокислот — заміщення атома галогену на аміногрупу в галогенозамінених кислотах. Цей спосіб аналогічний до добування амінів з алкілгалогенів та аміаку. Галогеноводень, який виділяється при заміщенні, зв’язують надлишком аміаку:
Cl − CH(R)− COOH + 2NH3 → H2N − CH(R)− COOH + NH4Cl.
Амінокислоти застосовують як лікувальні засоби при нервових захворюваннях, в тваринництві. Амінокапронова і аміноенантова кислоти застосуються для одержання синтетичних волокон.
БілКи. Білки (білкові речовини) — макромолекулярні природні сполуки (біополімери), структурну основу яких становлять поліпептидні ланцюги, побудовані із залишків α -амінокарбонових кислот. Білки неодмінно містять елементи C, H, N та O, майже завжди S, часто P, рідше Fe, Cu, Zn тощо.
За складом білки поділяють на:
—протеїни — прості білки, що складаються із залишків амінокислот;
—протеїди — складні білки, що складаються із залишків амінокислот та різних небілкових речо-
вин.
Будова білків
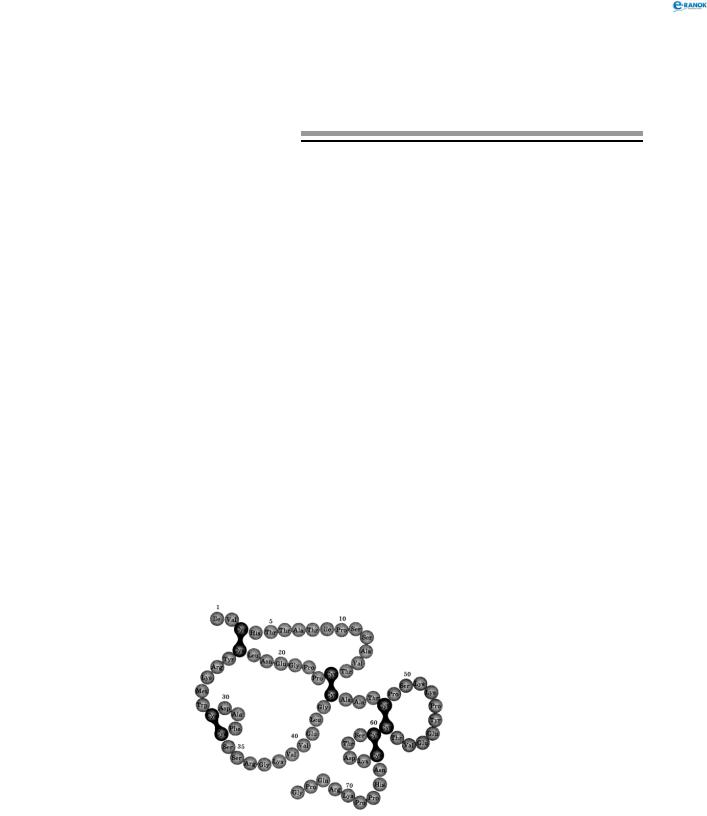
У складі білків зустрічаються залишки 20 амінокислот. Властивості білків залежать не тільки від того, які амінокислотні залишки утворюють їх, але і від того, в якій послідовності вони з’єднуються одна з одною. Таку послідовність називають первинною структурою білка:
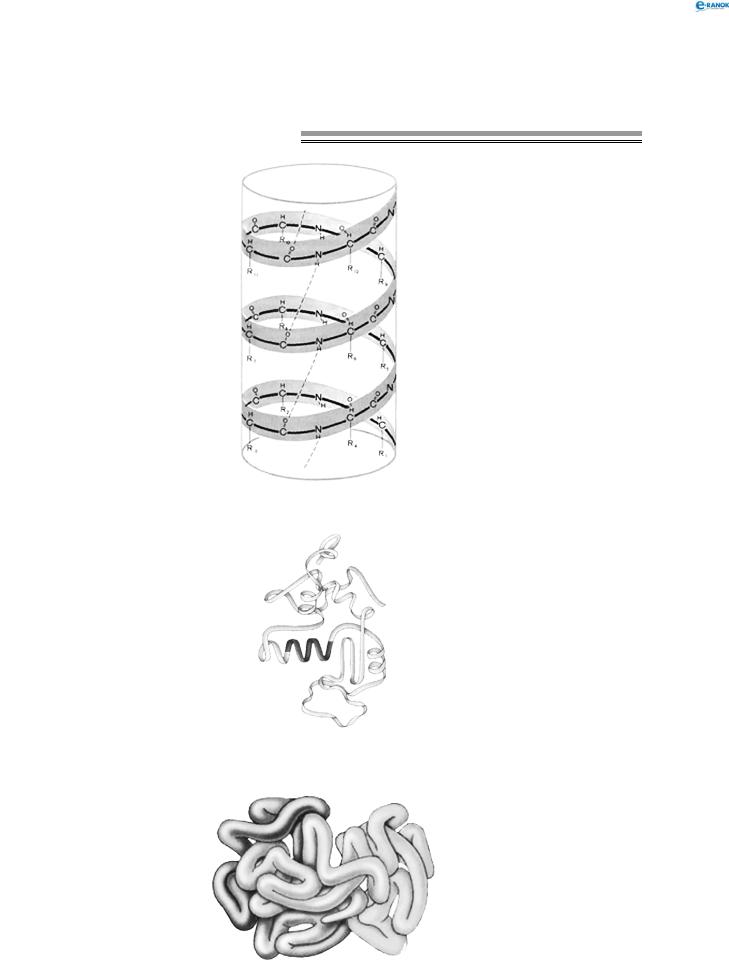
Поліпептидний ланцюг зазвичай згорнутий у спіраль, що має певну просторову структуру — α -спіраль:
160
www.e-ranok.com.ua
тема 23. аміни. амінокислоти. білки
Спіраль у свою чергу може приймати певну просторову будову, що є власною для кожного білка: спіраль згортається в клубок (глобулу). Таку будову називають третинною структурою білка:
Для деяких білків є характерним об’єднання декількох клубків (субодиниць) в одну частинку, що обумовлює четвертинну структуру білків:
161
www.e-ranok.com.ua

тема 23. аміни. амінокислоти. білки
До складу таких об’єднань можуть входити йони металів або інші речовини небілкової природи. Так, молекула білка гемоглобіну складається з чотирьох субодиниць, з’єднаних з йоном Феруму, що дозволяє такій молекулі переносити кисень і вуглекислий газ у тваринному організмі.
хімічні властивості білків
1. Денатурація білків.
Унаслідок дії деяких факторів відбувається руйнування тривимірної конформації білка — денатурація, пов’язане зі зміною вторинної, третинної та четвертинної структур; ця зміна може мати тимчасовий або постійний характер, але й у тому, і в іншому випадку амінокислотна послідовність білка (первинна структура) залишається незмінною.
Денатурація білків відбувається під впливом нагрівання або впливом яких-небудь випромінювань, наприклад інфрачервоного або ультрафіолетового. Сильні кислоти, сильні луги й концентровані розчини солей також спричинюють розрив зв’язків (при тривалому впливі й пептидних).
2. Ренатурація.
Інодіденатурованийбілокзасприятливихумовзновуспонтаннонабуваєсвоєїнативної(природної) структури. Цей процес називають ренатурацією.
3. Гідроліз.
Найважливішою хімічною властивістю білків є їхня здатність до гідролізу, який може протікати при нагріванні із сильними кислотами або з лугами (кислотно-основний гідроліз) і під дією ферментів (ферментативний гідроліз). Гідроліз призводить до розпаду поліпептидних зв’язків
зутворенням вільних амінокислот.
4.Якісні кольорові реакції білків.
а) біуретова реакція на пептидні зв’язки — дія розведеного розчину купрум(ІІ) сульфату на лужний розчин білка, яка супроводжується появою фіолетово-синього забарвлення розчину, що обумовлено комплексоутворенням між йонами Купруму та поліпептидами;
б) ксантопротеїнова реакція на ароматичні й гетероядерні цикли — дія концентрованої нітратної кислоти з появою жовтого забарвлення; забарвлення пояснюється нітруванням циклів й утворенням нітросполук залишками амінокислот;
в) реакція Міллона — дія на білок реактиву Міллона — розчину Hg(NO3 )2 та Hg2 (NO3 )2 у розведеній HNO3, що містить домішку HNO2,— з появою червоно-коричневого забарвлення, яке обумовлене утворенням пептидних солей Меркурію.
Деякі білки виконують транспортні функції — переносять молекули або йони в місця синтезу або накопичення речовин. Наприклад, в крові міститься білок гемоглобін, що переносить кисень до тканин і вуглекислий газ від них, а білок міоглобін накопичує кисень у м’язах.
Білки — це будівельний матеріал клітин. З них побудовані опорні, м’язові, покривні тканини. Білки-рецептори сприймають і передають сигнали, що надходять від сусідніх клітин або з навко-
лишнього середовища. Наприклад, дія світла на сітківку ока сприймає білок родопсин.
Білки життєво необхідні будь-якому організму і тому є найважливішою складовою частиною продуктів харчування. У процесі травлення вони гідролізуються до амінокислот, які служать вихідною сировиною для синтезу інших білків, необхідних даному організму. Існують такі амінокислоти, які організм не в змозі синтезувати сам і одержує тільки з їжею,— їх називають незамінними.
162
www.e-ranok.com.ua

тема 23. аміни. амінокислоти. білки
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
тест 46 (контрольний)
1.Позначте правильне закінчення твердження: «Первинна структура білків — це…»
Апослідовність залишків молекул амінокислот у білковій молекулі
Б амінокислотний склад молекули білка В молекулярна формула білка
Гбудова α-спіралі молекули білка
2.Укажіть функціональні групи, які зумовлюють амфотерні властивості амінокислот.
А –ОН, –SH |
В –NH |
2, –CHO |
Б –NH2, –COOH |
|
Г –NH2, –OH |
3. Визначте клас органічних сполук, для яких характерне утворення біполярних іонів.
А амінокислоти |
В вуглеводи |
Б спирти |
Г естери |
4. Установіть відповідність між структурою молекули білка та характером хімічного зв’язку, що визначає її утворення:
А первинне 1 водневий зв’язок Б вторинне 2 дисульфідні мостики
В третинне 3 міжмолекулярна взаємодія
Гчетвертинне 4 пептидний зв’язок
5.Установіть послідовність утворення речовин у ланцюгу перетворень від ацетилену до аніліну.
А C6H5NH2 |
В C2H2 |
Б C6H6 |
Г C6H5NO2 |
6. У процесі спалювання первинного аміну масою 5,9 г утворюється азот об’ємом 1,12 л (н. у.). Визначте молекулярну формулу аміну. Укажіть суму індексів у формулі.
163
www.e-ranok.com.ua

тема 24. синтетичні високомолекуляРні Речовини і ПолімеРні матеРіали на їх основі
Тема 24. Синтетичні високомолекулярні речовини і полімерні матеріали на їх основі.
Узагальнення знань про органічні сполуки
Перевірте свої знання
Виконайте тест 47. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
тест 47 (вступний)
1. Укажіть, до якого виду волокон належить капрон.
А синтетичні |
В штучні |
Б натуральні |
Г мінеральні |
2. Полімером, що не переробляється в природі мікроорганізмами та забруднює навколишнє середовище, є:
Аполіетилен Б волосся В крохмаль Г целюлоза
3.Укажіть назву реакції, унаслідок якої можна отримати тринітроцелюлозу.
Агідроліз
Б крекінг В естерифікації
Гполімеризація
4.Установіть відповідність між хімічними речовинами, формули яких наведено, та їхнім застосовуванням:
А H2N(CH2)5COOH |
1 |
регуляція водно-сольового обміну |
Б C17H35COONa |
2 |
профілактика карієсу |
В NaF |
3 |
виготовлення мила |
Г KCl |
4 |
виготовлення капронового волокна |
5. Установіть генетичний ланцюг утворення нітробензолу: |
||
А C6H5NO2 |
В CH≡CH |
|
Б C6H6 |
Г CaC2 |
|
6. Яку масу тетрафторетилену (F2C=CF2) (т) можна добути з хлороформу (СНСl3) масою 300 т із масовою часткою домішок 7%, якщо масова частка виходу тетрафторетилену становить 98% теоретично можливого?
164
www.e-ranok.com.ua