Материал: Агрегативная устойчивость золей наноалмазов, модифицированных катионами металлов
В результате такой очистки содержание металлических примесей в ДНА снижается до 0,9 маc. %, а содержание основного вещества повышается до 98,5 маc. %.
Предложенный авторами [9] способ химической очистки многостадиен, сложен в исполнении, дорог, отходы - чрезвычайно токсичны.
Окислительные системы на основе азотной кислоты или перекиси водорода при сбалансированном соотношении всех компонентов и соответствующих технологических режимах эффективно и в одну стадию окисляют до 99 % неалмазного углерода и переводят в растворимое состояние до 90 % неуглеродных примесей. Продукты реакций окисления имеют в основном газообразный характер.
Главным достоинством окислительных систем на основе азотной и серной кислот являются их доступность и дешевизна, а также простота аппаратурно-технологического решения процесса [11]. Недостатками данного способа является большой расход кислот - до 57 кг на 1 кг АШ, сложность регенерации и утилизации многокомпонентной смеси, загрязнение поверхности ДНА соединениями серы и азота.
Переход к водным растворам азотной кислоты успешно решает эти проблемы, причем качество очистки наноалмаза при этом принципиально улучшается, так как исключается образование серосодержащих производных на поверхности алмаза [12-14]. Процесс ведется при повышенном давлении; для изготовления аппаратуры, работающей при высокой температуре, требуется применение специальных коррозионностойких материалов.
С химической точки зрения очень привлекательным окислителем является перекись водорода: продукты ее взаимодействия с углеродом - только углекислый газ и вода [15]. При этом формируется специфическая поверхность алмазного материала, не содержащая ни сульфо-, ни нитропроизводных. Очистка ДНА окислительными системами на основе перекиси водорода существенно упрощает инфраструктуру процесса, в первую очередь систему экологической защиты и утилизации отходов.
Недостатками такого привлекательного процесса являются: необходимость использовать аппаратуру, работающую под давлением; недостаточная полнота удаления неалмазного углерода; а главное - полная невозможность удаления несгораемых примесей.
Наиболее простым и доступным окислителем является кислород воздуха. Этот окислитель известен в процессах газообразной очистки синтетических алмазов [7]. Авторам работы [10] удалось, используя особенности детонационной шихты, провести селективное окисление неалмазного углерода путем пропускания воздуха через водную суспензию шихты в присутствии катализаторов. При этом сохраняются все преимущества жидкофазных способов очистки наноалмазов. Правда, недостатки этого способа - те же, что и в случае очистки ДНА перекисью водорода.
.2 Образование двойного электрического слоя на поверхности частиц
Обычно частицы дисперсной фазы в жидкой среде несут на своей поверхности электрический заряд и двойной электрический слой (ДЭС). Различают три возможных механизма образования двойного электрического слоя:
¾ образование двойного электрического слоя в результате перехода ионов (диссоциации) или электронов (ионизации) из одной фазы в другую. При поверхностной ионизации с поверхности металла в газовую фазу переходят электроны, создавая электронное облако со стороны газовой фазы. Количественной характеристикой такого перехода может служить работа выхода электрона. В результате поверхность металла приобретает положительный заряд, а газовая фаза − отрицательный. Возникший электрический потенциал на границе раздела фаз препятствует дальнейшему переходу электронов: наступает равновесие, при котором положительный заряд поверхности металла скомпенсирован отрицательным зарядом, созданным электронами в газовой фазе, т.е. формируется двойной электрический слой.
¾ двойной электрический слой может образоваться при избирательной адсорбции ионов электролита из раствора.
¾ образование двойного электрического слоя вследствие ориентирования полярных молекул сопряженных фаз в результате их взаимодействия. Если в формировании двойного электрического слоя не принимают участие электролиты, для определения знака заряда на поверхности можно воспользоваться правилом Кёна. Согласно этому правилу из двух соприкасающихся фаз положительно заряжается фаза, имеющая большую диэлектрическую проницаемость. Именно поэтому многие вещества, находящиеся в контакте с водой, имеющей большую диэлектрическую проницаемость, заряжаются отрицательно.
Объекты коллоидной химии часто имеют непроводящую дисперсную фазу (золи и грубодисперсные суспензии нерастворимых солей, оксидов, гидроксидов, эмульсии) и для них наиболее характерно образование ДЭС по адсорбционному механизму, который предполагает возникновение на межфазной поверхности поверхностный избыток ионов определенного знака.
Образование ДЭС на межфазных поверхностях, как и адсорбция, является результатом взаимодействия соприкасающихся фаз благодаря избыточной поверхностной энергии. Стремление гетерогенной системы к уменьшению поверхностной энергии вызывает определенное ориентирование полярных молекул, ионов и электронов в поверхностном слое, вследствие чего соприкасающиеся фазы приобретают заряды противоположного знака, но равной величины. В результате на поверхности возникает двойной электрический слой.
В лиозолях дисперсных твердых частиц ионы способны переходить на поверхность из раствора или с поверхности частиц в раствор в зависимости от соотношения их химических потенциалов. Образовавшийся в результате двойной электрический слой состоит из слоя ионов, определяющих заряд поверхности - потенциалопределяющих ионов, и слоя противоположно заряженных ионов - противоионов.
Слой противоионов состоит из двух частей. Плотная часть -адсорбционный слой (слой Гельмгольца) примыкает непосредственно к межфазной поверхности; его толщина равна радиусу сольватированных ионов, его составляющих. Другая часть противоионов находится в диффузной части, толщина которого зависит от свойств и состава системы.
Частицу дисперсной фазы вместе с двойным электрическим слоем называют мицеллой. Внутреннюю часть мицеллы составляет агрегат атомов или молекул основного вещества. Агрегат вместе с расположенными на поверхности потенциалопределяющими ионами образует ядро мицеллы. Ядро с противоионами плотной части ДЭС составляет гранулу, которую окружают противоионы диффузного слоя. Мицелла в отличие от гранулы электронейтральна.
Смещение
фаз в дисперсной системе относительно друг друга, вызванное внешними силами,
вызывает разрыв двойного слоя по плоскости скольжения. Плоскость скольжения
проходит в диффузном слое, и часть его ионов остается в дисперсионной среде. В
результате дисперсионная среда и дисперсная фаза оказываются противоположно
заряженными. Потенциал, возникающий на плоскости скольжения при отрыве части
диффузного слоя, называется электрокинетическим потенциалом или ![]()
![]() потенциалом.
потенциалом.
Электрокинетический потенциал, отражая свойства ДЭС, характеризует природу фаз и межфазного взаимодействия и зависит от скорости движения фаз и вязкости среды [16].
Теория, рассматривающая устойчивость и коагуляцию лиофобных систем как результат совокупного действия молекулярных (вандерваальсовых) сил притяжения и электростатических сил отталкивания между частицами, называется теорией Дерягина - Ландау - Фервея - Овербека - теорией ДЛФО. В зависимости от баланса этих сил в тонкой прослойке жидкости (межфазной пленке) между сближающимися частицами возникает либо положительное расклинивающее давление (отталкивание), препятствующее их соединению, либо отрицательное расклинивающее давление (притяжение), приводящее к утончению прослойки и образованию контакта между частицами.
Если в системе происходит образование двойного электрического слоя, то при сближении двух частиц на такое расстояние, при котором диффузные части двойных слоев перекроются, произойдет вытеснение части противоионов в раствор. Образовавшиеся одноименно заряженные частицы отталкиваются. Силы отталкивания убывают с увеличением расстояния между частицами по экспоненциальному закону.
.3 Физико-химические свойства ДНА производства РФЯЦ-ВНИИТФ (ТУ 2-037-677-94)
Из литературных данных известны физико-химические свойства ДНА производства РФЯЦ-ВНИИТФ. В работе [17] приведены характеристики трех фракций порошка - осаждаемой (1), промежуточной (2) и взвешенной (3). Данные приведены в таблице 1.
Таблица 1 - Основные физико-химические показатели выделенных фракции
Параметр
Фракция 1
Фракция 2
Фракция 3
Диапазон размеров, нм
250-7000
100-250
5-100
Внешний вид
Светло серый легко
рассыпающийся порошок
Серый порошок
Черные кристаллоподобные
образования
Параметр
Фракция 1
Фракция 2
Фракция 3
Пикнометрическая плотность,
ρ·10-3 кг/м3
3,3
3,2
3.1
Несгораемый остаток [Н.о.],
мас. %
1.6
1,3
0,9
Окисляемый углерод [CОК], маc. %
1,0
1.5
1.9
Вязкость водной суспензии
ДНА, мПа·с, при [ДНА]= 10 кг/м3 [ДНА]= 60 кг/м3
1,04 1,32
1.07 1,63
1,12 5,15
Электрокинетический
потенциал, мВ
+16
+32
+39
Удельная поверхность, Сорбционная емкость по
бензолу, Исследования
агрегативной устойчивости золей таких ДНА остаются актуальными вследствие их
практических применений.
Объектом исследования в данной работе были гидрозоли наноалмазов,
полученные ультразвуковой обработкой порошка в течение 3 минут. Диспергирование
проводилось на источнике стержневого типа УЗДН-А с частотой 22кГц, концентрация
ДНА в гидрозоле составляла 0,1 массовый процент. В исследуемых гидрозолях
использовались ДНА, очищенные хромовой смесью, производства РФЯЦ-ВНИИТФ.
Содержание хрома на поверхности данных наноалмазов по данным
атомно-абсорбционной спектроскопии составляло 0,7%. Размерные
характеристики ДНА производства РФЯЦ-ВНИИТФ, определенные с помощью
дисковой центрифуги CPS 24000, приведены в таблице 2
(данные получены Чульмяковой Д.А.).
Таблица 2 - Размерные характеристики ДНА производства
РФЯЦ-ВНИИТФ (Dn - среднечисленный диаметр, Dw - средневесовой диаметр, Dw/Dn - индекс полидисперсности, CVDn - коэффициент вариации численный)
Dn, нм
Dw, нм
Dw/ Dn
CVDn, %
Весовая доля фракции с
размерами >50 нм
Весовая доля фракции с
размерами <20 нм
ДНА
14,0
26,9
1,9
33,2
12,7
54,4
В данной работе диспергирование порошков в воде проводилось на источнике
стержневого типа УЗДН-А с частотой 22 кГц (рис.1).
УЗДН-А представляет собой компактную настольную ультразвуковую установку
универсального применения. Прибор прост и удобен в эксплуатации и не требует
специальной подготовки при эксплуатации и обслуживании.
Диспергатор ультразвуковой УЗДН-А позволяет препарировать объекты из
кристаллических, порошкообразных, волокнистых и других веществ и наносить их на
пленку-подложку при электронномикроскопическом методе исследования.
УЗДН-А может быть использован: для приготовления суспензий и эмульсий из
различных веществ; для отмывки мелких деталей от механических загрязнений; для
экспериментальных работ по изучению воздействия ультразвука на различные
процессы.
Рисунок 1 - Ультразвуковой диспергатор стержневого типа УЗДН-А
Возможности и особенности диспергатора: ¾ исключение загрязнения диспергируемой среды материалом
насадки
¾ низкий акустический шум
¾ автоматическая подстройка частоты генератора
¾ предотвращение агрегации частиц при нанесении объекта на
пленку-подложку
¾ автоматическое выключение по истечении заданного времени.
Электрические колебания частотой 22 кГц, генерируемые транзисторным
генератором блока питания, преобразуются пъезострикционным преобразователем
излучателя в механические упругие колебания соответствующей частоты, которые
воздействуют на диспергируемую среду.
Диспергатор выполнен в виде настольной установки и конструктивно
представляет собой стойку, в которой размещены блок питания и шумозащитная
камера, стенки и дверка которой армированы звукоизоляционным материалом. На
вертикальной стенке внутри камеры закреплен штатив для установки и перемещения
рабочего излучателя.
Концентратор излучателя имеет выход под резьбу, что позволяет
устанавливать на него рабочие насадки различной конструкции, которыми
комплектуется диспергатор, обеспечивая его широкое использование
Диспергатор оснащен таймерным устройством с автоматической выдержкой
времени диспергирования.
Технические характеристики представлены в таблице 2.
Таблица 2 - Технические характеристики звукового диспергатора УЗДН-А
Рабочая частота, кГц
22±1,65
Амплитуда колебаний
рабочего торца излучателя с конической насадкой, мм, не более
20
Диапазон автоматической
выдержки длительности диспергирования, сек (минимум)
1 - 99
Питание от однофазной сети переменного
тока: напряжение (В), частота (Гц)
220, 50
Потребляемая мощность, Вт
300
Габаритные размеры, мм
390×260×540
Масса, кг
35
Электрофорезом называют перемещение частиц дисперсной фазы в жидкой или
газообразной среде по действием внешнего электрического поля. Это явление можно
наблюдать в седиментационно устойчивых дисперсных системах. При наложении на
такую систему внешней разности потенциалов происходит разрыв диффузной части
ДЭС по плоскости скольжения, в результате чего образуется комплекс дисперсная
частица + часть противоионов внешней обкладки. Так как поверхностный заряд
частицы в таком случае не полностью скомпенсирован противоионами, такой
комплекс несет электрический заряд и во внешнем электрическом поле перемещается
к соответствующему электроду.
Скорость
движения частиц дисперсной фазы при электрофорезе где
Методика измерения электрофореза сводится к непосредственной регистрации
скорости перемещения границы золя с индифферентным электролитом в
градуированной U-образной трубке.
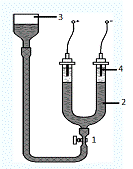
Схема прибора для измерения электрофоретической скорости представлена на
рисунке 2.
В качестве индифферентного электролита был выбран хлорид калия (KCl) с концентрациями
Проводимость
в золе НА и в фоновом электролите была одинаковой.
Рисунок
2 - Схема прибора для измерения скорости электрофореза методом подвижной
границы: 1- кран; 2 - U-образная трубка; 3 - тонкая трубка с расширяющимся
горлом; 4- электроды.
Водородный показатель рН - это десятичный логарифм концентрации
водородных ионов, взятый с обратным знаком: pH = -lg[H+],
где [H+] -
концентрация ионов водорода. Соответственно, при диссоциации с твердой
поверхности ионов водорода уменьшается величина показателя рН суспензии по
сравнению с чистой дисперсионной средой, например, с водой. Такие поверхности
имеют кислотный характер. Постоянное значение ионного произведения воды Kв при постоянной температуре можно приближенно выразить
произведением [H+]×[ОH-]. Соответственно при 25°С и Kв » 10-14 величина рН =
14-рОН. Если противоионами являются гидроксил-анионы ОН-, величина рН суспензии становится
выше, чем в чистой дисперсионной среде. Такие поверхности имеют основной
характер.
Для измерения рН растворов используют принцип потенциометрических
измерений. В основу потенциометрических измерений положена прямая
потенциометрия - измерение электродвижущей силы (ЭДС) гальванического элемента
ионоселективных электродов и преобразование её в значения рН (рХ), М и С.
Потенциометрические измерения проводятся несколькими методами. Работа
рН-метра марки Анион 4100, используемого в данной работе, основана на методе
градуировочного графика.
Метод градуировочного графика заключается в построении графика
зависимости ЭДС ионоселективных электродов от концентрации буферных растворов с
известными значениями рН (рХ). Градуировочный график строится прибором
автоматически на основе введённых в его память значений ЭДС ионоселективных
электродов в буферных растворах и соответствующих им значений рН (рХ).
рН (рХ) анализируемого раствора находится по измеренному в нём значению
потенциала ионоселективных электродов.
Метод рН-метрии широко используется для определения кислотности
поверхности твердых веществ (прежде всего оксидов) и практикуется для целей
рационального выбора материалов в различных сферах. Кинетическое изменение
величины рН водной среды отражает характер изменения поверхностной кислотности
образца в процессе его взаимодействия с водой.
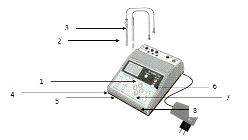
Конструкция рН-метра представлена на рисунке 3. рН-метр
состоит из преобразователя ЭДС и штатива для установки электродов, датчика
температуры и сосуда с раствором. Общий вид преобразователя и элементы его
конструкции показаны на рисунке.
Рисунок 3 - Внешний вид рН-метра, электрода и датчика температуры: 1 -
клавиатура; 2 - ионоселективный электрод; 3 - датчик температуры;
4 - кнопка градуировка; 5 - кнопка измерение ; 6 - кнопка вкл/выкл; 7 - кнопки
стрелки; 8 - кнопка ввод.
Для наноалмазов, произведенных РФЯЦ-ВНИИТФ, методом макроэлектрофореза
был определен заряд частиц и средние расстояния, на которые переместилось
положение границы золя с раствором в каждом колене с электродами противоположного
знака. Заряд частиц положительный, что объясняется тем, что потенциалопределяющими ионами
являются катионы хрома. Для ДНА была определена электрофоретическая скорость
движения частиц за время t=300 секунд. В таблице 3 приведены данные измерений для двух параллельных опытов и
двум границам: нисходящей и восходящей.
Линейную скорость движения частиц при электрофорезе определяли по
формуле:
где
Таблица
3 - Зависимость электрофоретической скорости от концентрации индифферентного
электролита
Концентрация электролита С,
М
5· h, мм
4,25±0,01
5,00±0,01
6,00±0,05
3,75±0,05
Из
таблицы 3 видно, что увеличение концентрации индифферентного электролита от Были
проведены расчеты электрокинетических характеристик наноалмазов -
электрокинетического потенциала и толщины диффузного слоя.
Толщина
диффузного слоя по аналогии с ионной атмосферой из теории Дебая и Гюккеля
зависит от ионной силы раствора I, равной полусумме произведений концентрации на
квадрат заряда ионов: I = 1/2Scoi Zi2. В общем виде можно записать:
λ=1/ где F - число Фарадея,
R -
газовая постоянная,
eeo - то же, что и в формуле (1).
Для расчётов величины электрокинетического потенциала использовали формулу
Духина-Дерягина для частиц ионитов [20]:
η, Е - то же, что и в формуле (1);
ε0 - диэлектрическая проницаемость
среды;
T -
температура среды;
(В
данной формуле учитывается поляризация двойного электрического слоя;
электрофоретическая подвижность не зависит от размера частиц и полидисперсность
не мешает определению электрокинетического потенциала [20].) Значения
рассчитанных величин приведены в таблице 4 и на рисунке 4.
Таблица 4 - Значение параметров ДЭС в зависимости от концентрации
электролита
Концентрация электролита С,
М
5· 50,40±0,10
60,48±0,50
39,64±0,53
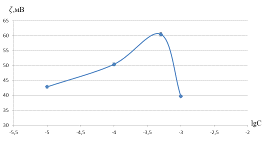
Рисунок 4 - Зависимость величины электрокинетического потенциала от
концентрации электролита
В соответствии с экстремальным характером зависимости электрофоретической
скорости от концентрации электролита полученная кривая также имеет немонотонный
характер. В общем случае, увеличение концентрации электролита должно приводит к
сжатию ДЭС и соответственно к падению электрокинетического потенциала, однако
наличие гидратных слоев на поверхности частиц может влиять на характер
зависимости.
В рамках теории ДЛФО был проведен расчет суммарной энергии молекулярного
притяжения и электростатического отталкивания частиц наноалмазов. Энергию
молекулярного притяжения частиц наноалмазов рассчитывали по уравнению Гамакера:
где
А Энергию
электростатического отталкивания частиц в растворах хлорида калия можно
определить по уравнению Маккартни - Левина [22]:
где
/ Полученные в результате расчетов потенциальные кривые взаимодействия
частиц приведены на рисунке 5.
Рисунок 5 - Потенциальные кривые парного взаимодействия частиц в
растворах хлорида калия
Для проверки предположения о влиянии наличия поверхностных гидратных
слоев на агрегативную устойчивость гидрозолей ДНА были проведены расчеты
суммарной энергии взаимодействия частиц с учетом гидратных слоев. Энергию
взаимодействия частиц, обусловленную действием сил структурного отталкивания,
определяемых наличием гидратных слоев, рассчитывали по уравнению:
Us = pal2K exp (-h/l), (7)
где K и l - эмпирические параметры, связанные с состоянием
ориентационной упорядоченности дипольных молекул воды и соответствующей длиной
корреляции, К = 2×106 н/м2 и l = 10-9 м для алмазных дисперсий [23]. Кривые
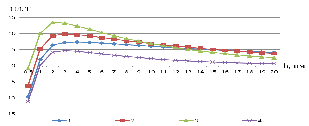
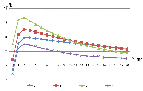
суммарного взаимодействия частиц приведены на рисунке 6.
Рисунок
6 - Потенциальные кривые парного взаимодействия частиц с учетом структурных
сил: 1 - ????= Величины
потенциального барьера, препятствующего агрегации частиц, приведены в таблице
5.
Таблица
5 - Зависимость величины потенциального барьера от концентрации индифферентного
электролита
Концентрация
индифферентного электролита С, М
Величина потенциального
барьера Величина потенциального
барьера В гидрозолях исследованных наноалмазов потенциальный барьер,
препятствующий агрегации частиц и обусловленный электростатическими силами, с
ростом концентрации индифферентного электролита сначала увеличивается, а затем
уменьшается. Как видно из таблицы 4, структурные силы значительно влияют на высоту потенциального
барьера, следовательно, причины немонотонной
зависимости потенциального барьера от концентрации наноалмазов могут быть
связаны с гидратацией частиц наноалмазов. Эта гидратация называется «вторичной»
гидратацией поверхности и связана с адсорбцией потенциалопределяющих ионов (в
данном случае катионов хрома).
Гидратация частиц наноалмазов зависит от гидролиза ионов
хрома, в свою очередь определяемого величиной рН системы.
Поверхностные
соединения состава Добавление
хлорида калия (ионов В
соответствии с изменением гидролиза изменяется и гидратированность частиц
наноалмазов, влияющая на величину определяемого электрокинетического
потенциала.
Измерения
электрофоретической скорости в зависимости от величины рН золей, варьируемой
добавлением растворов хлористоводородной кислоты и гидроксида калия, позволили
рассчитать соответствующую зависимость величины электрокинетического
потенциала, данные приведены в таблице 6.
Таблица
6 - Зависимость электрокинетического потенциала частиц ДНА от рН золей
рН раствора
2,40
4,50±0,15
3,70
30,50±0,53
5,00
43,24±0,10
5,20
45,66±0,10
5,30
46,57±0,50
5,40
44,08±0,53
6,40
47,10±0,50
7,00
46,01±0,15
Из данных таблицы 6 следует, что в интервале рН, соответствующему этим
величинам в золях ДНА в присутствии растворов хлорида калия, зависимость
электрокинетического потенциала проходит через экстремум. Немонотонный характер
зависимости электрокинетического потенциала частиц ДНА (полученных с помощью
очистки хромовой смесью), от величины рН золей согласуется с данными работы
[24]. Следует отметить, что увеличение значения
электрокинетического потенциала с ростом pH в кислой области объясняется
уменьшением сжатия двойного электрического слоя со снижением ионной силы
раствора.
Некоторое уменьшение величины потенциала при pH > 5 может
происходить в силу двух причин: диссоциации протоногенных карбоксильных групп и
понижения положительного заряда потенциалопределяющих ионов вследствие
протекания гидролиза ионов хрома. Обращает на себя внимание слабая связь между
величиной электрокинетического потенциала и устойчивостью золей ДНА
производства РФЯЦ-ВНИИТФ, а также различная чувствительность к добавлению
электролита в кислой области рН и нейтральной и щелочной средах. Золи ДНА
седиментационно устойчивы в кислой области при рН > 2 и СKCl £ 0,5×10-2 М. В
нейтральной и слабощелочной областях до рН £ 8 золь обратимо
коагулирует при СKCl ³ 10-3 М. При
рН > 8 коагуляция золя происходит уже при СKCl = 10-4
М. Модифицирование ДНА ТУ 3974-001-10172699-94 катионами никеля
проводили ранее в лаборатории Отдела молекулярной электроники КНЦ СО РАН.
Содержание никеля в полученных образцах модифицированных наноалмазов (МНА)
составило 2.9 мас%.
Измерения методом макроэлектрофореза показали, что
электрофоретическая подвижность частиц МНА практически равна нулю (в отличие от
ДНА, модифицированных катионами хрома).
В соответствии с отсутствием электростатического фактора
устойчивости гидрозоли МНА обладают пониженной агрегативной и седиментационной
устойчивостью, в отличие от ДНА, модифицированных катионами хрома. Агрегаты МНА
имеют рыхлое строение, что обусловлено наличием гидратных слоев на поверхности
частиц. Очевидная причина отличия гидрозолей с частицами, модифицированными
катионами хрома и никеля, связана с различной валентностью катионов.
Трехвалентные иона хрома обеспечивают частицам положительный заряд в
гидрозолях, двухвалентные ионы никеля нейтрализуют поверхностные карбоксильные
группы. При высоких концентрациях электролитов, применяемых для получения КГП,
различие в агрегативном поведении наночастиц будет определяться более развитыми
гидратными слоями на поверхности ДНА, модифицированных катионами хрома.
Размерные характеристики ДНА, модифицированных катионами
никеля приведены в таблице 7.
Таблица 7- Размерные характеристики ДНА, модифицированных
катионами никеля (Dn -
среднечисленный диаметр, Dw - средневесовой диаметр, Dw/Dn - индекс полидисперсности, CVDn - коэффициент вариации численный)
Dn, нм
Dw, нм
Dw/ Dn
CVDn, %
Весовая доля фракции с
размерами >50 нм
Весовая доля фракции с
размерами <20 нм
МНА
16,1
25,0
1,5
20,2
8,3
72,0
В ходе проделанной работы были получены следующие результаты:
¾ установлено, что
потенциалопределяющими ионами на поверхности частиц наноалмазов производства
РФЯЦ-ВНИИТФ являются катионы хрома, что придает частицам положительный заряд в
гидрозолях;
¾ показано, что зависимость электрокинетического потенциала
частиц наноалмазов от концентрации индифферентного электролита имеет
немонотонный характер. Величины электрокинетического потенциала частиц
наноалмазов при концентрациях индифферентного электролита ¾ в гидрозолях исследованных наноалмазов потенциальный
барьер, препятствующий агрегации частиц, с ростом концентрации индифферентного
электролита сначала увеличивается, а затем уменьшается. Причины такой
немонотонной зависимости потенциального барьера от концентрации электролита
связаны с гидратацией частиц наноалмазов;
¾ установлено, что золи ДНА производства РФЯЦ-ВНИИТФ обладают
повышенной агрегативной и седиментационной устойчивостью в кислой области рН,
что объясняется гидратацией ионов хрома. Данные золи можно успешно применять
для получения композиционных гальванических покрытий на основе хрома. При
электрофоретическом способе нанесения покрытий оптимальная область рН
соответствует области с высоким значением электрокинетического потенциала
частиц.
1. Долматов, В. Ю. Современные промышленные
возможности синтеза наноалмазов / В. Ю. Долматов, М. В.
Веретенникова, В. А. Марчуков, В. Г Сущев //
Физика твердого тела - 2004. - Т. 46, № 4. -
С. 596-600.
. Акимова, Л.Н. Детонация взрывчатых
веществ с образованием алмаза / Л.Н. Акимова, С.А. Губин, В.В. Одинцов, В.И.
Пепекин // Докл. V Всесоюз. совещ. по детонации, Красноярск, 1991. - Т. 1, - С.
14-19.
3. Губин, С.А. Диаргамма фазовых состояний
углерода и ее учет расчетах параметров детонации / С.А Губин, В.В Одинцов, В.В.
Пепекин // Химическая физика - 1986. -Т. 5, 1. - С. 111-120.
4. Долматов, В.Ю. Наноалмазы / В.Ю.
Долматов, Т. Фуджимура // Сверхтвердые материалы - 2001. - № 6. - С. 34-41.
5. Губаревич, Т. М. Полировальные системы на
основе ультрадисперсных алмазов / Т. М. Губаревич, В. Ю. Долматов // Журнал
прикладной химии - 1993. - Т. 66, № 8. - С. 1878-1881.
6. Долматов, В.Ю. Ультрадисперсные алмазы
детонационного синтеза: получение, свойства, применение / В.Ю. Долматов. -
Сант-Петербург: СПбГПУ, 2003. - 345 с.
. Губаревич Т.М. Химическая очистка
ультрадисперсных алмазов / Т.М. Губаревич, Р.Р. Сатаев, В.Ю Долматов // Докл. V
Всесоюз. совещ. по детонации, Красноярск, 1991. - Т. 1, - С. 135-139.
. Путятин А.А. Химические методы
извлечения алмазов из продуктов синтеза / А.А. Путятин, А.В. Никольская, Я.Н.
Калашников // Сверхтвердые материалы - 1982. - № 2. - С. 2-28.
9. Пат.
2019502 Российская Федерация, . Пат.
2077476 Российская Федерация, C 01 B 31/00. Способ очистки ультрадисперсных
алмазов/ Л.И. Филатов, С.И. Чухаева, П.Я. Детков ; заявитель и
патентообладатель РФЯЦ-ВНИИТФ ; заявл. 21.03.1991 ; опубл. 20.04.1997, Бюл. № 11. - 10 с.
. Бабушкин,
А.Ю.. Особенности получения ультрадисперсного материала на основе углерода из
взрывчатых веществ / А.Ю. Бабушкин, А.И. Лямкин, А.М. Ставер // Докл. V
Всесоюз. совещ. по детонации, Красноярск, 1991. - Т. 1, - С. 81-83.
. Международнная
заявка. PCT/SU 90/00169. Способ выделения алмазов из алмазсодержащей шихты. /
А.И. Шебалин, В.А. Молокеев ; заявл.18.07.88.
13. Пат. 2306258 Российская Федерация, МПК С
01 В 31/06. Синтетические алмазосодержащие вещества и способ их выделения /
А.П. Пузырь, В.Б. Воробьев (РФ). - № 2006106899/15 ; заявл. 06.03.2006; опубл.
20.09.2007, Бюл. № 26. - 15 с.
14. Пат. 2348580 Российская Федерация, МПК С
01 В 31/06, B 01 J 3/08. Синтетические алмазосодержащие вещества и способ их
выделения / В.Ю Долматов ; заявитель и патентообладатель ЗАО «Алмазный центр».
- № 2007118527/15 ; заявл. 30.12.2005; опубл. 10.03.2009, Бюл. № 7. - С. 3-11.
15. Пат. 2109683 Российская Федерация, C 01 B 31/00. Способ выделения
синтетических ультрадисперсных алмазов / В.Ю. Долматов, В.Г. Сущев, В.А.
Марчуков, T.М.
Губаревич, А.П. Корженсвский ; заявитель и патентообладатель ЗАО «Алмазный
центр» ; заявл. 05.03.1996; опубл. 27.04.1998, Бюл. № 12. - 13 с.
. Чиганова, Г.А. Физико-химические
свойства ультрадисперсных материалов : методические указания по лабораторным
работам для студентов инженерно-физического факультета / Г. А. Чиганова, А. И.
Лямкин. - Красноярск: КГТУ, 1999. - 32 с.
. Чухаева, С.И. Получение, свойства и
применение фракционированных наноалмазов / С.И. Чухаева // Физика твердого
тела. -2004. - Т. 46, № 4. - С. 611.
. Губаревич, Т.М. Исследование
микропримесного состава ультрадисперсного алмаза / Т.М. Губаревич, Н.М.
Костюкова, Р.Р. Сатаев, Л.В. Фомина // Сверхтвердые материалы. - 1991- № 5. -
С. 30-34.
19. Овчаренко, А.Г. Электрофоретическое поведение
агрегатов ультрадисперсных алмазных частиц / А.Г. Овчаренко, А.Б. Солохина,
Р.Р. Сатаев, А.В. Игнатченко // Коллоидный журнал. - 1991. - Т. 53, № 6. - С.
1067-1070.
. Духин, С. С. Электрофорез / С. С. Духин, Б. В.
Дерягин. - Москва: Наука,
1976. - 328 с.
21. Mc Cartney, L. M. An improvement on Derjaguin's
expression at small potentials for the double-layer interaction energy of two
spherical colloidal particlesrticles / L. M. Mc Cartney, S. Levine // J.
Colloid Interface Sci. - 1969. - V. 30, № 3. - P.
345-354.
22. Морару, В. Н. Устойчивость и электроповерхностные
свойства водных дисперсий окисленного синтетического алмаза / В. Н. Морару, Ф.
Д. Овчаренко, Л. А. Тоцкая // Коллоидный журнал. - 1991. - Т. 53, № 5. - С. 874-879.
. Игнатченко, А.В. Элетроповерхностные свойства
ультрадисперсных алмазов/ А.В. Игнатченко, А.В. Солохина, М.В. Ирдынеева // Докл. V Всесоюз. совещ. по детонации, Красноярск, 1991. -
Т. 1, - С. 164-170.
24. Чиганова, Г. А. Структура и свойства
ультрадисперсных алмазов детонационного синтеза / Г. А. Чиганова, А. С. Чиганов
// Неорганические материалы. 1999. - Т. 35, № 5. - С. 581-586.
25. Чиганова, Г. А. Разработка методов, способов и
технологии направленного изменения свойств ультрадисперсных порошков,
синтезированных детонационными методами: автореф. дис. … док. тех. наук :
05.16.06 / Чиганова Галина Александровна. - Красноярск, 2006. - 42 с.
![]()
![]() 170Не
определялась48
170Не
определялась48
![]()
![]() 17-1815-1612-13
17-1815-1612-13
![]()
![]() потенциал нефракционированного и несушеного ДНА производства
РФЯЦ-ВНИИТФ равен +(25-26) мВ при 297
потенциал нефракционированного и несушеного ДНА производства
РФЯЦ-ВНИИТФ равен +(25-26) мВ при 297![]()
![]() 298 К.
298 К.
2. Экспериментальная часть
2.1 Объект исследования
.2 Методы исследования
Методы ультразвукового диспергирования золей
наноалмазов
Устройство ультразвукового диспергатора УЗДН-А

Технические характеристики и работа диспергатора
Метод макроэлектрофореза
![]()
![]() связана
с величиной
связана
с величиной ![]()
![]() потенциала уравнением Гельмгольца-Смолуховского:
потенциала уравнением Гельмгольца-Смолуховского:
![]()
![]() (1)
(1)
![]()
![]() -
вязкость среды, Па·с;
-
вязкость среды, Па·с;
![]()
![]() -
напряженность электрического поля, В/м (
-
напряженность электрического поля, В/м (![]()
![]() , где U -
разность потенциалов внешнего поля, L - расстояние между
электродами);
, где U -
разность потенциалов внешнего поля, L - расстояние между
электродами);
![]()
![]() -
диэлектрическая проницаемость среды, Ф/м.
-
диэлектрическая проницаемость среды, Ф/м.
![]()
![]()
![]()
![]() , 5·
, 5·![]()
![]() (
(![]()
![]() ,
, ![]()
![]() (
(![]()
![]() . Разность потенциалов
внешнего поля равна 100 В, расстояние между электродами равна 23,2 см.
. Разность потенциалов
внешнего поля равна 100 В, расстояние между электродами равна 23,2 см.
Метод pH-метрии
3. Результаты и их обсуждение
3.1 Электроповерхностные характеристики
наноалмазов
![]()
![]() (2)
(2)
![]()
![]() -
среднее расстояния, на которые переместилось положение границы золя с
электролитом в каждом колене.
-
среднее расстояния, на которые переместилось положение границы золя с
электролитом в каждом колене.
![]()
![]()
![]()
![]()
![]()
![]()
![]() ,
м/с1,417±0,0031,667±0,0032,000±0,0171,250±0,017
,
м/с1,417±0,0031,667±0,0032,000±0,0171,250±0,017
![]()
![]() М до 5·
М до 5·![]()
![]() М
вызывает увеличение электрофоретической скорости частиц. Дальнейшее увеличение
концентрации приводит к уменьшению скорости. Немонотонный характер зависимости
электрофоретической скорости частиц ДНА производства НПО «Алтай» от
концентрации раствора KCl наблюдался так же в работе [19]. При объяснении
такого явления авторы указывали на необходимость учета структурно- измененных
слоев воды на поверхности частиц и иммобилизации дисперсионной среды внутри
агрегатов ДНА.
М
вызывает увеличение электрофоретической скорости частиц. Дальнейшее увеличение
концентрации приводит к уменьшению скорости. Немонотонный характер зависимости
электрофоретической скорости частиц ДНА производства НПО «Алтай» от
концентрации раствора KCl наблюдался так же в работе [19]. При объяснении
такого явления авторы указывали на необходимость учета структурно- измененных
слоев воды на поверхности частиц и иммобилизации дисперсионной среды внутри
агрегатов ДНА.
![]()
![]() = [2F2I/(eeoRT)]1/2,
(4)
= [2F2I/(eeoRT)]1/2,
(4)
![]()
![]() , (3)
, (3) ![]()
![]() :
: ![]()
![]() , e -
элементарный заряд, k - константа Больцмана.
, e -
элементарный заряд, k - константа Больцмана.
![]()
![]()
![]()
![]()
![]()
![]()
![]() , мВ42,84±0,10
, мВ42,84±0,10
![]()
![]() ,
нм96,030,413,69,6
,
нм96,030,413,69,6
.2 Расчет энергии взаимодействия частиц в золях
ДНА
![]()
![]() , (5)
, (5)
![]()
![]() константа
Гамакера, А =
константа
Гамакера, А = ![]()
![]() Дж для
дисперсий алмаза [21]; = (2a + h)/a (h
Дж для
дисперсий алмаза [21]; = (2a + h)/a (h ![]()
![]() расстояние
между поверхностями частиц, a
расстояние
между поверхностями частиц, a ![]()
![]() их
радиус).
их
радиус).
![]()
![]() , (6)
, (6)
![]()
![]() потенциал
слоя Штерна, приравниваемый в разбавленных растворах электролитов к
электрокинетическому потенциалу;
потенциал
слоя Штерна, приравниваемый в разбавленных растворах электролитов к
электрокинетическому потенциалу;
![]()
![]() толщина
диффузной части двойного электрического слоя.
толщина
диффузной части двойного электрического слоя.
![]()
![]() ????, 2 - ????=
????, 2 - ????=![]()
![]() ????, 3 - ????=5∙
????, 3 - ????=5∙![]()
![]() ????, 4 - ????=
????, 4 - ????=![]()
![]() ????.
????.
![]()
![]()
![]()
![]()
![]()
![]() Дж3,04
4,075,53 1,963
Дж3,04
4,075,53 1,963
![]()
![]() Дж (с
учетом структурных сил)3,23 4,41 6,13 2,31
Дж (с
учетом структурных сил)3,23 4,41 6,13 2,31
.3 Измерение рН
![]()
![]() в воде
гидролизуются, что приводит к подкислению воды:
в воде
гидролизуются, что приводит к подкислению воды:
![]()
![]() (8)
(8)
![]()
![]() )
сдвигает равновесие реакции гидролиза влево (в соответствии с правилом Ле
Шателье). Соответственно, и подкисление среды уменьшается с ростом концентрации
хлорида калия, что подтверждено данными измерений величины рН золей. Так,
величина рН дистиллированной воды составила 5,40, в отсутствие электролита для
0,1 % золя ДНА рН = 5,20, при концентрации хлорида калия в золе
)
сдвигает равновесие реакции гидролиза влево (в соответствии с правилом Ле
Шателье). Соответственно, и подкисление среды уменьшается с ростом концентрации
хлорида калия, что подтверждено данными измерений величины рН золей. Так,
величина рН дистиллированной воды составила 5,40, в отсутствие электролита для
0,1 % золя ДНА рН = 5,20, при концентрации хлорида калия в золе ![]()
![]() М рН =
5,25, при
М рН =
5,25, при![]()
![]() М КCl рН
= 5,30 и при
М КCl рН
= 5,30 и при ![]()
![]() М
величина рН = 5.35.
М
величина рН = 5.35.
![]()
![]() , мВ
, мВ
3.4 ДНА ТУ 3974-001-10172699-94, модифицированные
катионами никеля
Заключение
![]()
![]() составляют 40 - 60 мВ;
составляют 40 - 60 мВ;
Список использованных источников
![]()
![]() С 01 В 31/06, B01J3/06. Устройство для очистки и модификации
наноалмазов / И.Л. Петров, Ю. А. Скрябин, О.А. Шендерова ; заявитель и
патентообладатель ООО «СКН». - № 2010152860/05 ; заявл. 09.01.1994; опубл.
15.09.1994, Бюл. № 17. - 9 с.
С 01 В 31/06, B01J3/06. Устройство для очистки и модификации
наноалмазов / И.Л. Петров, Ю. А. Скрябин, О.А. Шендерова ; заявитель и
патентообладатель ООО «СКН». - № 2010152860/05 ; заявл. 09.01.1994; опубл.
15.09.1994, Бюл. № 17. - 9 с.