Материал: А27878 Андреев АК Материалы для низкотемпературной техники
заданного режима эксплуатационного нагружения получают непосредственно распределения и значения местных упругих либо упругопластических напряжений или деформаций. По этим распределениям могут быть определены номинальные напряжения или деформации, которые в дальнейшем используются при оценках прочности и ресурса. Вместе с тем следует признать, что для многих режимов и геометрических форм элементов конструкций такие расчеты чрезвычайно трудоемки, а их точность определяется заданием исходных краевых условий – по усилиям, температурам, фи- зико-механическим свойствам материалов.
Как показывает многолетняя практика проектирования и отработки наиболее сложных и ответственных машин и конструкций, повышенная точность при анализе прочности, ресурса и надежности достигается в тех случаях, когда используются комбинированные методы анализа истории эксплуатационного нагружения, номинальных и местных напряжений и деформаций.
61
2. ХЛАДНОЛОМКОСТЬ КОНСТРУКЦИОННЫХ СТАЛЕЙ
Хладноломкость – склонность металлов к появлению или значительному возрастанию хрупкости при понижении температуры. Проявление хладноломкости связано с получением при понижении температуры эффекта торможения движения дислокаций и значительным повышением предела текучести материала. Начиная с некоторой температуры (так называемая критическая температура хрупкости, или порог хладноломкости) хрупкое разрушение наступает раньше, чем состояние пластической текучести.
Наибольшее внимание уделяется процессам хладноломкости, протекающим в сплавах железа, как основного конструкционного материала современности. Хладноломкость в железных сплавах вызывается вредными примесями, главным образом фосфором, группой цветных металлов (свинцом, оловом, мышьяком и сурьмой); в меньшей степени – примесями серы, меди и цинка. Из этих примесей наибольшее влияние оказывает фосфор, концентрация которого жестко ограничивается всеми нормативными документами, регламентирующими производство сталей. Влияние его проявляется тем сильнее, чем выше содержание в стали углерода; эти элементы, конкурируя друг с другом в границах зерен, взаимно усиливают охрупчивающее влияние на сталь при понижении температуры.
Хладноломкость присуща не только углеродистым и низколегированным сталям, но также танталу, вольфраму, хрому, молибдену и некоторым другим металлам с объемно центрированной кубической решеткой и сплавам на их основе.
Температура перехода от вязкого разрушения к хрупкому зависит от режима термической обработки, величины зерна, скорости нагружения, величины концентрации напряжений. Чаще всего хладноломкость оценивают путем испытаний на ударный изгиб призматических образцов с надрезом, определяя при этом работу деформации и разрушения. Склонность к хладноломкости можно также оценить по температуре резкого снижения пластичности или по доле волокнистого излома на поверхности разрушения.
Знание процессов хладноломкости материалов имеет особое значение при эксплуатации конструкций в температурных условиях северных районов, для космических аппаратов, систем ядерной фи-
62
зики, криобиологии, водородных и других криогенных двигателей. Снижение хладноломкости достигается очисткой металлов от вредных примесей, термообработкой, легированием.
2.1. Общая характеристика металлов и сплавов
Металлы и их соединения – сплавы повсеместно используются для конструкций машин, оборудования, инструмента и т. д. Несмотря на широкий круг искусственно созданных материалов, керамики, клеев, металлы служат основным конструкционным материалом и в обозримом будущем по-прежнему будут доминировать.
В природе металлы встречаются как в чистом виде, так и в рудах, оксидах и солях. В чистом виде встречаются химически устойчивые элементы (Pt, Аu, Ag, Hg, Сu). Из 109 открытых элементов, представленных в Периодической системе элементов Д.И. Менделеева, только 22 являются неметаллами.
Металлические материалы обычно делят на две большие группы: железо и сплавы железа (сталь и чугун) называют черными металлами, а остальные металлы и их сплавы – цветными. Кроме того, все цветные металлы, применяемые в технике, в свою очередь, делятся на следующие группы:
–легкие металлы (Mg, Be, Al, Ti) с плотностью до 5 г/см3;
–тяжелые металлы (Pb, Mo, Ag, Аu, Pt, W, Та, Ir, Os) с плотностью, превышающей 10 г/см3;
–легкоплавкие металлы (Sn, Pb, Zn) с температурой плавле-
ния 232, 327, 410 °С;
–тугоплавкие металлы (W, Мо, Та, Nb) с температурой плавления существенно выше, чем у железа ( > 1536 °С);
–благородные металлы (Аu, Ag, Pt) с высокой устойчивостью против коррозии;
–урановые металлы, или актиноиды (актиниды), используемые в атомной технике;
–редкоземельные металлы (РЗМ) – лантаноиды, применяемые для модифицирования стали;
–щелочные и щелочно-земельные металлы (Na, К, Li, Ca)
всвободном состоянии, применяемые в качестве жидкометаллических теплоносителей в атомных реакторах; натрий также использу-
63
ется в качестве катализатора в производстве искусственного каучука, а литий – для легирования легких и прочных алюминиевых сплавов, применяемых в самолетостроении.
Свойства металлов разнообразны. Ртуть замерзает при температуре –38,8 °С; вольфрам выдерживает рабочую температуру до 2000 °С (Тпл = 3410 °С); литий, натрий, калий легче воды, а иридий и осмий в 42 раза тяжелее лития. Электропроводность серебра в 130 раз выше, чем у марганца. Вместе с тем металлы имеют характерные общие свойства. К ним относятся:
–высокая пластичность;
–высокая тепло- и электропроводность;
–положительный температурный коэффициент электрического сопротивления, означающий рост сопротивления с повышением температуры, и сверхпроводимость многих металлов (около 30) при температурах, близких к абсолютному нулю;
–хорошая отражательная способность (металлы непрозрачны и имеют характерный металлический блеск);
–термоэлектронная эмиссия, т. е. способность к испусканию электронов при нагреве;
–кристаллическое строение в твердом состоянии.
2.1.1. Кристаллическое строение Дефекты кристаллического строения
Общее свойство металлов и сплавов – их кристаллическое строение, характеризующееся определенным закономерным расположением атомов в пространстве. Для описания атомно-кристал- лической структуры используют понятие кристаллической решетки, являющейся воображаемой пространственной сеткой с ионами (атомами) в узлах.
Атомно-кристаллическая структура может быть представлена одной элементарной ячейкой. Трансляцией этого наименьшего объема можно полностью воспроизвести структуру кристал-
ла (рис. 2.1).
В кристалле элементарные частицы (атомы, ионы) сближены до соприкосновения. Для упрощения пространственное изображение принято заменять схемами, где центры тяжести частиц представлены точками. В точках пересечения прямых линий рас-
64
полагаются атомы; они называются узлами решетки. Расстояния между центрами атомов, находящихся в соседних узлах решетки, называют параметрами, или периодами решетки. Величина их в металлах порядка 0,1–0,7 нм; размеры элементарных ячеек 0,2–0,3 нм.
Рис. 2.1. Кристаллическая решетка
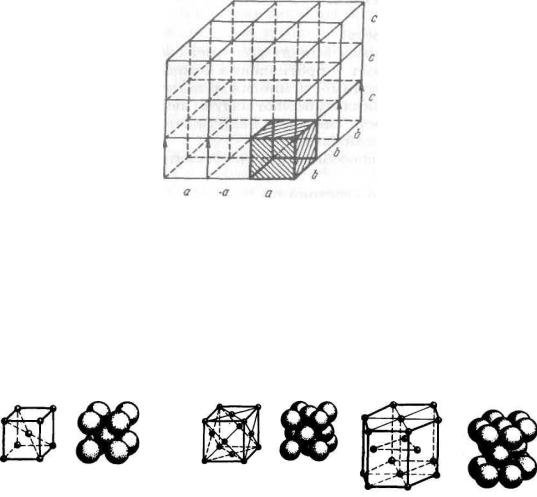
На рис. 2.2 показаны три типа элементарных ячеек кристаллических решеток, наиболее характерных для металлов: объемно центрированная кубическая (ОЦК), гранецентрированная кубическая (ГЦК) и гексагональная плотноупакованная (ГП), а также схемы упаковки в них атомов.
а |
б |
в |
Рис. 2.2. Типы элементарных ячеек кристаллических решеток
исхемы упаковки в них атомов:
а– обьемно центрированная кубическая; б – гранецентрированная кубическая;
в– гексагональная плотноупакованная
Вкубической гранецентрированной решетке атомы расположены в вершинах куба и в центре каждой грани (см. рис. 2.2, а).
Вкубической объемно ценрированной решетке атомы распо-
ложены в вершинах куба, а один атом – в центре его объема (см. рис. 2.2, б). В гексагональной плотноупакованной решетке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома – в средней плоскости призмы (см. рис. 2.2, в).
65