Материал: А27137 Проверить Рогов Б.А. Пищевая инженерия производства жировой про
Биологическая активность изомеров токоферолов
|
Наименование изомеров |
Биологическая активность в % |
Наименование изомеров |
Биологическая активность в % |
|
d-α-токоферол dl-α-токоферол d-β-токоферол dl-β-токоферол |
100 67 33 16 |
d-γ-токоферол dl-γ-токоферол d-δ-токоферол ε-токоферол ζ-токоферол |
1 Меньше 1 Меньше 1 Около 20 50 |
Помимо витаминной активности важнейшей особенностью токоферолов является их сильные антиокислительные свойства. Они хорошо защищают растительные масла или жиры от окисления. При этом сами токоферолы окисляются, теряя витаминные свойства. Устойчивость токоферолов к кислороду воздуха и к температурным воздействиям зависит от их строения.
В растительных маслах соотношение между различными изомерными формами токоферолов неодинаково.
Подсолнечное масло содержит максимальное количество α-токо-ферола по отношению к другим формам; за ним следует в убывающем порядке хлопковое масло, масло пшеничных зародышей и оливковое масло. В соевом и кукурузном маслах преобладают γ- и δ-токоферолы.
Содержание токоферолов в растительных маслах зависит от вида масличного сырья, способа получения масла и степени его очистки (табл. 6.2). При щелочной рафинации и дезодорации содержание токоферолов снижается. Однако в силу их значительной устойчивости к водным растворам щелочей и к тепловым воздействиям в рафинированных маслах сохраняется 84…85 % токоферолов от первоначального количества. Кроме самих растительных масел, носителями витамина Е могут быть синтетический α-токоферолацетат и концентраты витамина Е, которые получают или путем экстракции пшеничных зародышей, или молекулярной дистилляцией, или омылением растительных масел, богатых токоферолами.
Таблица 6.2
Содержание различных изомеров токоферолов в % от их общего количества
|
Наименование масла
|
Изомеры токоферолов |
||||||
|
α |
β |
γ |
β+γ |
δ |
ε |
ζ |
|
|
Соевое Кукурузное Хлопковое Арахисовое Подсолнечное Рапсовое Льняное Горчичное Оливковое Пшеничных зародышей Пшеничных отрубей Ячменя Овса Ржи |
13,5 11,0 58,0 35,5 92,2 27,0 38,8 26,8 44,2 56,0 11,0 15,3 28,0 39,0 |
– – – – – – – – – 33,5 5,5 – – – |
59,0 89,0 42,0 64,5 – 73,0 – 55,0 – – – 6,0 36,0 5,0 |
– – – – – – 30,6 – 27,9 – – – – – |
27,5 – – – 7,8 – 30,6 18,2 27,9 – – – 10,0 – |
– – – – – – – – – 10,5 68,0 34,2 4,0 32,0 |
– – – – – – – – – – 15,5 44,5 22,0 24,0 |
Витамины группы К – антигеморрагические витамины, регулирующие свертываемость крови. Витамины группы К содержатся в зеленых час-тях растений, овощах, некоторых ягодах.
И з
витаминов группы К наиболее распространены
витамины К1 и К2, которые
являются производными нафтохинона.
Корме того, синтетическим путем получен
витамин К3 и ряд других замещенных
гидрохинонов и нафтохинонов, обладающих
свойствами витамина К. Витамины группы
К имеют общую формулу:
з
витаминов группы К наиболее распространены
витамины К1 и К2, которые
являются производными нафтохинона.
Корме того, синтетическим путем получен
витамин К3 и ряд других замещенных
гидрохинонов и нафтохинонов, обладающих
свойствами витамина К. Витамины группы
К имеют общую формулу:
Они различаются строением боковой цепи (R) .
Витамин К1 (филлохинон) имеет радикал R следующего строения:
СН3
СН3
СН3
СН3
│ │ │
СН3–СН
=С
– (СН2)3
– СН – (СН2)3
– СН – (СН2)3
– СН
СН3
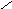

Витамин К1 – желтое вязкое масло, кристаллизующееся при температуре около –20 °C.
В противоположность филлохинону витамин К2 – твердое желтое вещество. От витамина К1 он отличается более длинной боковой цепью с шестью этиленовыми связями (радикал R):
СН3
СН3
│
СН2
– (СН =
С – СН2
– СН2)5
– СН =
С
СН3


Витамины группы К растворимы в жирах, в ряде органических растворителей и нерастворимы в воде. Они относительно термоустойчивы, но сравнительно легко разрушаются при действии света и щелочей. Витаминная активность витамина К2 почти в два раза ниже активности витамина К1.
В итамин
К3, называемый метионином или
менадионом, обладает биологической
активностью, в 2…2,5 раза превышающей
активность витамина К1. Он отличается
отсутствием боковой цепи в молекуле и
имеет следующее строение:
итамин
К3, называемый метионином или
менадионом, обладает биологической
активностью, в 2…2,5 раза превышающей
активность витамина К1. Он отличается
отсутствием боковой цепи в молекуле и
имеет следующее строение:
Витамин К3 представляет собой кристаллический порошок лимонно-желтого цвета со слабым характерным запахом. Температура плавления его 104…107 °C.
В табл. 6.3 приведена обобщенная характеристика различных наиболее распространенных витаминов, их функции и примерная суточная потребность человека в данных витаминах.
Таблица 6.3
|
. Витамин |
Суточная потребность |
Функции |
|
Аскорбиновая кислота (витамин С) |
50–110 мг |
Антициготный фактор. Участвует в окислительно-вос-становительных реакциях, повышает сопротивляемость организма к экстремальным воздействиям |
|
Тиамин (витамин В1) |
1,2–2,4 мг |
Необходим для нормальной деятельности центральной и периферической нервной системы |
|
Рибофлавин (витамин В2) |
1,5–3,0 мг |
Участвует в окислительно-восстановительных реакциях |
|
Пантотеновая кислота (витамин В3) |
5–10 мг |
Участвует в реакциях биохимического ацетилирования, обмена липидов, углеводов |
|
Ниацин (витамин РР, В5) |
15,0–25,0 мг |
Участвует в окислительно-восстановительных реакциях в клетках. Недостаточность вызывает пеллагру |
|
Пиридоксин (витамин В6) |
2,0–2,2 мг |
Участвует в синтезе и метаболизме аминокислот, жирных кислот и ненасыщенных липидов |
|
Фолиевая кислота, фолацин (витамин В9) |
200 мкг |
Кроветворный фактор, переносчик одноуглеродных радикалов, участвует в синтезе аминокислот, холина, пуриновых и пиримидиновых оснований |
|
Цианкобаламин, оксикобаламин, (витамин В12) |
2,0–50 мкг |
Фактор кроветворения, участвует в превращениях аминокислот |
|
Биотин (витамин Н) |
50–300 мкг |
Участвует в реакциях карбоксилирования-декарбокси-лирования, обмене аминокислот, липидов, углеводов, нуклеиновых кислот |
|
Холин, холинхлорид |
1–4 г |
Участвует в синтезе биологически важных соединений |
|
Ретинол (витамин А) |
0,5–2,5 мг |
Участвует в деятельности мембран клеток. Необходим для роста и развития человека, для функционирования слизистых оболочек. Участвует в процессе фоторецеп-ции – восприятии света |
|
Витамины группы D |
2,5–10 мкг |
Регуляция содержания кальция и фосфора в крови, минерализации костей, зубов |
|
Токоферолы (витамины группы Е) |
8–15 мг |
Предотвращают окисление липидов. Активные антиокислители
|
|
Витамины группы К |
1,5–4 мг |
Антигеморрагический фактор. Регулируют процесс свертывания крови |
6.3. Антивитамины
В природе встречаются вещества, способные оказывать на организм влияние, противоположное действию витаминов. Они инактивируют витамины. Такие вещества называют антивитаминами.
Многие из антивитаминов схожи по строению и реакционной способности с витаминами, но не обладают их биологическими свойствами. Занимая (например, в ферменте) место соответствующего витамина, аналога по строению, они лишают фермент присущих ему функций и тем самым нарушают обмен веществ. В других случаях структуроразличные соединения лишают витамин его действия, изменяя его молекулу или комплексно соединяясь с ним.
Антивитамин тиамина – окситиамин, будучи по строению близок тиамину, отличается от него тем, что вместо аминогруппы имеет оксигруппу. Из льняных семян выделено активное вещество линатин – антивитамин пиридоксина. В зерне кукурузы найден антагонист ниацина. Антивитамины нередко образуются в процессе жизнедеятельности растений. Вытяжка из проростков гороха и лепестков мака задерживают рост дрожжей, так как содержит антивитамины биотина и пантотеновой кислоты.
7. Фенольные соединения
К фенольным соединениям ФС относится обширный класс циклических веществ, являющихся производными ароматического спирта фенола (С6Н5ОН). В молекуле фенольных соединений имеется ароматическое кольцо, содержащее одну или несколько гидроксильных групп. Фенольные соединения находятся в растениях, плодах и овощах преимущественно в виде гликозидов и реже в свободном виде.
Биосинтез фенольных соединений в растительной клетке происходит в протоплазме, в частности, в хлоропластах. Однако основная масса водорастворимых фенолов сосредоточена в вакуолях, ограниченных от цитоплазмы белково-липидной мембраной тонопластом, который регулирует участие веществ, содержащихся в вакуолях, в метаболизме клетки. В животном организме фенольные соединения не синтезируются, а поступают с растительной пищей и участвуют в обменных процессах.
К гликозидам относятся разнообразные вещества, у которых какой-либо сахар (чаще глюкоза, реже другие моносахариды) соединен за счет гликозидного гидроксила с другими веществами, не являющимися сахарами (спиртами, альдегидами, фенолами, алкалоидами, стероидами и др.). Вторая часть молекулы гликозидов называется агликоном (не сахар).
От содержания и превращений фенольных соединений зависят цвет и аромат плодов, качество чая, кофе, вина. Многие фенолы обладают свойствами витамина Р и являются антиоксидантами.
Все фенольные соединения являются активными метаболитами клеточного обмена и играют важную роль в различных физиологических функциях, плодов, картофеля и овощей дыхании, росте, устойчивости к инфекционным заболеваниям.
О важной биологической роли фенольных соединений свидетельствует их распределение в растительной ткани. Разные органы и ткани растений, плодов и овощей различаются не только количественным содержанием фенолов, но и качественным их составом.
В настоящее время известно более 2000 фенольных соединений, существенно различающихся по своим свойствам. В связи с этим важное значение имеет классификация фенольных соединений, представленная на рис. 7.1.
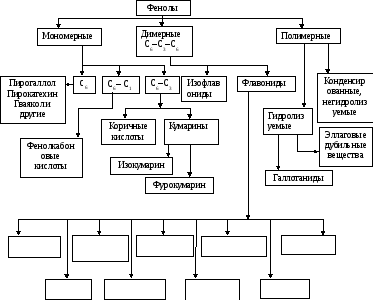
Катехины Лейкоанто- Флаваноны Флаванонолы Антоцианы
цианы
Флавоны Флавонолы Холконы Ауроны
Рис. 7.1. Классификация фенольных соединений
Фенольные соединения условно разделяются на три основные группы:
1. Мономерные.
2. Димерные.
3. Полимерные.
Мономерные фенольные соединения содержат одно ароматическое кольцо и делятся на три подгруппы:
соединения С6-ряда, состоящие из ароматического кольца без углеродных боковых цепей; к ним относятся гидрохинон, пирокатехин и его производные, гваякол, флороглюцин, пирогаллол. Все они содержатся в растениях главным образом в связанном виде;
соединения с основной структурой С6С1-ряда включают в себя группу фенолкарбоновых кислот и их производных протокатеховую, ванилиновую, галловую, салициловую, оксибензойную и другие кислоты; эти соединения встречаются в плодах и овощах в свободном виде;
соединения с основной структурой С6С3-ряда, состоящие из ароматического кольца и трехуглеродной боковой цепи, делятся на коричные кислоты, кумарины и производные последних: изокумарины, фурокумарины.
Кумарины рассматриваются как лактоны оксикоричных кислот. Наиболее распространенными коричными кислотами являются п-кумаровая, кофейная, феруловая и синаповая.
Фенолкарбоновые кислоты, обладая фенольными и кислотными группами, могут реагировать друг с другом с образованием соединений типа сложных эфиров, называемых депсидами. Если в реакции участвуют две фенолкарбоновые кислоты, то образуется дидепсид, если три тридепсид и т. п. Соединения С6С3-ряда участвуют в формировании аромата и вкуса плодов и овощей.
Димерные фенольные соединения имеют основную структуру с двумя ароматическими кольцами С6С3С6 и делятся на флавоноиды и изофлавоноиды (ротеноиды). Эти соединения наиболее широко распространены в природе, и многие из них принимают участие в формировании аромата и цвета растительных продуктов.
В зависимости от структуры связующего трехуглеродного фрагмента в молекуле и степени окисленности флавоноиды подразделяются на катехины, лейкоантоцианы, флаваноны, флаванонолы, антоцианы, флавоны, флавонолы и другие (см. рис. 7.1). Наиболее восстановленные соединения катехины, наиболее окисленные флавонолы.
Катехины бесцветные соединения, легко окисляются, в результате чего приобретают разную окраску. Например, различный цвет чая (черный, красновато-коричневый, желтый) обусловлен степенью окисления катехинов, содержащихся в чайном листе. Существует несколько форм катехинов: катехин, галлокатехин, галлокатехингаллат и другие. Каждый катехин может существовать в виде четырех оптических изомеров, различающих-ся по направлению и величине угла вращения: (+)-катехин, ()-катехин; (+)-эпикатехин, ()-эпикатехин. Кроме того, для каждого катехина известны два рацемата, т. е. смеси, лишенные оптической активности: (+)-ка-техин и (+)-эпикатехин. Все они отличаются по физическим свойствам и биологическому действию. Например, высокой Р-витаминной активностью обладает ()-эпикатехин.
В плодах и овощах катехины могут присутствовать в свободном и связанном состоянии (в составе полимерных форм). Много катехинов содержится в винограде, айве, черной смородине, яблоках, черноплодной рябине, косточковых плодах и ягодах.
Катехины хорошо растворимы в воде, имеют слабый вяжущий вкус, легко окисляются на свету, при нагревании, особенно в щелочной среде под действием окислительных ферментов (фенолоксидазы и пероксидазы). Продукты окисления хиноны и полимеризации катехинов флобафены придают плодам и овощам при термической и механической обработке темную окраску.
Окисление фенольных соединений может быть обратимым и необратимым. Этот процесс происходит и в здоровых, неповрежденных растительных клетках, но ткань их при этом не темнеет. Это обусловлено тем, что через тонопласт в цитоплазму поступает строго ограниченное количество фенолов, рассчитанное на тот ферментативный аппарат, который имеется в цитоплазме.
При окислении в здоровой клетке часть фенолов окисляется до карбоновых кислот и в качестве конечных продуктов окисления образуются СО2 и Н2О.