Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Пленочные и объемные конструкции были получены из полиоксибутирата и сополимеров оксибутирата с оксигексаноатом с при-
менением «salt leaching techniques» (Zhao et al., 2003). В ходе полу-
чения таких конструкций авторы варьировали плотность растворов полимеров, используемых для получения пленок и объемных матриц, а также соотношение компонентов в смеси «ПОБ-ПОБ-со- ПОГ». В результате были получены изделия, различающиеся структурой и свойствам, главным образом, температурными характеристиками и кристалличностью и, следовательно, различающиеся по прочности и эластичности Наиболее удачные объемные конструкции (scaffolds), полученные из композита двух полимеров, содержащие 60 % ПОБ-со-ПОГ, испытаны в эксперименте с культивируемыми in vitro клетками. Использовали первичную культуру хондроцитов, которые выделяли из 3-5 дневных кроликов. Культурой клеток засевали scaffolds и анализировали адгезию, рост клеток, формирования монослоя, а также синтез и выделение остеокальцина
(рис. 4.12).
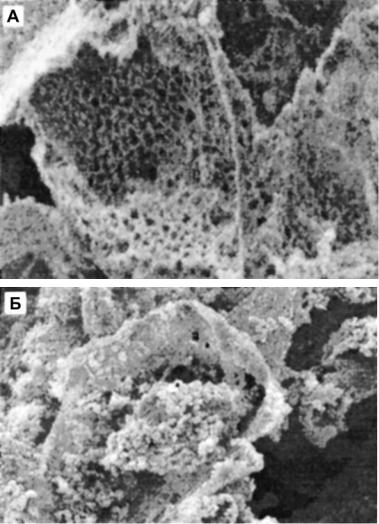
Рис. 4.12. Хондроциты, выращиваемые на матрицах из ПОБ-со-ПОГ: А – исходная матрица без клеток; Б – полимерная матрица с
растущими хондроцитами. Видны сферические клетки, вросшие в полимерную матрицу из ПОБ-со-ПОГ
(Zhao et al., 2003).
180
Клетки хондроцитов нормально росли на такой подложке и формировали костно-подобный слой, в котором соотношение кальция и фосфора соответствовало таковым в нормальной костной ткани. В следующем эксперименте подложки были имплантированы крысам линии Вистар на длительный срок. Все это время конструкции сохраняли прочностные характеристики. На сроке 26 недель отмечена выраженная деструкция полимерной матрицы, в основном, за счет аморфной фазы. В целом, продемонстрированы высокие фи- зико-механические и медико-биологический свойства конструкции и пригодность для реконструктивной хирургии костных тканей.
Впоследнее время для восстановительной хирургии костных тканей достаточно широкое развитие получили работы по получению композиционных материалов и scaffolds на их основе с использованием ПОА и гидроксиапатита Описаны успешные примеры получения пленочных и объемных конструкций ПОА с гидроксиапатитом и антибиотиками для заживления поврежденных костей, а также лечения хронических костных инфекций (Doyle et al., 1991; Lukinska and Bonfield, 1997 ; et al.).
Полиоксиалканоаты в чистом виде, а также в сочетании с полилактидами и другими материалами смешивают с трифосфатом кальция. Далее из такого композита формуются объемные или пленочные изделия, которые засеваются клетками. В зависимости от типа смешиваемых компонентов, молекулярного веса и условий формования получают конструкции различной структуры (плотные или пористые). Стандартными термомеханическими методами получают композиты на основе трифосфата кальция и полиоксибутирата,
вслучае же использования композитов ПОА с хитином используют растворные технологии. Пример таких технологий успешно иллюстрируется одной из работ этого направления (Wang et al., 2001). Авторы получили биоактивные биодеградируемые композиты, используя ПОА в смеси с гидроксиапатитом и хитином в сравнении с композитами хитина с полилактидом. Анализировали структуру и свойства полученных конструкций и характер развития на их основе клеток in vitro. В ходе экспериментов наблюдали процесс образование костеподобных кристаллов на поверхности и внутри данных конструкций. В композите ПОА/хитин происходит образование кристаллов минерала в виде островков спустя 28 дней (рис. 4.13a, а нормальный минеральный слой образуется через 72 дня (рис. 4.13б)
Вэкспериментах in vitro показано, что включение частиц биокерамики в биоразрушающиеся полимеры позволяет получать биоактивные композиты с улучшенными свойствами, например, обладающие стимулирующим эффектом по отношению к остеобластам. Постепенная биодеградация полимерного матрикса в таких конструкциях способствует проникновению в них размножающихся клеток и
181
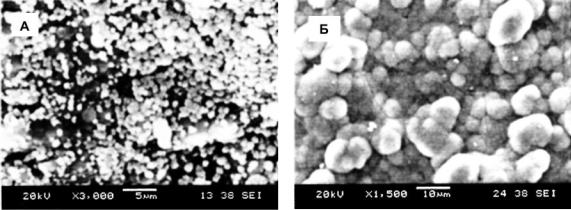
Рис. 4.13. Образование костеподобного слоя на подложке из композита «ПОА-хитин» (20 вес. % ПОА): А – 2 дня, Б – 72 дня эксперимента (Wang et al., 2001).
усиливает формирование тканей, тем самым способствует более эффективной регенерации тканей.
Таким образом, из представленных нескольких примеров видно, что, несмотря на то, что исследования ПОА применительно к задачам клеточной и тканевой инженерии находятся в стадии становления, уже сейчас просматриваются вполне реальные предпосылки для применения в этом перспективном направлении.
4.4. Стерилизация изделий из полиоксиалканоатов
Важной характеристикой материалов медицинского назначения является возможность применения для их стерилизации общепринятых методов, т. е. сохранение устойчивости при воздействии повышенных температур и др. стерилизующих агентов.
Термопластичность и радиационная устойчивость ПОА позволяют использовать для их стерилизации различные методы. Однако имеющиеся результаты по устойчивости ПОА-изделий к методам стерилизации фрагментарны и неоднозначны. Так, в работе (Lootz et al.,1997) показано, что при обработке экспериментальных изделий из ПОБ окисью этилена, парами формалина и автоклавированием не происходит деградации (разложения) материала, а также изменений молекулярного веса и прочности изделий, однако при стерилизации γ-источником (доза 40 kGy) было отмечено значительное падение величины Мв и снижение твердости изделий. Авторы другой работы (Miller and Williams, 1987) наблюдали резкое снижение прочностных свойств моножильных ПОБ- и ПОБ-cо-ПОВ-нитей при облучении γ- источником дозой существенно меньшей, 10 kGy, в то время, как меньшие дозы (2.5 и 5.0 Мрад) практически не влияли на структуру и прочностные показатели.
182

С целью определения устойчивости полимерных пленок к воздействию стерилизующих агентов исследовано влияние термических и химических методов стерилизации на физико-механические свойства (Шишацкая с соавт., 2001). Пленки стерилизовали термообработкой (в сухожарочном шкафу в течение 24 ч. при 120° и 140°С, автоклавированием при 120°С в течение 45 мин. (1.1 атм), облучением γ-источником (доза 2.5 Мрад) и выдерживанием в дезинфицирующих растворах (96 % этанол (24 ч.) и 6 % перекиси водорода (6 ч.) (рис. 4.14).
Существенных различий влияния способа стерилизации на величину молекулярной массы полимерного материала не выявлено, однако прочностные свойства пленок из ПОБ после автоклавирования и суховоздушной термообработки при 140°С несколько ухудшались. Пленки, изготовленные из ПОБ, при этом становились хрупкими. Отмечено некоторое (менее 20 %) снижение прочности. Негативного влияния исследованных способов стерилизации на аналогичные свойства пленок, изготовленных из ПОБ-со-ПОВ, не обнаружено. Результаты изучения влияния стерилизации на свойства поверхности полимерных пленок представлены в таблице 4.7.
Шовные нити, изготовленные из двух типов ПОА, стерилизовали паровым способом (автоклавированием в течение 45 мин. при 120 (1.1 атм) и 130°С (2.0 атм) и γ-облучением (доза 2.5 Мрад). Оба метода практически не влияли на прочностные свойства нитей, изготовленных из ПОБ-со-ПОВ. Зарегистрированные незначительные изменения показателей прочности ПОБ-нитей (абсолютная разрывная нагрузка и модуль упругости) в пределах 10 % от исходных значений находятся в пределах точности применяемых методов измерений (таблица 4.9). Отметим, что Европейская Фармакопея допускает падение прочности хирургических нитей после стерилизации на 25 %.
А Б
Рис. 4.14. Топография поверхности пленок, изготовленных из ПОБ (А) и ПОБ-со-ПОВ (Б): 1 – исходная, 2 – обработка этанолом, 3 – сухожаровая стерилизация,
4 – автоклавирование (Шишацкая с соавт., 2001).
183
Таблица 4.7 Влияние метода стерилизации на свойства полимерных пленок
(Волова с соавт., 2003)
Метод |
|
ПОБ |
ПОБ-со-ПОВ |
||
|
|
|
|
|
|
стерилизации |
Мw, кDа |
|
Прочность, |
Мw, кDа |
Прочность, |
|
|
кг/мм2 |
кг/мм2 |
||
без обработки |
340 ± 25 |
|
3.8 ± 0.6 |
260 ± 19 |
4.0 ± 0.3 |
(контроль) |
|
||||
|
|
|
|
|
|
120 С, 24 ч. |
330 ± 19 |
|
3.6 ± 0.3 |
258 ± 22 |
4.2 ± 0.2 |
|
|
|
|
|
|
140 С, 24 ч. |
300 ± 21 |
|
3.4 ± 0.4 |
240 ± 15 |
4.2 ± 0.4 |
|
|
|
|
|
|
γ-облучение |
342 ± 21 |
|
3.7 ± 0.3 |
264 ± 20 |
4.0 ± 0.2 |
(2.5 Мрад) |
|
||||
|
|
|
|
|
|
Автоклавиро- |
306 ± 28 |
|
3.2 ± 0.5 |
250 ± 31 |
4.1 ± 0.5 |
вание (1.1 атм) |
|
||||
|
|
|
|
|
|
Этанол, 96 % |
340 ± 19 |
|
3.8 ± 0.2 |
265 ± 23 |
4.1 ± 0.3 |
|
|
|
|
|
|
Н2О2, 6 % |
329 ± 23 |
|
3.7 ± 0.24 |
259 ± 22 |
4.0 ± 0.2 |
|
|
|
|
|
|
Таблица 4.9 Влияние метода стерилизации на прочностные свойств полимерных нитей
(Волова с соавт., 2003)
|
ПОБ-со-ПОВ |
|
ПОБ |
||
Метод |
|
|
|
|
|
стерилизации |
Абсолютная |
Прочность при |
Абсолютная |
|
Прочность при |
разрывная |
разрывная |
|
|||
|
|
||||
|
разрыве, МПа |
|
разрыве, МПа |
||
|
нагрузка, Н |
нагрузка, Н |
|
||
|
|
|
|
||
Без обработки |
9.40 ± 0.19 |
274 ± 27 |
7.10 ± 0.21 |
|
205 ± 31 |
(контроль) |
|
||||
|
|
|
|
|
|
Автоклавирова- |
9.41 ± 0.17 |
262 ± 22 |
7.21 ± 0.22 |
|
195 ± 12 |
ние (1.1 атм) |
|
||||
|
|
|
|
|
|
Автоклавирова- |
9.39 ± 0.24 |
286 ± 19 |
7.49 ± 15 |
|
182 ± 14 |
ние (2.0 атм) |
|
||||
|
|
|
|
|
|
γ-облучение |
8.95 ± 0.19 |
269 ± 21 |
7.00 ± 0.31 |
|
179 ± 21 |
(2.5 Мрад) |
|
||||
|
|
|
|
|
|
184