Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
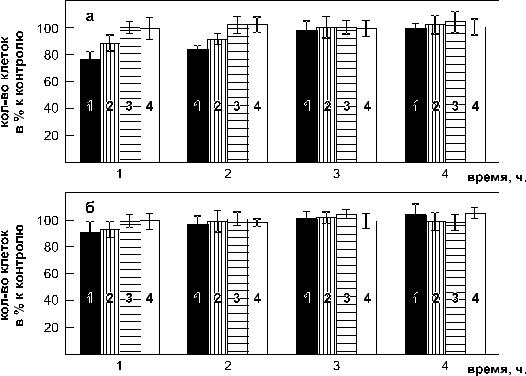
Рис. 4.15. Влияние способа стерилизации на адгезию фибробластов мыши линии NIH 3T3 на поверхности пленок ПОБ (а) и ПОБ-со-ПОВ (б) после стерилизации суховоздушной обработкой при 140°C (1), автоклавированием (2), γ-облучением 2.5 Mрад (3) и спиртом
(4). Контроль – стекло. По вертикали – среднее количество клеток в поле зрения (в % относительно контроля) (Шишацкая Е.И. с соавт., 2001).
Результаты исследования адгезии фибробластов мыши линии NIH 3T3 на поверхности полимерных пленок после стерилизации относительно контроля (стекло) представлены на рис. 4.15. Фибробласты культивировали в течение 4 часов в среде с 10 % ЭТС в прямом контакте с обработанными полимерными пленками. Следует отметить, что, независимо от способа стерилизации, вследствие низкой смачиваемости, пленки перед посевом клеток необходимо выдерживать не менее 2 часов в дистиллированной воде, так как на гидрофобной поверхности клетки плохо адгезируют. После стерилизации сухим жаром в течение двух часов и спиртовой обработки (с последующим выдерживанием образцов в стерильной деионизированной воде) количество клеток, прикрепленных на поверхности полимерных пленок, через 4 часа сопоставимо с контролем, хотя в первые два часа их было значительно меньше (рис. 4.15а). Аналогичные результаты получены в ходе исследования пленок из ПОБ-со-ПОВ (рис. 4.15б). Таким образом, стерилизованные ПОА-пленки обладают хорошими адгезионными свойствами по отношению к культивируемым фибробластам мыши.
Тем самым установлена возможность стерилизации пленок и нитей из полиоксиалканоатов общепринятыми методами и показано, что их прочностные свойства не ухудшаются в процессе термообработки, а также после γ-облучения.
185
Глава 5. БИОДЕГРАДАЦИЯ ПОЛИОКСИАЛКАНОАТОВ
Способность полиоксиалканоатов разрушаться до конечных продуктов (аэробно, до СО2 и Н2О) в различных биологических средах является одним из наиболее ценных их свойств (Jendrossek et all., 1990; Brandl et al., 1990; Abe et al., 1995; 1998; 2000; Abe, Doi, 1996;1999; Doi, Abe, 1997; Jendrossek, 2001).
Полиоксиалканоаты могут разрушаться не только под воздействием температуры, но в результате кислотного и щелочного гидролиза, а также под биологическим путем, под воздействием ферментов – деполимераз. При термальном разложении происходит случайное разделение полимера (Grassie and Murray,1984). Под влиянием кислот или щелочей полиоксиалканоаты разлагаются, как обычные эфиры. Гидролиз ПОБ сильной кислотой (например, 3N НСl) при 104.5 показал, что кислота атакует эфирные соединения кристаллизованной оболочки, но не кристаллизованного ядра ПОБ гранул. (Yu et all., 2000). В разбавленных растворах процесс химического гидролиза полиоксиалканоатов протекает крайне медленно, но увеличивается при высоких температурах (Mergaert, 1993). Биологическая деградация ПОА происходит гидролитически под воздействием специфических ферментов-деполимераз, продуцируемых микроорганизмами, а также ферментами крови и тканей высших животных
(Doi et al., 1992 a,b; Gogolewski et al. , 1993a, b; Abe and Doi, 1996; Abe et al., 1998;).
5.1. Биодеградация ПОА в модельных и природных средах
Наиболее изучаемым аспектом биодеградации ПОА является способность микроорганизмов использовать данные полимеры в качестве субстрата для роста. Микроорганизмы разрушают ПОА внутри клеток эндодеполимеразами и внеклеточно – под воздействием внеклеточных деполимераз (Jendrossek et all., 1996). Микробные ПОА-деполимеразы относят к сериновым эстеразам (Brucato, Wong, 1991; Müller, Jendrosek, 1993).
Внутриклеточные деполимеразы ПОА не гидролизуют полукристаллические полиоксиалканоаты, выделенные из биомассы, а внеклеточные деполимеразы не обладают субстратной специфичностью по отношению к полимеру, ассоциированному в гранулах внутри клеток. Это связано с различным фазовым состоянием и различиями в
186
структуре внутриклеточного «нативного» и внеклеточного «денатурированного» из гранул полимера (Jendrossek et all., 1996).
При внеклеточной деградации полимера продукт гидролиза поглощается микроорганизмами, утилизируется в виде разложенных на составные части соединений в качестве источников питания. Экзодеполимеразы многих бактерий, а также грибов выделены в чистом виде и охарактеризованы. К их общим свойствам следует отнести следующее: а) стабильность при изменяющихся условиях pH, температуры и ионной силы среды; б) относительно низкую молекулярную массу (менее 100 кДа); в) большинство деполимераз состоит только из одного полипептида; г) ПОА-деполимеразы не связываются с анионами таких веществ как ДЕАЕ (нейтральная pH), но близки по свойствам к гидрофобным материалам; д) оптимум pH для них составляет 7.5-9.8,(исключение составляют экзодеполимеразы P. pickettii и P.funiculosum, имеющие оптимум рН, соответственно, 5.5 и 6.0) большинство PHA деполимераз подавляются ингибиторами сериновых гидролаз, такими как диизопропилфлуорофосфат или ацилсульфаниловыми соединениями, которые ковалентно связываются с активным участком серина у сериновых гидролаз (Jendrossek et all., 1996).
Показано, что процесс энзиматической деградации пленок из ПОБ на 2–3 порядка выше, чем обычная небиологическая гидролитическая деградация в водных средах (Kumagai, 1992a, b). Факторами, наиболее воздействующими на биоразрушаемость, являются стереоконфигурация, степень кристалличности и молекулярная масса данных полимеров, а также химический состав (Kanewasa et all., 1994; Abe et al., 1998). Установлено, что между длиной углеродной цепи ПОА и ее разрушением существует прямая связь (Quinteros et all., 1999). При изучении пленочных образцов было показано, что ПОАэкзодеполимераза в первую очередь гидролизует полимерные цепи в аморфной фазе и только после этого затрагивает упорядо-
ченные зоны (Organ, Barham, 1988; Doi et al., 1989b; 1992a; Hocking et al., 1996). В целом процесс энзиматической деградации полимера в аморфном состоянии примерно в 20 раз превышает деградацию цепей кристаллического строения ( Abe et all., 1995).
Сотрудники под руководством профессора Дои, проводящие широкие исследования в области биосинтеза и изучения структуры и свойств различных по составу ПОА, предположили, что ферментный гидролиз полиоксиалканоатов имеет двухступенчатый характер. Сначала происходит адсорбция деполимеразы на полимере и далее начинается его гидролиз (Doi et all., 1994; Kasuya et all; 1995).
Продуктами, образуемыми в ходе энзиматической деполимеризации ПОА, могут быть мономеры (например, у Comamonas sp., Al.eutrophus), димеры (P.fluorescens) или смесь олигомеров, от мономеров до тримеров (A. faecalis и P. lemoignei). Олигомеры затем
187
разрушаются до мономеров олигомерными гидролазами (Abe et all.,
1999; Jendrossek et all., 1996; Shirahura et all., 1986)
Возможны два места энзиматической атаки фермента при взаимодействии с упорядоченной фазой ПОА. В первом случае размер кристалла уменьшается от грани по направлению к центру. Фермент последовательно деградирует индивидуальные цепи вдоль гранул кристалла, начиная от доступного конца цепи (Urmeneta et all., 1995; Yu et all., 2000). В другом случае деградация цепей основана на разделении цепи. Вначале атака инициирует складки цепей и затем продолжается перпендикулярно ламелярному слою до тех пор пока не достигнет плотного ламелярного центра, после этого процесс останавливается. Существует мнение, что отдельные кристаллы атакуются от конца кристалла предпочтительнее, чем от складки по-
верхности (Urmeneta et all., 1995).
Бактериальная деградация различных типов полиоксиалканоа-
тов Comamonas sp., Pseudomonas lemoignei и Pseudomonas fluorescens GK 13 показала, что процесс гидролиза зависим от поверхностного слоя, где полимер подвергается действию бактериальных ферментов. Сканирующей микроскопией частично разрушенных образцов выявлено, что гидролиз начинается на поверхности, потом повреждение полимера продолжается частично и внутрь. Для не деградируемых полиоксиалканоатов этого не наблюдается (Molitoris et all., 1996; Yu et all., 2000). Так, (Doi and Iwata, 1992; Iwata et all., 1999) изучена деградация отдельных кристаллов сополимеров 3- оксибутирата с различными оксикислотами деполимеразой, выделенной из Alcaligenes faecalis T1. Энзиматическая деградация отдельных кристаллов продвигалась от края и конца кристалла до раскалывания на небольшие кристаллические фрагменты. Лямелярный слой отдельных кристаллов и молекулярный вес цепей сополимеров оставались при этом без изменений в течение энзиматического гидролиза. Полученные результаты подтверждают гипотезу, по которой гидрофобная адсорбция фермента способствует увеличению подвижности молекулярных цепей отдельных кристаллов и производит расстройство в области упаковки цепей. Активный участок ПОБ деполимеразы беспорядочно связывается с областью упаковки цепей краев и концов кристалла (Iwata et all., 1999). Энзиматическая деградация ПОА имеет ограничения вследствие затруднений, возникающих при диффузии гидрофильного фермента в гидрофобный полимер (Wu et all., 1998).
В литературе встречаются немногочисленные примеры изучения биодеградации ПОА. Так, изучены динамика разрушения сополимеров оксибутирата и оксивалерата, с различной величиной включения последнего (Madden et al., 1998) и установлено, что сополимерные образцы разрушаются быстрее. Стереоизомеры различных
188
структурных вариаций ПОА, полученные в различных режимах биосинтеза и химического синтеза, исследованы в работе (Abe et al., 1994). Биосинтетический полимер был взят из A. eutrophus и синтезирован химически из бутуролактона в присутствии различных катализаторов. Установлено, что добавлением атактического синтетического ПОБ можно изменять температурные характеристики и степень кристалличности материала в широком интервале, что значительно влияет на скорость разрушения. Среди водорастворимых продуктов гидролиза бактериального полимера обнаружена смесь димеров и мономеров, смесей [RS]-полимеров – смесь мономеров, димеров, тримеров и тетрамеров.
Выявлено, что морфология надмолекулярой структуры ПОА влияет на его биодеградацию (Canetti et al., 1999. Авторами исследованы пленки, полученные из расплава полимера при различных температурах, деградируемые экзодеполимеразой Aureobacterium saperdae. Увеличение степени кристалличности и размеров кристаллов приводило к уменьшению скорости деградации полимера. Отрицательное влияния увеличения степени кристалличности ПОА на скорость их биодеструкции отмечено также в работе (Kusaka, Doi, 1999). Авторами изучена разрушаемость высокомолекулярного полиоксибутирата, синтезированного рекомбинантным штаммом E. coli, трансформированного генами Ralstonia eutropha, под воздействием деполимеразы Al. faecalis. Выявлено существенное влияния на скорость деградации степени кристалличности материала и температуры среды и практическое отсутствие влияния на процесс величины молекулярной массы ПОА.
В модельных лабораторных системах (почве, почвенных вытяжках и воде) исследована кинетика разрушения пленок, изготовленных из ПОБ и сополимеров оксибутирата и оксивалерата (ПОБ-со- ПОВ) с различными исходными свойствами (таблица 5.1) (Волова с соавт., 1992а; 1996; 1998).
Таблица 5.1 Свойства ПОА, использованных для получения пленок и изучения
биодеградации
№ п/п |
Соотношение |
Мв |
Тпл |
Кристалличность |
образца |
3(ПОБ-со-ПОВ) |
(Da) |
(°С) |
Сх (%) |
|
(мол. %) |
|
|
|
1 |
100 |
0 |
179 |
70 |
2 |
100 |
0 |
178 |
67 |
3 |
100 |
0 |
182 |
72 |
4 |
90 |
10 |
168 |
55 |
5 |
85 |
15 |
160 |
53 |
6 |
70 |
30 |
143 |
не определено |
189