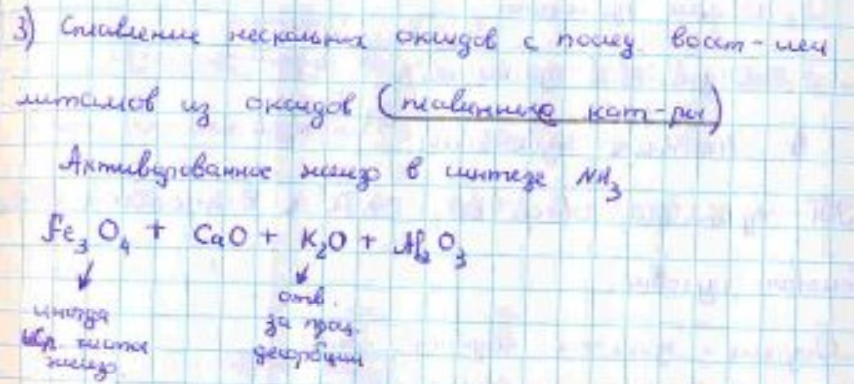Материал: OKhT_lektsii
В процессах, протекающих в гетерофазных системах, в частности, в рамках гетерогеннокаталитических процессов, к которым относится синтез формальдегида, важную роль играют массообменные процессы.
1) диффузия газообразных (или жидких) реагентов из потока через пограничный газовый (или жидкий) слой к внешней поверхности катализатора (внешняя диффузия);
2) внутренняя диффузия газообразных (или жидких) реагентов в порах твердого вещества катализатора к внутренней поверхности;
3) адсорбция реагентов, химическая реакция на поверхности, десорбция продуктов;
4) внутренняя диффузия газообразных (или жидких) продуктов реакции в обратном направлении;
5) внешняя диффузия газообразных (или жидких) продуктов через пограничный слой в поток.
В зависимости от соотношения скоростей этих стадий гетерогенные процессы могут протекать в диффузионной, переходной или кинетической области.
В качестве примера рассмотрим некий гетерогенно-каталитический процесс с участием газообразного реагента. Выражения для скоростей внешней (через пограничный газовый слой толщиной у поверхности катализатора) и внутренней (в порах к внутренней поверхности катализатора) диффузии запишем по закону Фика уравнениями (3.1.8) и (3.1.9), соответственно.

- коэффициент массоотдачи ( = D/, D - коэффициент диффузии, - толщина ламинарной газового слоя вокруг твёрдой частицы);
k - константа скорости химической реакции; ' - коэффициент массоотдачи в твердой фазе ( ' =Dэф/Rз , Dэф - эффективный коэффициент диффузии, Rз – радиус зерна катализатора).
Поскольку концентрации у внешней и внутренней поверхности катализатора трудно измерить и они, как правило, не известны, выразим скорость реакции в стационарном режиме (скорости всех последовательных стадий, перечисленных выше, равны между собой) через известную концентрацию реагента в объеме. Приравняв скорости внешней, внутренней диффузии и химической реакции (r = rU = rF) и проведя простые преобразования для исключения неизвестных концентраций CF и CS, получим (3.1.11).

Если сопротивление на одной из стадий значительно превышает сопротивление двух других стадий, то эффективная константа скорости с достаточно хорошим приближением будет равна константе скорости этой стадии. Эта стадия называется лимитирующей (или скорость определяющей) и характеризуется следующими особенностями:
- обладает максимальным сопротивлением и, следовательно, минимальным коэффициентом интенсивности в уравнении скорости (k, или ');
- на лимитирующей стадии происходит максимально возможное изменение концентрации газообразного реагента от CU до нуля (для необратимых реакций) или от CU до CU * (для обратимых реакций);
- скорость гетерогенного процесса может быть рассчитана как скорость лимитирующей стадии.
Гетерогенные процессы протекают в кинетической области, если велика скорость массообмена и относительно мала скорость химической реакции. Для кинетической области характерно сильное влияние температуры на скорость процесса (энергия активации для большинства реакций достаточно велика и составляет 40 - 280 кДж/моль). Это обычно бывает при низких температурах и давлениях, больших скоростях газового потока и при высокой пористости или отсутствии слоя «золы» (для процессов с участием твердых реагентов, например, различные виды обжига и выщелачивания). При этом >> k, ' >> k и r k CU (для реакций первого порядка).
Для интенсификации процесса необходимо повышать температуру (если наблюдаемая энергия активации имеет положительную величину) и концентрации (парциальные давления) реагентов.
Если скорость процесса массопереноса из потока к поверхности значительно меньше скорости химической реакции и внутренней диффузии, то процесс протекает во внешней диффузионной области. Величина энергии активации составляет 8-20 кДж/моль. При этом << k, << '.
Для интенсификации процессов, протекающих во внешнедиффузионной области, необходимо увеличивать скорость потока, а также проводить процесс при интенсивном перемешивании.
Если выполняются условия ’ << k, ' << , процесс лимитируется внутридиффузионным торможением. Увеличение скорости внутренней диффузии возможно, главным образом, за счет уменьшения размера зерна катализатора (или частиц твердого реагента, участвующего в процессе).
В переходной области наблюдается примерно одинаковое влияние кинетики химической реакции и процессов массопереноса на скорость гетерогенного процесса, а коэффициенты интенсивности k, и ' и, соответственно, сопротивления на каждой стадии соизмеримы по величине.
Как следует из экспериментальных данных, образование формальдегида на серебряном катализаторе при линейной скорости газового потока W 2 м/сек и температурах ниже 300 ОС протекает в кинетической области, при 300 - 500 ОС - в переходной и выше 500 ОС - во внешнедиффузионной области.

2.6Каталитические процессы. Технологические характеристики твердых катализаторов, требования, предъявляемые к ним. Каталитические особенности. Промышленный катализ. Свойства катализаторов и их классификация. Требования к промышленным катализаторам и их технологические характеристики. Способы изготовления катализаторов. Причины дезактивации катализаторов. Основные стадии и кинетические особенности гетерогенных процессов. Признаки протекания процессов в диффузионной и кинетической областях. Пути интенсификации гетерогенно-каталитических процессов. Гомогенный катализ. Ферментативный катализ. Автокатализ
Катализатор-вещества, которые многократно вступают в промежуточные взаимодействия с участниками реакции изменяют ее механизм и увеличивают скорость реакции. При этом они восстанавливают свой химический состав после каждого цикла промежуточных взаимодействий.
95% всех процессов-каталитические.
Катализ-ускорение химических превращений, химическое равновесие при этом не сдвигается ,так как ускоряются как прямая, так и обратная реакция.
Использование катализатора меняет механизм реакции. Она протекает через ряд последовательных стадий. При этом высокий потенциальный барьер делиться на несколько мелких барьеров, то есть реакция идет по более энергетически выгодному пути.
Гомогенный и микрогетерогенный катализ — однофазные процессы, и к ним применимы закономерности, характерные для гомогенных и газожидкостных химических процессов.
Ферментативный катализ( биокатализ), ускорение биохимических реакций при участии белковых макромолекул, называемых ферментами ( энзимами). Ферментативный катализ- разновидность катализа. 5 пункт природный катализатор
АВТОКАТАЛИЗ, ускорение р-ции, обусловленное накоплением конечного или промежут. продукта, обладающего каталитич. действием в данной р-ции. В более широком смысле автокатализ - самоускорение р-ции, вызванное к.-л. изменением в системе из-за протекания хим. р-ции. Автокатализ наблюдается, напр., при гидролизе сложных эфиров из-за накопления к-ты.
Классификация катализаторов
1. Металлы ( Реакция изомеризации окисления димеризации гидратации)
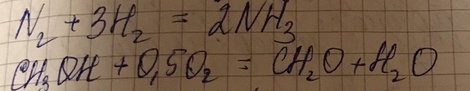
а) компактные/ массивные (шарики сетки) состав один металл
б) нанесённые катализаторы (нитраты карбонаты) методы холодной горячей пропитки
в) скелетные катализаторы


Катализаторы загораются на воздухе
2. Бинарные катализаторы
Комбинация оксидов
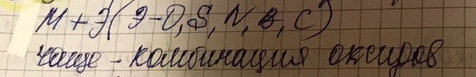
а) нанесённые- раствор в растворителе вносится носитель горячий/ холодный и на него садится соединение (карбонаты/ нитраты и т.д.) и потом улетают с поверхности
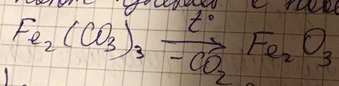
б) Смешанные- в воде или др. растворяют соли, затем подщелачивают. При этом происходит:
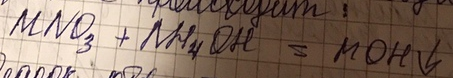
Осадок отфильтруется, выпадает смесь гидроксидов, фильтруем сушим добавляем формообрзование добавки для прочности прокаливаем придаёт форму
Бинарные катализаторы хорошую гидрируют
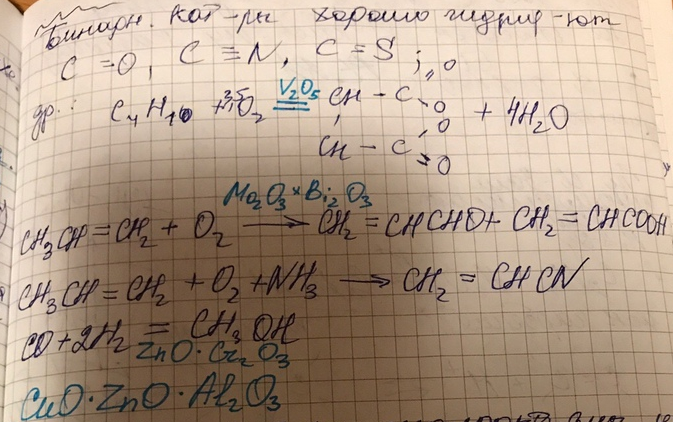
Сульфидные катализаторы малоактивны, но очень стабильны – не отравляются ,очищают от серосодержащих соединений ( в том числе для нефти)
3. Кислоты и основания ( органические и неорганические)
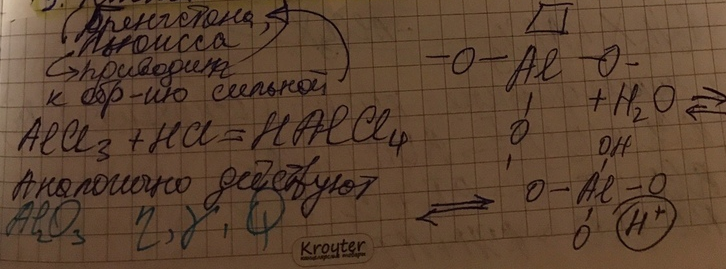
При 1000 0С Al2O3 не способен к кислотному катализу.
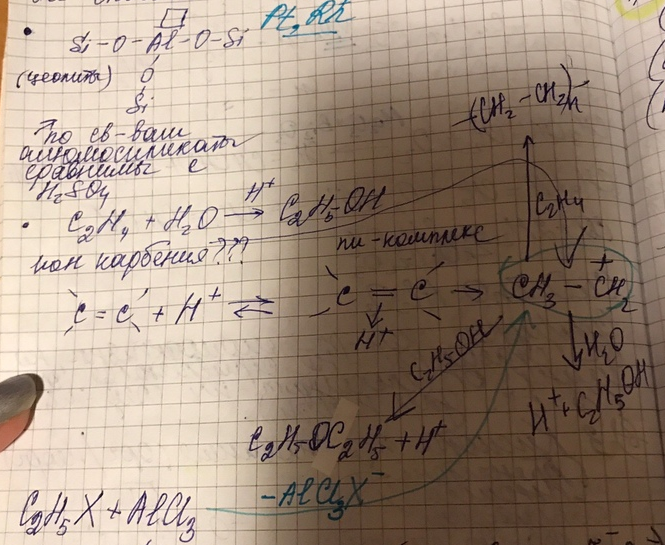
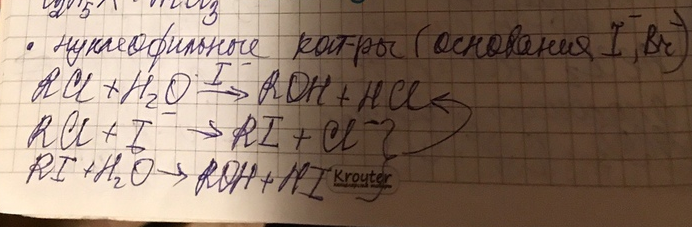
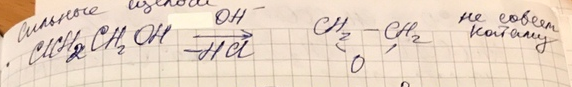
4. Комплексы металлов (кроме бинарных соединений)
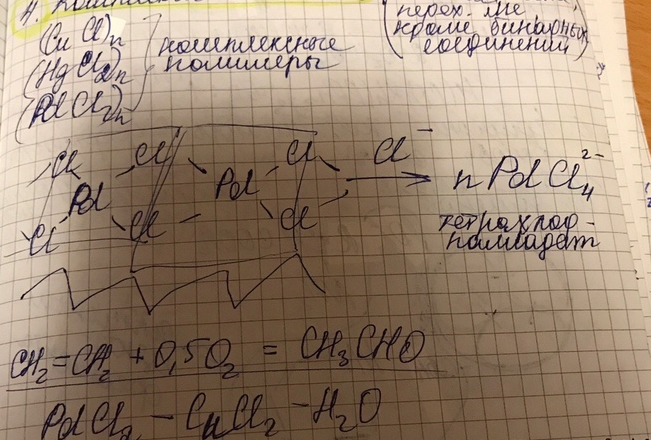

Регенирируются все компоненты системы цикл может повторятся много раз

5. Природные катализаторы- ферменты (основа белок)
Сложное строение активного центра
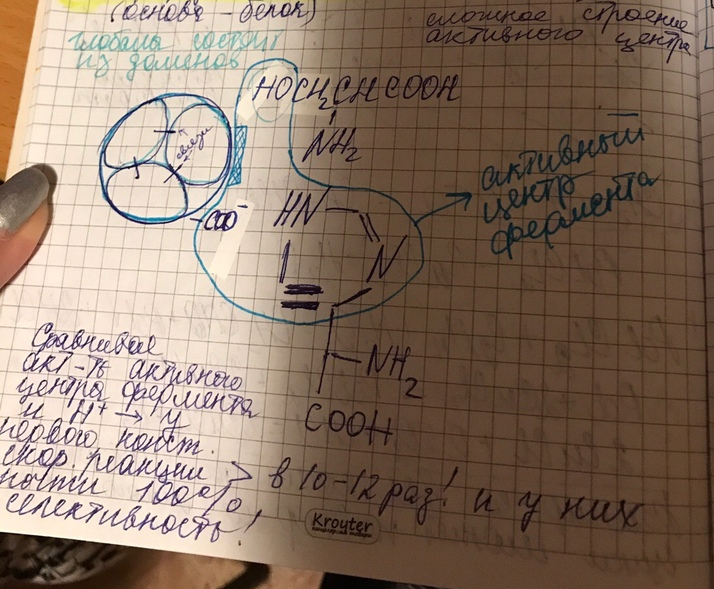
Катализатор снижает энергию активации!и позволяет проводить процесс при более низких температурах, это особенно важно для обратимых экзотермических реакции.
Необходимыми стадиями каталитического гетерогенного процесса являются
) диффузия газообразных (или жидких) реагентов из потока через
пограничный газовый (или жидкий) слой к внешней поверхности
катализатора (внешняя диффузия);
2) внутренняя диффузия газообразных (или жидких) реагентов в
порах твердого вещества катализатора к внутренней поверхности;
3) химическая реакция на поверхности;(адсорбция вещества на поверхности катализатора с образование комплекса реагент-катализатор,перегруппировка атомов с образованием комплекса продукт-катализатор,десорбция продукта с поверхности –внутрь зерна катализатора)
4) внутренняя диффузия газообразных (или жидких) продуктов
реакции в обратном направлении;
5) внешняя диффузия газообразных (или жидких) продуктов через
пограничный слой в поток.
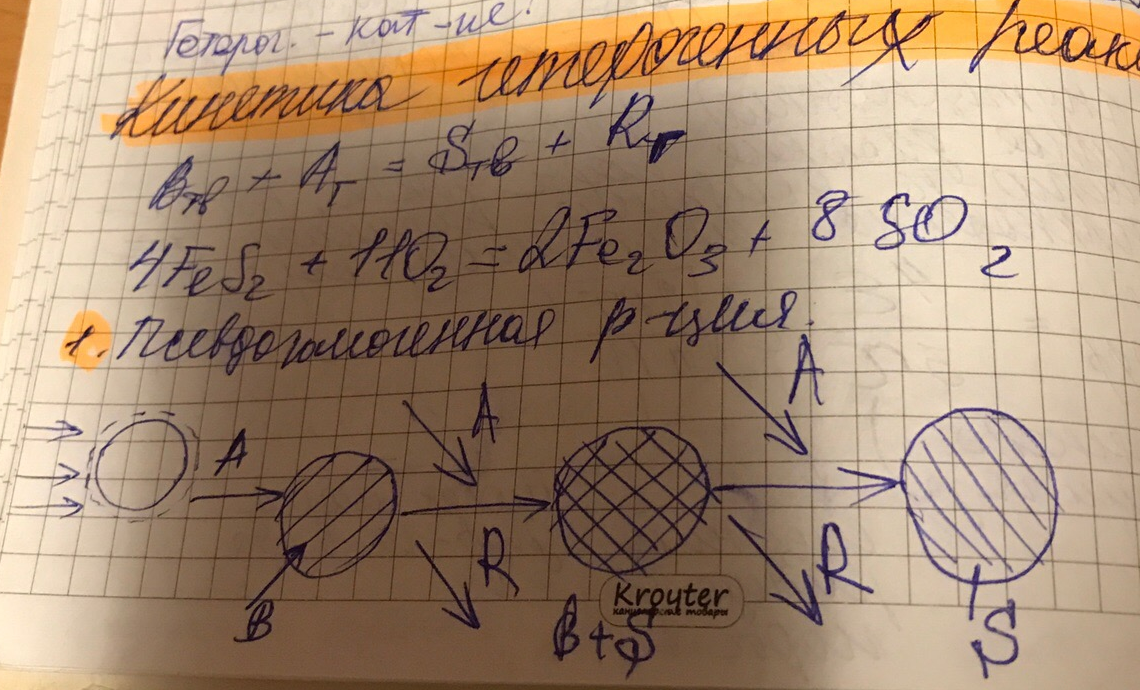
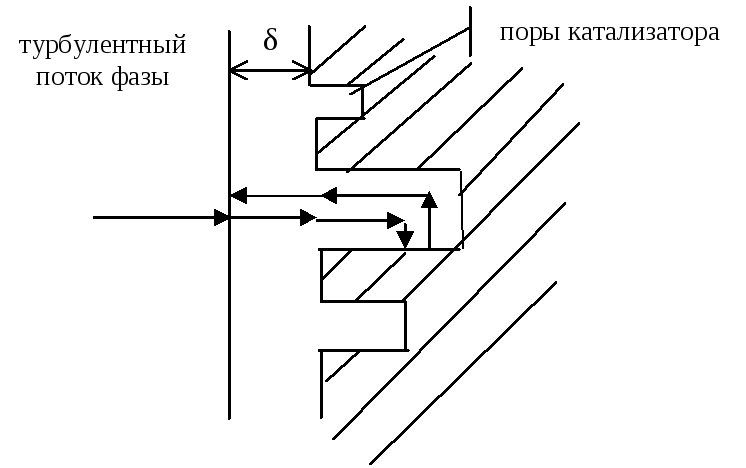
В общем случае процесс гетерогенного катализа складывается из следующих стадий:
1 – внешняя диффузия молекул реагентов из ядра потока к поверхности катализатора через пограничный слой δ;
2 – внутренняя диффузия молекул в порах катализатора;
3 – активированная адсорбция молекул на поверхности катализатора с образованием поверхностных непрочных химических соединений – активированных комплексов;
4 – перегруппировка атомов с образованием поверхностных комплексов «продукт-катализатор» (химическая реакция);
5 – десорбция молекул продуктов с поверхности;
6 – внутренняя диффузия молекул продуктов в порах катализатора;
7 – внешняя диффузия молекул продуктов от поверхности катализатора в ядро потока через пограничный слой
Стадии 3, 4, 5 являются химическими, 1, 2, 6, 7 – массообменные (диффузионные).
Любая стадия может быть лимитирующей.
Изменение энергии активации зависит от природы катализатора:
-
без катализатора-250
-
Fe2O3-160
-
V2O5-92,
-
Pt-68
Катализаторы не бывают индивидуальные вещества,они представляют собой сложную контактную массу,в которой одни вещества являются собственно катализаторами,а другие активаторами или носителями.
Активаторы-вещества повышают активность основного катализатора.(для серы V2O5*K2S2O7)
Активация может происходить вследствии химических взаимодействий добавок с каталитическими веществами с образование продуктов имеющих большую каталитическую активность. Активатор может увеличивать термостойкость и защищает от действия каталитических ядов.
Носители-термостойкие, пористые вещества ,на которые осаждают из растворов или другим способом наносят катализатор.
В качестве носителей используют, глинозем, силико-гель ,алюмосиликаты, различные соли, активный уголь.
Активность катализатора зависит не только от состава, но и от физических величин
-
Величина зерен
-
Пористость
-
Размер пор
-
Характер их поверхностей
-
Активность катализатора зависит от его способа приготовления.
Основные методы приготовления кат:
1)осаждение гидроксидов из раствора их солей, совместно с носителями или без них. С последующим формирование и прокаливанием контактн.массы. Массу формируют в виде таблеток, зерен и гранул.
2)Смешение и совместное прессование порошков=смешанные кат
3)пропитка пористого носителя раствором содержащим кат и активатор.С последующей сушкой и прокалкой .К кат такого вида относятся –метал.,оксиные,солевые,кислотные,основные.
4)сплавление нескольких веществ(ме или оксид) с послед.восстановлением ме из оксидов водородом
Иногда кат выполняют в виде сетки.
Требования предъявляемые к катализатору.
1)Активность-мера ускоряющая действие катализатора по отношению к данной реакции.A=eE-Ek/RT
2)Низкая температура зажигания-это температура ,при которой процесс начинает идти с достаточной для промышленной цели скоростью. Чем ниже температура зажигания, тем лучше, так как расширяется рабочий интервал, уменьшаются энергозатраты и становится более устойчивым технологический режим. Это особенно важно для экзотермических реакции.
3)Селективность-возможное ускорение основной реакции при наличии побочных взаимодействий.
4)устойчивость к ядам-частичное или полное потеря его активности в результате действия некоторых примесей. Если после вывода из системы каталитического яда, активность восстанавливается-обратимое отравление, если не восстанавливается-не обратимое
5. Однородность и воспроизводимость технологии производства
6. экологичность
7 Экономичность (себестоимость катализатор меньше 1% от всего процесса)
Причины потери активности
1.Перегрев-приводит к процессам рекристализации ,плавления, спекания, в результате чего уменьшается активность катализатора
2.Экранирование нового катализатора механическими примесями-пылью, маслами.
3.В органических производствах образовываются высокоуглеродистые пленки, которые покрывают поверхность катализатора
Требования: активность, селективность, низкая температура зажигания, устойчивость к кат.ядам, термостойкость, механическая прочность, большая теплопроводность, доступность и дешевизна
Гомогенный катализ
Катализ является гомогенным, если катализатор образует с компонентами одну фазу. Реакции такого типа происходит в жидких и газообразных средах.
Увеличение скорости реакции обусловлено снижением энергии активации за счет применения
Скорость гомогенного катализа пропорционально концентрации катализатора в системе, а ее зависимость т основных параметров определяется закономерностями кинетики гомогенных реакции. Интенсивность в гомогенном катализе выше чем в гетерогенном. Основной недостаток –трудность разделения продукта и катализатора, при этом теряется катализатор и загрязняется продукт.
Способы получения Катализаторов
Стабильность свойств катализаторов определяется способом получения катализаторов.
Катализатор контактной массы, состоит из катализатора, активаторов(промоторов) и носителей. Промоторы усиливают активность контактной массы.

1) метод осаждения гидроксидов или карбонатов из растворов их солей с последующими формированием и термообработкой
Такие катализаторы называют осаждёнными.

Формовка даёт фору катализатора гранулы таблетки кольца

Катализаторы смешения
3)