Материал: Lysenko_physics_lek_2

æ |
|
1 |
|
|
|
1 ö |
(n = 6, 7, 8, ...) . |
|
|||
серія Пфунда w = Rç |
|
|
|
- |
|
|
|
÷ |
|
||
|
|
|
|
|
|
|
|||||
è 52 |
|
|
|
|
n2 ø |
|
|
||||
Частоти усіх ліній спектра водневого атома можна подати однією формулою |
|
||||||||||
æ |
1 |
|
|
|
|
1 |
ö |
|
|||
w = Rç |
|
|
|
|
- |
|
|
÷ , |
(78.3) |
||
|
|
|
|
n2 |
|||||||
è m2 |
|
|
ø |
|
|||||||
де m має значення 1 для серії Лаймана, 2 – для серії Бальмера і т.д. Для заданого m число n
набуває всіх цілих значень, починаючи |
з |
m +1. Вираз |
(78.3) називають узагальненою |
||||
формулою Бальмера. |
|
|
|
|
|
||
При зростанні n частота лінії в кожній серії прямує до граничного значення R / m2 , |
|||||||
яке називається межею серії (на рис. 78.1 символом H∞ позначена межа серії Бальмера). |
|||||||
2 Візьмемо ряд значень виразів T (n) = R / n2 : |
|
||||||
|
R |
, |
R |
, |
R |
, ... |
(78.4) |
|
2 |
2 |
2 |
||||
1 |
|
2 |
3 |
|
|
||
Частота будь-якої лінії спектра водню може бути подана у вигляді різниці двох чисел ряду (78.4). Ці числа називають спектральними термами, або просто термами. Так, наприклад, частота першої лінії серії Бальмера дорівнює T (2) −T (3) , другої лінії серії Пфунда
T (5) −T (7) і т.д.
Вивчення спектрів інших атомів показало, що частоти ліній і в цьому випадку можуть
бути подані у вигляді різниці двох термів: |
|
w = T1(m) -T2 (n) . |
(78.5) |
Формула (78.5) виражає основний закон спектроскопії, встановлений емпірично в
1908 р., який називається комбінаційним принципом Рітца. Принцип Рітца полягає у тому,
що все різноманіття спектральних ліній атома може бути отримане шляхом попарних комбінацій набагато меншого числа величин, які називаються спектральними термами.
Частота кожної спектральної лінії дорівнює різниці двох термів (78.5). Однак терм T (n) для
інших атомів звичайно має більш складний вигляд, ніж для водневого атома. Крім того, перший і другий члени формули (78.5) беруться з різних рядів термів.
§ 79 Борівська теорія воднеподібного атома. Узагальнена формула Бальмера. Стала Рідберга. Недоліки теорії Бора [3]
1 Використовуючи постулати (Бора), умови квантування орбіт та деякі закони класичної механіки, Бор створив напівкласичну теорію воднеподібного атома. Розглянемо детально цю теорію.
Відповідно до моделі атома Резерфорда електрон у воднеподібному атомі рухається в полі атомного ядра із зарядом Ze по колу під дією сили Кулона. При Z = 1 така система відповідає атому водню, при інших Z – воднеподібному іону, тобто атому з порядковим номером Z , у якого вилучені всі електрони, крім одного. В атомі електрон під дією сили Кулона рухається по коловій орбіті радіуса r зі швидкістю υ з доцентровим прискоренням
aдоц = u2 / r . Рівняння другого закону Ньютона для електрона в цьому випадку має вигляд
m a |
|
= F , або m |
u2 |
= |
1 |
Ze2 |
. |
(79.1) |
|
|
r |
4pe0 |
r2 |
||||||
e |
доц |
К |
e |
|
|
|
|||
Також згідно з першим постулатом Бора електрон може рухатися тільки по стаціонарних орбітах, для яких момент імпульсу електрона L = meur відповідно до правила квантування орбіт задовольняє умову:
meur = nh (n =1, 2,3,...) . |
(79.2) |
162
Число n у виразі (79.1) називається головним квантовим числом, де me |
– маса електрона; |
||||||
υ - його швидкість; r – радіус орбіти; h – стала Планка. |
|
||||||
Система рівнянь (79.1) (79.2) повністю описує поведінку електрона у воднеподібному |
|||||||
атомі. |
|
|
|
|
|
|
|
Виключивши швидкість υ |
із рівнянь (79.1) |
і (79.2), отримаємо вираз для радіусів |
|||||
стаціонарних орбіт: |
|
|
|
|
|
|
|
r º r |
= 4pe |
|
h2 |
n2 (n =1, 2,3,...) . |
(79.3) |
||
0 m Ze2 |
|||||||
n |
|
|
|
|
|||
|
|
|
e |
|
|
|
|
Радіус першої орбіти ( n = 1) атома водню ( Z = 1) |
називається борівським радіусом. Його |
||||||
значення дорівнює |
|
|
|
|
|
|
|
|
r |
= 0,529×10−10 |
м. |
(79.4) |
|||
|
0 |
|
|
|
|
|
|
Відзначимо, що борівський радіус має порядок значення газокінетичних розмірів атома. Внутрішня енергія атома складається з кінетичної енергії електрона (ядро є
нерухомим) і енергії електростатичної взаємодії електрона з ядром:
|
|
|
|
|
m u2 |
1 |
|
|
|
Ze2 |
|
|
|
|
|||||||||
|
|
E = |
|
e |
|
|
- |
|
|
|
|
|
|
|
|
|
. |
|
|
|
|||
|
|
2 |
|
4pe0 r |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
З (79.1) випливає, що |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m u2 |
|
1 |
|
1 |
|
Ze2 |
|
|
|
|
|
|
|||||||
|
|
|
|
e |
|
|
= 2 |
|
|
|
|
|
|
|
r . |
|
|
|
|
||||
|
|
2 |
|
|
4pe0 |
|
|
|
|
|
|
|
|||||||||||
Отже, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
E = |
1 |
|
|
Ze2 |
|
- |
|
1 |
|
|
|
Ze2 |
= - |
|
|
1 |
|
Ze2 |
. |
||||
8pe0 |
|
|
r |
|
4pe0 |
|
|
r |
8pe0 |
|
r |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Підставивши сюди вираз (79.3) для r , знайдемо значення енергії атома на стаціонарних орбітах:
æ |
1 |
ö2 |
meZ |
2 |
e |
4 |
1 |
|
|
||
ç |
÷ |
|
|
|
|
||||||
E º En = -ç |
|
÷ |
|
|
|
|
|
|
(n =1, 2,3,...) . |
(79.5) |
|
4pe0 |
2h |
2 |
|
|
n |
2 |
|||||
è |
ø |
|
|
|
|
|
|
|
|||
Як бачимо, повна енергія воднеподібного атома визначається числом n . Саме тому число n отримало назву головного квантового числа.
При переході атома водню ( Z = 1 ) зі стану n в стан m випромінюється фотон, енергія якого визначається другим постулатом Бора
æ |
1 |
ö2 |
mee |
4 |
æ |
1 |
|
1 |
ö |
|||
ç |
÷ |
|
|
|||||||||
hw = En - Em = -ç |
|
÷ |
|
|
ç |
|
|
- |
|
|
÷ . |
|
4pe0 |
2h |
2 |
|
2 |
m |
2 |
||||||
è |
ø |
|
|
è n |
|
|
|
ø |
||||
Частота випромінюваного світла дорівнює
|
En - Em |
æ |
1 |
ö2 |
mee |
4 |
æ |
1 |
|
1 ö |
æ |
1 |
|
1 ö |
|||||||
|
ç |
÷ |
|
|
|
||||||||||||||||
w = |
|
= ç |
|
÷ |
|
|
ç |
|
|
- |
|
|
÷ |
= R ç |
|
|
- |
|
|
÷ . |
|
h |
4pe0 |
2h |
3 |
|
2 |
n |
2 |
|
2 |
n |
2 |
||||||||||
|
è |
ø |
|
|
è m |
|
|
|
ø |
è m |
|
|
|
ø |
|||||||
Ми прийшли до узагальненої формули Бальмера, причому для сталої Рідберга отримали значення
æ |
1 |
ö2 |
mee |
4 |
16 |
|
−1 |
|
|
|
ç |
÷ |
|
|
|
|
|||||
R = ç |
|
÷ |
|
|
= 2,07×10 |
c |
|
. |
(79.6) |
|
4pe0 |
2h |
3 |
|
|||||||
è |
ø |
|
|
|
|
|
|
|
||
Як бачимо, при підстановці у вираз (79.6) числових значень me , e |
і h отримуємо величину, |
|||||||||
що дуже добре узгоджується з експериментальним значенням сталої Рідберга. 163
2 Теорія Бора була великим кроком у розвитку теорії атома. Вона пояснила ряд експериментальних фактів, стала потужним стимулом для проведення багатьох експериментальних досліджень, які принесли важливі результати. Навіть у тих випадках (а таких випадків була більшість), коли теорія не могла кількісно пояснити багато явищ, два постулати Бора були керівною ниткою при класифікації і якісній інтерпретації цих явищ. На їх основі, наприклад, був класифікований величезний емпіричний матеріал атомної й молекулярної спектроскопії.
Після перших успіхів теорії Бора усе чіткіше проявлялися її недоліки. Особливо тяжкою була невдача при побудові теорії атома гелію – одного з найпростіших атомів після атома водню.
Самою слабкою стороною теорії Бора була її внутрішня логічна суперечливість: вона не була ні послідовно класичною, ні послідовно квантовою теорією. Після відкриття хвильових властивостей речовини стало зрозуміло, що теорія Бора, яка опирається на класичну механіку, є перехідним етапом на шляху до створення послідовної квантової теорії атомних явищ.
ТЕМА 14 ХВИЛЬОВІ ВЛАСТИВОСТІ МІКРОЧАСТИНОК
§ 80 Гіпотеза де Бройля. Довжина хвилі де Бройля для електрона, що вільно рухається [6, 11]
1 У результаті поширення уявлень про природу світла з'ясувалося, що світло виявляє корпускулярно хвильовий дуалізм (подвійність). В одних явищах проявляється його хвильова природа, і він веде себе як електромагнітна хвиля (інтерференція, дифракція), в інших явищах проявляється корпускулярна природа світла, і він веде себе як потік фотонів (фотоефект, явище Комптона).
У 1924 р. де Бройль висунув сміливу гіпотезу, що дуалізм не є особливістю тільки світла. Він припустив, що і частинки речовини поряд з корпускулярними властивостями мають також і хвильові (корпускулярно-хвильовий дуалізм частинок). Де Бройль переніс на частинки речовини такі самі правила переходу від корпускулярних характеристик до хвильових, які є справедливими у випадку світла.
Так відомо, що фотон світла має енергію
E = hω |
(80.1) |
й імпульс |
|
p = 2πh / λ , |
(80.2) |
які пов’язані з частотою ω та довжиною λ світлової хвилі.
За гіпотезою де Бройля рух будь-якої частинки пов'язаний із хвильовим процесом, довжина хвилі визначається аналогічно до (80.2)
|
λ = 2πh / p |
(80.3) |
||
а частота – аналогічно до (80.1) |
|
|||
|
|
|
. |
(80.4) |
|
|
ω = E / h |
||
Формули (80.3) та (80.4) визначають довжину та частоту хвилі де Бройля (хвилі, що відповідає частинці речовини).
2 Все викладене вище є гіпотетичним і тому не має доказової сили. Точним доведенням або спростуванням отриманих результатів може бути тільки дослід. У яких саме явищах природи можуть виявитися хвильові властивості речовини, якщо вони дійсно існують? Незалежно від фізичної природи хвиль до таких явищ відносять інтерференцію й дифракцію. Безпосередньо величиною, яка тут досліджується, є довжина хвилі λ . У всіх випадках довжини хвиль де Бройля визначаються формулою (80.3). Застосуємо її до
164
нерелятивістського руху частинок. Для електронів з масою me , які прискорені різницею потенціалів U , імпульс визначається із закону збереження енергії
|
p2 |
|
m υ2 |
|
||||
|
|
= |
|
e |
= eU , |
|
||
|
2m |
|
||||||
|
|
2 |
|
|
|
|
||
|
e |
|
|
|
|
|
|
|
тобто |
|
|
|
|
|
|
|
|
|
p = |
|
|
. |
|
(80.5) |
||
|
|
2eUme |
||||||
Тоді з (80.3) отримаємо |
|
|
|
|
|
|
|
|
|
λ = 2πh / |
|
. |
(80.6) |
||||
|
2eUme |
|||||||
Визначимо довжину хвилі де Бройля для електронів, які прискорені напругою від 100 В
до 10 кВ. Підставивши у співвідношення (80.6) відповідні числа, отримаємо, що довжина хвилі де Бройля такого електрона змінюється від 0,39 нм до 0,012 нм, тобто відповідає рентгенівському діапазону.
Таким чином, довжина хвилі де Бройля для електронів, які прискорені напругою від 100 В до 10 кВ, мають такий самий порядок, що й довжини хвиль рентгенівських променів. Тому дифракцію таких електронів потрібно намагатися шукати методами, аналогічними до тих, які застосовуються у випадку рентгенівських променів. Однак гіпотеза де Бройля уявлялась настільки фантастичною, що порівняно довго ніхто з експериментаторів не намагався піддати її експериментальній перевірці.
§ 81 Досліди Девісона й Джермера. Досліди Томсона й Тартаковського [3] 1 Гіпотеза де Бройля була підтверджена експериментально в дослідах Девісона й
Джермера, а також Томсона (1927) та Тартаковського. |
|
|
|
|
|
Девісон і Джермер досліджували в 1927 р. відбиття |
|
|
|
|
|
електронів від монокристала нікелю, що належить до кубічної |
|
|
|
|
До |
системи. Вузький пучок моноенергетичних електронів |
|
|
ϕ |
гальва- |
|
спрямовувався на поверхню монокристала, який був |
|
|
|
|
нометра |
|
|
|
|
||
відшліфований перпендикулярно до великої діагоналі |
|
|
|
|
|
кристалічної комірки. Відбиті електрони вловлювалися |
|
|
|
|
|
циліндричним електродом, який був приєднаним до |
|
|
|
|
|
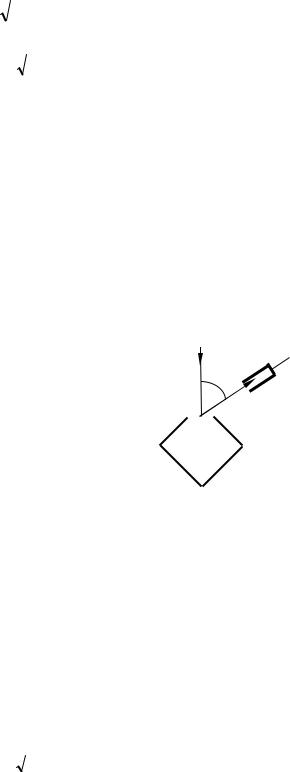
гальванометра (рис. 81.1). Інтенсивність відбитого пучка |
Рисунок 81.1 |
|
|||
оцінювалася за силою електричного струму, що проходить |
|
||||
|
|
|
|
|
|
через гальванометр. Змінювалися швидкість електронів і кут ϕ . |
На рис. 81.2 |
показана |
|||
залежність сили струму, яка вимірювалася гальванометром, від кута ϕ при різних енергіях
електронів.
Вертикальна вісь на графіках визначає напрям електронного пучка, що падає на монокристал. Сила струму в заданому напрямку відображається довжиною відрізка, який проведено від початку координат до точки перетину з кривою. З рисунка бачимо, що розсіювання виявилося особливо інтенсивним при певному значенні кута ϕ . Цей кут
відповідав відбиттю від атомних площин, відстань d між якими була відома з рентгенографічних досліджень. При даному ϕ сила струму виявилася особливо значною при
прискорювальній напрузі, яка дорівнювала 54 В. Обчислена за формулою де Бройля довжина хвилі електрона
λ = |
h |
= |
|
h |
|
, |
(81.1) |
|
p |
|
|
|
|||||
2meU |
||||||||
|
|
|
|
|
|
165