Материал: LS-Sb88915
сятки микрограмм на литр. В загрязненных водах концентрация фосфора достигает нескольких миллиграмм на литр.
Определение ортофосфатов фотометрическим методом основано на образовании в кислой среде желтого фосфорно-молибденового гетерополианиона [P(Mo2O7)6]7− с последующим восстановлением его до «молибденовой сини».
Реакция образования комплекса, проходящая в присутствии серной кислоты, выглядит следующим образом:
H3PO4 +12(NH4)2MoO4 +14H2O ® H7[P(Mo2O7)6] + 24(NH4)OH .
Образовавшийся комплекс имеет желтую окраску. Для перевода его в форму, удобную для колориметрического и фотометрического определения,
проводят восстановление комплекса (Мо6+ частично восстанавливается до Мо5+) аскорбиновой кислотой в присутствии сурьмяновиннокислого калия (калий антимонилтартрат) до образования комплекса, окрашенного в синий цвет.
Минимально определяемая концентрация фосфора – 5 мкг/л. Закон Бера соблюдается до концентрации фосфора в растворе порядка 0.5 мг/л (более концентрированные пробы необходимо разбавлять).
Исходные реактивы и приготовление рабочих растворов
1. Для приготовления раствора молибдата аммония ((NH4)2MoO4 × 4H2O ) 15 г соли растворяют в 500 мл дистиллированной воды. После приготовления раствор отфильтровывают.
2. Для приготовления раствора серной кислоты (H2SO4) к 500 мл ди-
стиллированной воды добавить 140 мл концентрированной серной кислоты. Раствор разбавить до 1 л.
3. Для приготовления раствора аскорбиновой кислоты (С6Н8О6) 13.5 г
кислоты растворить в 250 мл дистиллированной воды. Раствор хранить в холодильнике.
4. Для приготовления раствора сурьмяновиннокислого калия ( K(SbO)C4H4O6 × 12 H2O ) 0.34 г вещества растворить в 250 мл дистиллиро-
ванной воды.
Приготовление смешанного реактива
К 20 мл раствора молибдата аммония последовательно добавляют 50 мл раствора серной кислоты, 20 мл раствора аскорбиновой кислоты и 10 мл раствора сурьмяновиннокислого калия. Смесь тщательно перемешивают. Полученный раствор хранят не более 6 ч или в холодильнике.
16

Ход определения
1.Пипеткой Мора отбирают 25 мл анализируемой пробы и помещают в мерную колбу объемом 50 мл.
2.Добавляют 2.5 мл смешанного реактива. Раствор перемешивают, доводят до метки дистиллированной водой и перемешивают снова.
3.Через 10…15 мин измеряют его оптическую плотность на спектрофотометре (СФ-26) при 882 нм (фотоэлемент К) в кюветах толщиной 5 см (раствор сравнения – дистиллированная вода). При измерении на фотоэлектроколориметре (КФК-2) используют светофильтр 750 нм. В качестве холостого раствора используется смесь реагентов.
4.На основании найденных значений оптической плотности по градуировочному графику находят значение концентрации ортофосфата в растворе.
Построение градуировочного графика
1. В мерные колбы объемом 50 мл вносят мерными пипетками по 0.5; 1.0; 2.0; 4.0; 5.0; 7.5 и 10.0 мл стандартного раствора дигидрофосфата калия КН2РО4 концентрации 1 мг/л (стандартный раствор готовят непосредственно перед использованием).
2. В каждую колбу добавляют по 2,5 мл смешанного реагента, растворы доводятся до метки дистиллированной водой и тщательно перемешиваются.
2. В полученном ряду стандартных растворов с концентрациями фосфора 10; 20; 40; 80; 100; 150 и 200 мкг/л определяют оптическую плотность рас-
творов. Измерения проводят относительно холостого раствора, представляющего собой смесь реагентов, и строят градуировочный график.
6. ОПРЕДЕЛЕНИЕ АММОНИЯ
Ионы аммония определяют фотометрически по реакции с реактивом Несслера – щелочным раствором тетрайодмеркурата калия. В результате реакции образуется желто-коричневый коллоидный раствор NН2Нg2I3:
NH+4 + 2K2HgI4 + 2KOH = NH2Hg2I3 + 5KI + 2H2O + K+.
Определению аммония мешают ионы кальция и магния, поэтому перед анализом их маскируют добавлением виннокислого натрия-калия – сегнетовой
соли (KNaC4H4O6·4H2O). Диапазон определяемых концентраций ионов ам-
мония – 0.05…4.0 мг/л.
Исходные реактивы и приготовление рабочих растворов
17
1. Для приготовлений раствора сегнетовой соли – KNaC4H4O4 · 4H2O –
растворяют 50 г соли в дистиллированной воде при нагревании, доводят раствор до 100 мл, перемешивают, фильтруют, добавляют 5 мл 10 %-го раствора NaOH и кипятят 30 мл для удаления следов аммиака, охлаждают, после чего переводят в мерную колбу объемом 100 мл и доводят раствор до метки дистиллированной водой. Затем тщательно перемешивают.
2.Реактив Несслера – щелочной раствор тетрайодмеркурата калия (K2HgI4) – торговый препарат.
3.Безаммиачную воду получают пропусканием дистиллированной воды через колонку с ионообменной смолой КУ-2 или кипячением в течение 1 ч дистиллированной воды с добавкой щелочи (25 мл 5 %-го раствора NaOH на 1 л воды).
Ход определения
1.В мерную колбу объемом 50 мл пипеткой Мора отбирают 10 мл анализируемой пробы и добавляют 0.2 мл раствора сегнетовой соли и 0.2 мл реактива Несслера. Доводят до метки дистиллированной водой и тщательно перемешивают.
2.Оптическую плотность измеряют при 400 и 425 нм (фотоэлемент Ф) в
кювете толщиной 1 см (раствор сравнения – смесь реагентов, приготовленная аналогичным способом).
3. На основании найденных значений оптической плотности по градуи-
ровочному графику находят значение концентрации аммиака в растворе.
Построение градуировочного графика
1. В мерные колбы объемом 50 мл вносят мерными пипетками по 1.0; 2.0; 3.0; 4.0; 6.0 и 10.0 мл стандартного раствора хлорида аммония концен-
трации 5 мг/л (раствор готовят непосредственно перед использованием, раз-
бавляя раствор концентрации 500 мг/л) и разбавляют дистиллированной без-
аммиачной водой, доводя каждый раствор до объема 50 мл.
2.Каждый раствор перемешивают.
3.Оптическую плотность стандартных растворов определяют по методике,
описанной ранее, используя в качестве холостого раствора смесь реагентов. 4. Строят градуировочный график, где A = f (c) .
18

7.ОПРЕДЕЛЕНИЕ НИТРИТОВ
Вкислой среде нитриты взаимодействуют с сульфаниламидом с образо-
ванием солей диазония (реакция диазотирования).
NO2- + H2N |
O |
|
|
|
|
|
NH2 + HCl |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl- + H2O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
S |
|
|
|
|
|
|
|
|
|
H2N |
|
S |
|
|
|
|
|
|
|
N |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Соль диазония реагирует с N-(1-нафтил)-этилендиамином с образованием интенсивно окрашенного в розовый цвет азосоединения (реакция азосочета-
ния). Реакция специфична. Закон Бера соблюдается для в концентрационном диапазоне 3…350 мкг/л.
Исходные реактивы и приготовление рабочих растворов
1. Для приготовления раствора сульфаниламида растворяют 5 г соеди-
нения в дистиллированной воде, подкисляют 50 мл концентрированной со-
ляной кислоты, переводят в мерную колбу объемом 500 мл. Доводят до мет-
ки дистиллированной водой и перемешивают.
2. Для приготовления раствора N-(1-нафтил)-этилендиамина 0.5 г соеди-
нения растворяют в дистиллированной воде, переводят в мерную колбу объ-
емом 500 мл. Доводят до метки дистиллированной водой и перемешивают.
Ход определения
1.Пипеткой Мора в мерную колбу объемом 50 мл отбирают 25 мл анализируемой пробы, в которую добавляют 0.5 мл раствора сульфаниламида и через 5 мин 0.5 мл раствора N-(1-нафтил)-этилендиамина. Раствор доводят до метки дистиллированной водой.
2.Смесь перемешивают в течение 10…15 мин.
3.В кювете толщиной 1 см измеряют оптическую плотность раствора при 540 нм (фотоэлемент Ф). Холостой раствор – смесь реагентов.
4.На основании найденных значений оптической плотности по градуировочному графику находят значение концентрации нитрита в растворе.
Построение градуировочного графика
1. В мерные колбы объемом 50 мл мерными пипетками вносят 0.1; 0.2; 0.4; 0.6; 0.8; 1.0; 1.5 и 2.0 мл стандартного раствора нитрита натрия (NaNO2)
концентрации 5 мг/л (стандартный раствор готовят непосредственно перед использованием, разбавляя раствор концентрации 250 мг/л), доводят раствор до метки дистиллированной водой и перемешивают.
19
2. Оптическую плотность стандартных растворов с концентрациями нитрита 10; 20; 40; 60; 80; 100; 150 и 200 мкг/л определяют по методике, опи-
санной ранее, используя в качестве холостого раствора смесь реагентов. 3. Строят градуировочный график, где A = f (c) .
8. ОПРЕДЕЛЕНИЕ НИТРАТОВ
Ионы нитратов определяют фотометрически после их индивидуального концентрирования (выделения) новым полимерным сорбентом – полистирол- азо-2,3-диаминобензолом, представляющим собой тонкодисперсный порошок темно-коричневого цвета, нерастворимый в воде, кислотах, щелочах и органических растворителях. Структурная формула фрагмента полимерной молекулы сорбента выглядит следующим образом:
|
H2N |
NH2 |
HC |
N N |
|
CH2 |
|
|
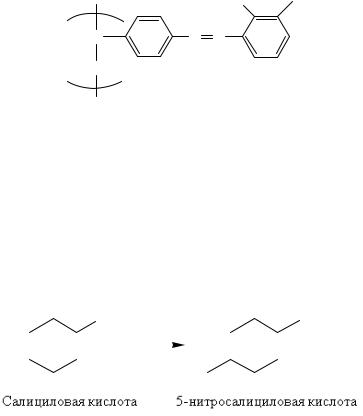
Количественное извлечение иона NO3− этим сорбентом (R = 98…100 %) происходит в статических условиях в интервале значений рН 1–2 при t = = 20 ± 2 °С в течение 25…30 мин. Определения массовой концентрации нит- рат-ионов основано на реакции синтеза: при взаимодействии нитрат-ионов с 1 %-ным спиртовым раствором салициловой кислоты образуется 5-нитроса- лициловая кислота желтого цвета:
|
COOH |
|
|
|
COOH |
|||||
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
+ OH- |
|
NO3- + |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
O2N |
|||||
Предел обнаружения составляет 10–3…10–6 %.
Исходные реактивы и приготовление рабочих растворов
1. Для приготовления 0.1 н. раствора нитрата серебра в 50 мл дистиллированной воды растворяют 1.433 г нитрата серебра, затем переводят в мерную колбу объемом 100 мл, доводят до метки дистиллированной водой и тщательно перемешивают.
20