Материал: LS-Sb88915

МИНОБРНАУКИ РОССИИ
–––––––––––––––––––––––––––––––––
Санкт-Петербургский государственный
электротехнический университет «ЛЭТИ»
–––––––––––––––––––––––––––––––––––––––
О. В. РАХИМОВА В. В. ГУСАРОВ O. A. ЛЕБЕДЕВ
АБСОРБЦИОННЫЕ МЕТОДЫ ХИМИЧЕСКОГО АНАЛИЗА РАСТВОРОВ
Электронное учебное пособие
Санкт-Петербург
Издательство СПбГЭТУ «ЛЭТИ»
2012

УДК 54.062 ББК 24.4
Г96
Рахимова О. В., Гусаров В. В., Лебедев О. А.
Г96 Абсорбционные методы химического анализа растворов: Электронное учеб. пособие. СПб.: Изд-во СПбГЭТУ «ЛЭТИ», 2012. 28 с.
ISBN 978-5-7629-1313-3
Содержит сведения о физико-химических основах абсорбционного метода анализа растворов. Приводится описание работы спектрофотометра. Дается подробное описание порядка работы при химическом анализе некоторых ионов, растворенных в воде, с использованием спектрофотометрического метода.
Предназначено для студентов технических вузов, специализирующихся в области экологии и защиты окружающей среды. Кроме того, пособие может быть полезно для инженерно-технических работников, связанных с анализом экологической ситуации в лабораторных и полевых условиях.
Рецензенты: кафедра канд. хим. наук В. А. Кескинов (кафедра технологии редких элементов и наноматериалов на их основе (СП6ГТИ(ТУ)).
УДК 54.062 ББК 24.4
Утверждено редакционно-издательским советом университета
в качестве электронного учебного пособия
ISBN 978-5-7629-1313-3 |
© СПбГЭТУ «ЛЭТИ», 2012 |
2
ВВЕДЕНИЕ
Основной задачей аналитической химии является определение химического состава веществ и их смесей. Аналитический процесс проходит на разных иерархических уровнях:
1.Определение общих физико-химических принципов анализа.
2.Создание конкретного аналитического метода.
3.Разработка индивидуальной аналитической методики, содержащей точные инструкции по проведению отдельного определения (рабочей прописи).
Рабочая пропись должна содержать подробное описание операции пробоотбора, пробоподготовки, порядка проведения измерений, перечня необходимых реактивов, данных об области определяемых концентраций и селективности, об источниках погрешности и точности анализа, о затратах времени на проведение анализа и его стоимости.
Независимо от метода любой химический анализ состоит из следующих стадий:
– пробоотбора;
– пробоподготовки;
– измерения (определения);
– оценки результатов.
Так как точность любой методики определяется максимальной погрешностью ее отдельных стадий, то для рациональной аналитической работы необходимо, чтобы относительные погрешности всех стадий были соизмеримы. Обычно лимитирующей точность анализа является стадия измерения. Поэтому переход от одного метода измерения к другому вызван прежде всего необходимостью повышения точности химического анализа. В частности, это является причиной перехода от колориметрического метода к фотометрии в рамках одной группы методов, базирующихся на поглощении (абсорбции) светового потока.
1.ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ АБСОРБЦИОННЫХ МЕТОДОВ ХИМИЧЕСКОГО АНАЛИЗА
Абсорбционные методы химического анализа (от лат. sarbeo – по-
глощаю) основаны на явлении ослабления светового потока при его прохождении через поглощающую среду. Поглощение света веществом проис-
ходит вследствие электронного возбуждения составляющих его атомов и мо-
3
лекул. Энергия квантов поглощаемого света – фотонов – равна разности энергий возбужденного и основного электронных состояний атомов (ионов). Следует отметить, что при поглощении света возбуждаются только электроны, находящиеся на внешних – валентных – орбиталях атомов. Кроме того, в молекулах и комплексах видимый свет может также возбуждать неспаренные электроны, π-электронные пары и d-электроны центрального атома.
Закон Ламберта–Бера. Рассмотрим однородное тело, на которое падает монохроматический поток излучения (монохроматическим называют излучение с определенной длиной волны). Интенсивность света, прошедшего через вещество, может быть определена на основании соотношения, впервые предложенного Бугером:
In(I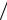 I0 ) = −kl,
I0 ) = −kl,
где I0 – интенсивность падающего пучка монохроматического светового из-
лучения, Вт/м2; I – интенсивность света, прошедшего через раствор, Вт/м2; k – константа; l – толщина поглощающего слоя. Отношение
T = I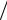 I0
I0
называют пропусканием, а
A= −lgT
–поглощением (оптической плотностью).
Несложными преобразованиями приведенных выражений можно вывести закон Ламберта:
A = lg(I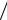 I0 ) = −lg(T ) = al,
I0 ) = −lg(T ) = al,
где А – оптическая плотность раствора, зависящая от длины волны падающего света и характеристик поглощающей среды; а – показатель поглощения раствора единичной концентрации.
Для смеси веществ величина а пропорциональна концентрации поглощающего вещества в растворе (закон Бера):
a = εc,
где ε – молярный десятичный коэффициент поглощения, в настоящее время чаще называемый коэффициентом экстинкции, в единицах СИ (ИЮПАК) выражается в м2/моль, в справочной литературе обычно используется единица измерения л/моль·см; с – концентрация поглощающего вещества, моль/л.
Комбинация последних двух выражений представляет собой закон Лам-
берта– Бера:
4
A = lg(I0 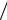 I ) = εcl.
I ) = εcl.
Данный закон справедлив только для разбавленных растворов, в которых концентрация определяемого вещества не превышает 0,01 моль/л, так как выполняется лишь при условии постоянства коэффициента преломления среды, значение которого зависит от концентрации веществ в растворе. Подобная зависимость коэффициента преломления приводит к нелинейности градуировочного графика при использовании абсорбционных методов для количественного химического анализа веществ в растворах.
2. КОЛОРИМЕТРИЯ
Колориметрией называется метод определения концентрации вещества в растворе по его окраске в видимой области спектра. Принцип колори-
метрии обычно используется в тест-методах контроля качества воды в полевых условиях.
Интенсивность окраски пробы при колориметрическом методе анализа визуально сравнивают с интенсивностью окраски ряда стандартных растворов известной концентрации. В качестве стандартов могут быть использованы и растворы одинаковой концентрации, но с разной толщиной поглощающего слоя. В соответствии с законом Ламберта–Бера для двух растворов одного и того же вещества в одном и том же растворителе при одинаковых значениях оптической плотности выполняется соотношение
c1l1 = c2l2,
где c1, c2 – концентрации поглощающего вещества в первом и втором раство-
рах; l1, l2 – толщина первого и второго поглощающих слоев соответственно.
Если известны значения c1 и l1 то, зная l2 , можно рассчитать c2.
|
|
Таблица 2.1 |
Дополнительные цвета в видимой области |
||
|
|
|
Поглощаемый свет |
Длина волны λ, нм |
Наблюдаемая окраска |
Фиолетовый |
40 |
Желто-зеленая |
Синий |
450 |
Желтая |
Сине-зеленый |
500 |
Красная |
Зеленый |
550 |
Пурпурная |
Желтый |
600 |
Синяя |
Оранжево-красный |
650 |
Сине-зеленая |
Красный |
700 |
Сине-зеленая |
Темно-красный |
750 |
Сине-зеленая |
5