Материал: 59-64
Вопрос 59 Цикл лимонной кислоты: последовательность реакций и характеристика ферментов. Роль цикла в метаболизме.
Цикл лимонной кислоты (цитратный цикл, цикл Кребса, цикл трикарбоновых
кислот, ЦТК) – заключительный этап катаболизма, в котором углерод ацетильного остатка ацетил-КоА окисляется до 2 молекул СO2.
Атомы водорода, освобождающиеся в окислительно-восстановительных реакциях,
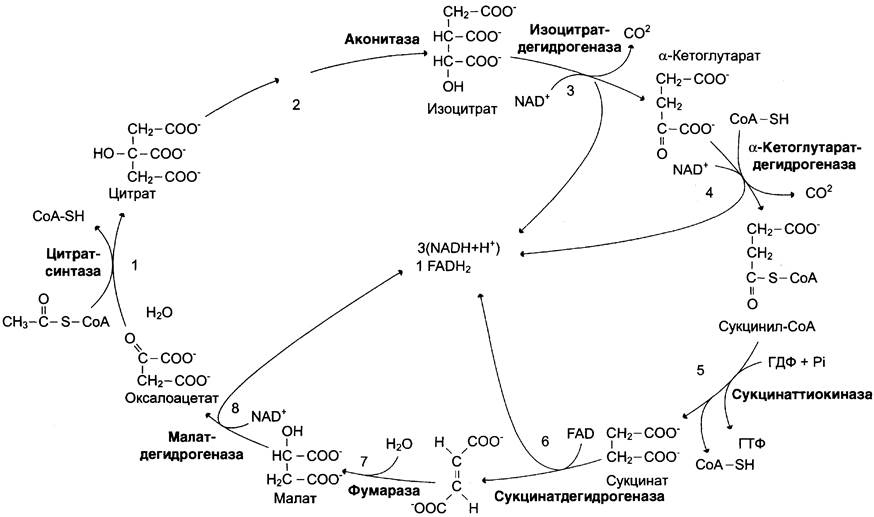
доставляются в ЦПЭ при участии NAD- и FAD-зависимых дегидрогеназ, в результате чего происходят синтез воды и окислительное фосфорилирование АДФ. Связь между атомами углерода в ацетил- КоА устойчива к окислению. В условиях организма окисление ацетильного остатка происходит в несколько этапов, образующих циклический процесс из 8 реакций.
1. Образование цитрата: углеродный атом метильной группы ацетил-КоА
связывается с карбонильной группой оксалоацетата; одновременно расщепляется тиоэфирная связь и освобождается коэнзим A. Реакция сопровождается потерей большого количества энергии в виде теплоты.
Фермент: цитратсинтаза, фермент, локализованный в матриксе митохондрий.
2. Превращение цитрата в изоцитрат: обратимая реакция.
Фермент: аконитаза, назван по промежуточному продукту, цис-аконитовой кислоте, которая предположительно образуется в реакции (не обнаруживается в свободном виде, так как не отделяется от активного центра фермента до завершения реакции).
3. Окислительное декарбоксилирование изоцитрата: обр. α-кетоглутарата
Фермент: изоцитратдегидрогеназа.
Существуют 2 формы изоцитратдегидрогеназы: одна содержит в качестве
кофермента NAD+ (локализован в митохондриях и участвует в ЦТК), вторая – NADP+. (присутствует и в митохондриях, и в цитоплазме, играет иную метаболическую роль).
Это самая медленная реакция цитратного цикла.
АДФ – аллостерический активатор фермента.
4. Окислительное декарбоксилирование α-кетоглутарата: α-КГ подвергается
окислительному декарбоксилированию с образованием сукцинил-КоА, СO2 и NADH + Н+. Фермент: α-кетоглутаратдегидрогеназный комплекс, который по структуре и функциям сходен с пируватдегидрогеназным комплексом (ПДК).
Подобно ПДК, он состоит из 3 ферментов:
α-кетоглутаратдекарбоксилазы
дигидролипоилтранссукцинилазы
дигидролипоилдегидрогеназы.
В этот ферментный комплекс входят 5 коферментов: тиаминдифосфат, кофермент А, ли- поевая кислота, NAD+ и FAD.
Отличие этой ферментной системы от ПДК: она не имеет сложного механизма
регуляции, какой характерен для ПДК (в этом комплексе отсутствуют регуляторные субъединицы)
5. Превращение сукцинил-КоА в сукцинат
Фермент: сукцинаттиокиназа
Сукцинил-КоА – высокоэнергетическое соединение. В митохондриях разрыв
тиоэфирной связи сукцинил-КоА сопряжён с реакцией фосфорилирования гуанозиндифосфата (ГДФ) до гуанозинтрифосфата (ГТФ). Промежуточный этап реакции – фосфорилирование молекулы фермента по одному из гистидиновых остатков АЦ. Затем остаток фосфорной кислоты присоединяется к ГДФ с образованием ГТФ.
6. Дегидрирование сукцината: он превращается в фумарат
Фермент: сукцинатдегидрогеназы – флавопротеин, молекула которого содержит прочно связанный кофермент FAD. Прочно связана с внутренней митохондриальной мембраной.
Состоит из 2 субъединиц, одна из которых связана с FAD.
Обе субъединицы содержат железосерные центры; одна – Fe2S2, а другая – Fe4S4. В железосерных центрах атомы железа меняют свою валентность, участвуя в транспорте электронов.
7. Образование малата из фумарата
Фермент: фумараза – олигомерный белок, состоящий из 4 идентичных ППЦ. Он расположен в матриксе митохондрий. Это ф. с абсолютной субстратной специфичностью: катализирует гидратацию только трансформы фумарата.
8. Дегидрирование малата: обр. оксалоацетат
Фермент: NAD-зависимая малатдегидрогеназа, содержащаяся в матриксе митохондрий.
В
цитозоле содержится изоформа
малатдегидрогеназы, также NАD-зависимая,
но не принимающая участие в цитратном
цикле.
Роль цитратного цикла:
1. Энергетическая
Генерация атомов водорода для работы дыхательной цепи, а именно трех молекул НАДН и одной молекулы ФАДН2,
Синтез одной молекулы ГТФ (эквивалентна АТФ).
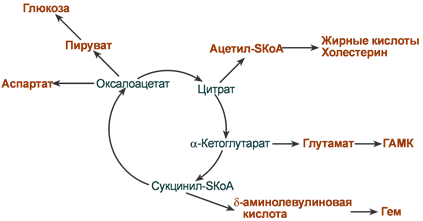
2. Анаболическая. В ЦТК образуются:
Предшественник гема – сукцинил-SКоА,
Кетокислоты, способные превращаться в аминокислоты – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой,
Лимонная кислота, используемая для синтеза жирных кислот,
Оксалоацетат, используемый для синтеза глюкозы.
Вопрос 60 Цикл лимонной кислоты, схема процесса. Связь цикла с целью переноса электронов и протонов. Регуляция цикла лимонной кислоты. Анаболические и анаплеротические функции цитратного цикла.
Цикл (см. 59 вопрос)
Связь окислительного декарбоксилирования пирувата с ЦПЭ: окислит.
декарбокс-е пирувата (ЦТК) сопровождается образованием NADH, поставляющим электроны в дыхательную цепь и обеспечивающим синтез 3 молей АТФ на 1 моль пирувата путём окислительного фосфорилирования.
Так как отношения АДФ/АТФ и NADH/NAD+ в клетке относительно постоянны,
ускорение утилизации АТФ приводит к повышению концентрации АДФ и ускорению окисления NADH в дыхательной цепи. Повышение концентрации NAD+, стимулирует окислительное декарбоксилирование пирувата.
И наоборот, повышение концентрации АТФ и NADH снижает скорость процесса.
Т.о., изменения отношений АДФ/АТФ и NADH/ NAD+ – важнейшие сигналы, отражающие энергетические потребности клетки и регулирующие скорость окислительного декарбоксилирования пирувата.
Каталитическая активность пируват-дегидрогеназного комплекса снижается, когда
в клетках имеется достаточно "топлива" в виде жирных кислот и ацетил-КоА.
Анаболические и анаплеротические функции цитратного цикла.
Цикл лимонной кислоты – амфиболический, т.к. помимо окисления в-в, там
происходит обр-е субстратов для других метаболических путей.
Промежуточные продукты цикла: α-кетоглутарат, сукцинат, оксалоацетат
могут использоваться для синтеза заменимых аминокислот.
Убыль промежуточных продуктов цикла восполняется в реакциях, катализируемых
специфическими ферментами. Реакции, забирающие промежуточные продукты из цикла и восполняющие их убыль, находятся в состоянии равновесия, так что концентрация продуктов в митохондриях постоянна.
Анаплеротические реакции – р., обеспечивающие пополнение фонда
промежуточных продуктов ЦТК
Важнейшая из них: реакция синтеза оксалоацетата из пирувата.
Фермент: пируваткарбоксилаза (олигомерный фермент, содержащий 4 простетические группы, представленные биотином).
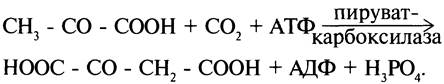
Если для ЦТК не хватает оксалоацетата или другого промежуточного продукта, то
карбоксилирование пирувата ускоряется (источник энергии АТФ).
Реакция протекает в 2 стадии.
Происходит активация СO2 путём присоединения к одному из атомов азота в молекуле биотина. Эта реакция сопряжена с гидролизом АТФ.
АТФ + СO2+ Е-биотин + Н2O → АДФ + Н3РO4 + Е-биотин-СОО- + 2 Н+
Активированная карбоксильная группа переносится на пируват.
Е-биотин-СОО- + Пируват → Е-биотин + Оксалоацетат
Пируваткарбоксилаза – регуляторный фермент. Если концентрация ацетил-КоА
увеличивается, то он действует как аллостерический активатор пируваткарбоксилазы, ускоряя образование оксалоацетата. Т.о., избыток ацетил-КоА способствует активации цитратного цикла.
Метаболиты цитратного цикла используются как субстраты синтеза углеродного
скелета ряда соединений и явл. донорами Н+для образования восстановленных коферментов, участвующих в реакциях синтеза жирных кислот, стероидов и других веществ.
Два метаболита ЦТК могут дегидрироваться при участии NADP-зaвиcимыx
дегидрогеназ: малата и изоцитрата (обеспечивают обр около половины общего фонда NADPН, используемого в восстановительных синтезах)
Вопрос 61 Основные углеводы животных, биологическая роль. Углеводы пищи, переваривание углеводов. Всасывание продуктов переваривания.
Углеводы – основные поставщики энергии. На долю углеводов приходится
примерно 75% массы пищевого суточного рациона и более 50% от суточного количества необходимых калорий.
Основные углеводы животных:
В пище содержатся в основном в виде олигосахаридов и полисахаридов
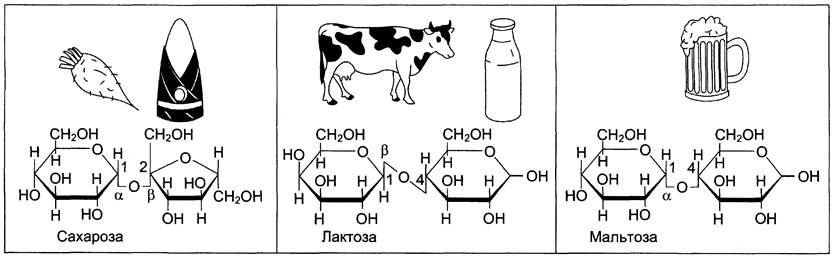
Сахароза – дисахарид, состоящий из α-D-глюкозы и β-D-фруктозы, соединённых
α, β-1,2-гликозидной связью. Растворимый дисахарид со сладким вкусом. Источником сахарозы служат растения, особенно сахарная свёкла, сахарный тростник.
Лактоза – молочный сахар; важнейший дисахарид молока млекопитающих.
В лактозе аномерная ОН-группа первого углеродного атома остатка D-галактозы связана β-гликозидной связью с четвёртым углеродным атомом D-глюкозы (β-1,4-связь).
Мальтоза поступает с продуктами, содержащими частично гидролизованный
крахмал, например, солод, пиво. Мальтоза также образуется при расщеплении крахмала в кишечнике. Она состоит из 2х остатков D-глюкозы, соединённых α-1,4-гликозидной св.
Гликоген – главный резервный полисахарид высших животных и человека,
построенный из остатков D-глюкозы. Гликоген содержится практически во всех органах и тканях животных и человека; наибольшее количество обнаружено в печени и мышцах.
При гидролизе: гликоген → декстрины →мальтоза → глюкоза
Крахмал – наиболее важный углеводный компонент пищевого рациона.
Резервный полисахарид растений (подобно гликогену у человека). Состоит из остатков глюкозы в двух формах: амилозы (неразветвленная молекула – только α-1,4-гликозидная связь) и амилопектина (разветвленная – α-1,4- и α-1,6-гликозидные связи)
Целлюлоза (клетчатка) – состоит из остатков глюкозы, соед. β-1,4-гликозид. св)
В организме человека нет ферментов, разрывающих β-связи в полисахаридах, но клетчатка все равно требуется для нормального пищеварения
Биологическая роль углеводов:
Основной источник энергии
Выполняют структурную роль – в виде гликозаминогликанов входят в состав межклеточного матрикса
Рецепторная функция – входят в состав рецепторов
Из углеводов в процессе метаболизма образуется большое число орг. соед, которые служат исходными субстратами для синтеза липидов, аминокислот, нуклеотидов.
Участвуют в детоксикации ксенобиотиков и инактивации веществ эндогенного происхождения (в составе глюкоуронидов)
Углеводы нельзя считать незаменимыми компонентами пищи, но если исключить
углеводы из рациона, то следствием м.б. гипогликемия, для компенсации которой будут расходоваться белки и липиды.
Эпителиальные клетки кишечника способны всасывать только моносахариды.
Поэтому процесс переваривания заключается в ферментативном гидролизе гликозидных связей в углеводах, имеющих олиго- или полисахаридное строение
А. Переваривание углеводов в ротовой полости
В ротовой полости пища измельчается при пережёвывании, смачиваясь при этом
слюной. В слюне присутствует α-амилаза, расщепляющая в крахмале α-1,4-гликозидные связи. В ротовой полости не может происходить полное расщепление крахмала, так как действие фермента на крахмал кратковременно и амилаза слюны не расщепляет α-1,6-гликозидные связи, поэтому крахмал переваривается частично с образованием крупных фрагментов – декстринов и небольшого количества мальтозы.
+ Амилаза слюны не гидролизует гликозидные связи в дисахаридах.
Действие амилазы прекращается в кислой среде желудка. Желудочный сок не содержит ферментов, расщепляющих углеводы.
Б. Переваривание углеводов в кишечнике: след. этапы переваривания крахмала и др. углеводов происходит в тонком кишечнике под действием – гликозидаз.
Панкреатическая α-амилаза
В двенадцатиперстной кишке рН среды желудочного содержимого нейтрализуется,
так как секрет поджелудочной железы имеет рН 7,5-8,0 и содержит бикарбонаты.
С секретом поджелуд. железы в кишечник поступает панкреатическая α-амилаза.
Продукты переваривания крахмала на этом этапе – дисахарид мальтоза, содержащая 2 остатка глюкозы, связанные α-1,4-связью.
Из тех остатков глюкозы, которые в молекуле крахмала находятся в местах
разветвления и соединены α-1,6-гликозидной связью, образуется дисахарид изомальтоза. Также образуются олигосахариды, содержащие 3-8 остатков глюкозы,
связанные α-1,4- и α-1,6-связями.
Целлюлоза проходит через кишечник неизменённой – выполняет важную
функцию балластного вещества, придавая пище дополнительный объём и положительно влияя на процесс переваривания. В толстом кишечнике целлюлоза может подвергаться действию бактериал. ферментов и частично расщепляться с образованием спиртов, органических кислот и СО2 = стимуляторы перистальтики кишечника.
Мальтоза, изомальтоза и триозосахариды, образующиеся из крахмала –
перевариваются под действием ферментов в тонком кишечнике. Дисахариды пищи сахароза и лактоза также гидролизуются специфическими дисахаридазами в тонком кишечнике.
Тонкий кишечник изнутри имеет ворсинки, благодаря чему увеличивается
поверхность контакта ферментов и субстратов в содержимом кишечника.
Ферменты, расщепляющие гликозидные связи в дисахаридах (дисахаридазы), образуют ферментативные комплексы, локализованные на наружной поверхности цитоплазматической мембраны энтероцитов.
Сахаразо-изомальтазный комплекс состоит из двух ППЦ и имеет доменное
строение. Связь фермента с мембраной способствует эффективному поглощению продуктов гидролиза клеткой. Этот комплекс гидролизует сахарозу и изомальтозу (имеея сахаразную и изомальтазную субъединицы), расщепляя α-1,2- и α-1,6- гликозидные связи.
Оба ферментных домена имеют мальтазную и мальтотриазную активности,
гидролизуя α-1,4-гликозидные связи в мальтозе и мальтотриозе, но сахаразная субъединица – единственный фермент в кишечнике, гидролизующий сахарозу.
Гликоамилазный комплекс – этот ферментативный комплекс катализирует
гидролиз α-1,4-связи между глюкозными остатками в олигосахаридах. Комплекс расщепляет связи в мальтозе, действуя как мальтаза. В гликоамилазный комплекс входят две разные каталитические субъединицы, имеющие небольшие различия в субстратной специфичности. Гликоамилазная активность комплекса наибольшая в нижних отделах тонкого кишечника.
β-Гликозидазный комплекс (лактаза) – ф. комплекс является гликопротеином.
Лактаза расщепляет β-1,4-гликозидные связи между галактозой и глюкозой в лактозе. Лактоза распределена неравномерно по всему тонкому кишечнику. Активность лактазы колеблется в зависимости от возраста. Так, активность лактазы сохраняется на высоком уровне до 5-7-летнего возраста.
Трегалаза – ф. комплекс, гидролизующий связи между мономерами в трегалозе
(дисахарид, содержащийся в грибах)
Совместное действие всех перечисленных ферментов завершает переваривание
пищевых олиго- и полисахаридов с обр. моносахаридов, основной из которых – глюкоза.
Моносахариды всасываются эпителиальными клетками тощей и подвздошной
кишок с помощью специальных механизмов транспорта через мембраны этих клеток.
В. Всасывание моносахаридов в кишечнике
Транспорт моносахаридов в клетки слизистой оболочки кишечника может
осуществляться 2 способами:
Путём облегчённой диффузии
Путем активного транспорта
При разной концентрации глюкозы в просвете кишечника "работают" различные механизмы транспорта. В случае
1. Активный транспорт – когда конц. глюкозы в просвете кишечника мала.
Глюкоза и Na+ проходят через мембраны с люминальной стороны, связываясь с разными участками белка-переносчика.
При этом Na+ поступает в клетку по градиенту концентрации, и одновременно
глюкоза транспортируется против градиента концентрации. Градиент концентрации Na+ создаётся работой Nа+,К+-АТФ-азы (такой же способ характерен также для галактозы)