Материал: 4140
16
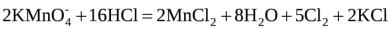 .
.
ПРИМЕР 8: Расставить коэффициенты методом полуреакций в уравнении реакции
Na2SO3 + H2O + Cl2 Na2SO4 + HCl.
1.Записываем схему реакции с указанием степеней окисления элементов
ивыделяем элементы, изменяющие свои степени окисления
Na+2S+4О-23 + H+2O-2 + Cl02 Na+2S+6O2–4 + H+Cl– .
2. Приводим эту схему в ионно-молекулярной форме, чтобы определить реальные частицы, существующие в растворе
2Na+ + SO3-2 + H2O + Cl2 2Na+ + SO42– + H+ + Cl– .
Участие в реакции ионов H+ говорит о том, что процесс протекает в кислой среде.
3. Полуреакции имеют вид
SO3-2 SO42–
Cl2 2Cl– .
Так как среда кислая, то ионно-молекулярное уравнение полуреакции имеет вид (см. табл. 3)
SO3-2 + H2O SO42– + 2H+ .
4. Составляем электронно-ионные уравнения полуреакций. Для этого в левую часть каждой полуреакции добавляем или вычитаем такое число электронов, чтобы суммарный заряд в обеих частях уравнений стал одинаковым. Получаем
SO32– + H2O – 2ē SO42– + 2H+ |
– процесс окисления |
Cl20 + 2ē 2Cl– |
– процесс восстановления |
5. В данном случае баланс по электронам есть. Поэтому суммируем элек- тронно-ионные уравнения
SO32– + H2O – 2ē + Cl20 + 2ē SO42– + 2H+ + 2Cl– .
17
6. Сокращаем подобные члены и получаем ионно-молекулярное уравнение окислительно-восстановительной реакции
SO32– + H2O + Cl20 SO42– + 2H+ + 2Cl– .
7. По полученному ионно-молекулярному уравнению окислительновосстановительной реакции составляем молекулярное уравнение.
Na2SO3 + H2O + Cl2 Na2SO4 + 2HCl.
Направление протекания ОВР в зависимости от различных факторов
Реакция между окислителем и восстановителем может протекать различно в зависимости от следующих факторов:
температуры;
реакции среды (рН);
природы реагирующих веществ;
концентрации реагентов.
ПРИМЕРЫ.
(В данных примерах приведены схемы реакций. Студенту предлагается самостоятельно уравнять реакции).
а) В зависимости от температуры термическое разложение хлората калия протекает различно
КClO3 |
КClО4 + КCl |
(4000 C) |
КClO3 |
КCl + O2 |
(2000 C) |
б) В кислой, нейтральной и щелочной среде перманганат калия и сульфит натрия реагируют различно
KMnO4 + Na2SO3 |
+ H2SO4 = MnSO4 |
+ Na2SO4 |
+ K2SO4 + H2O |
|
KMnO4 |
+ Na2SO3 |
+ H2O = MnO2 + Na2SO4 + KOH |
||
KMnO4 |
+ Na2SO3 |
+ KOH = K2MnO4 |
+ Na2SO4 |
+ H2O |
18
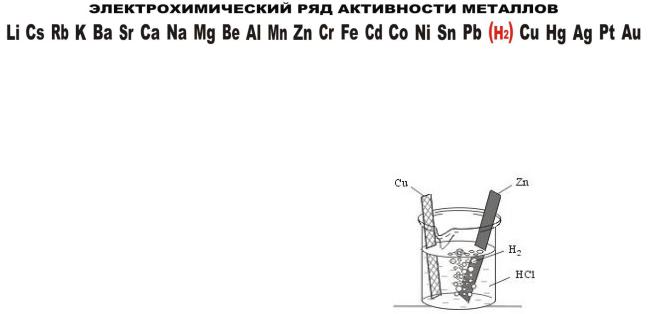
в) Взаимодействие металлов с кислотами протекает различно в зависимости от
природы кислоты
Zn + HCl ZnCl2 + H2
Zn + HNO3 Zn(NO3)2 + H2O + NO
г) Концентрация кислоты влияет на взаимодействие ее с металлами
H2SO4 (разб) + Zn ZnSO4 + H2
H2SO4 (конц) + Zn ZnSO4 + H2О + H2S
Взаимодействие металлов с кислотами
(Все приводимые ниже реакции даны в виде схем. Студентам следует их уравнять)
Продукты взаимодействия металлов с кислотами определяются несколькими факторами: природой и концентрацией кислоты, природой металла, температурой.
Все кислоты (кроме азотной и концентрированной серной!) реагируют с металлами, стоящими в ряду активности до водорода, при этом из растворов кислот вытесняется газообразный водород. Окислителем является катион Н+.
HCl + Zn ZnCl2 + H2
HCl + Cu (реакция не идет)
Серная кислота разбавленная подчиняется этому же правилу, то есть в реакциях с металлами окислителем также является катион Н+
H2SO4 (разб) + Ni NiSO4 + H2
H2SO4 (разб) + Cu (реакция не идет)
19
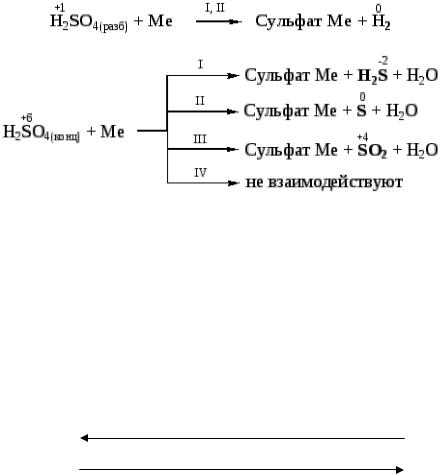
Серная кислота концентрированная с металлами реагирует по-
другому. Окислителем является ион SO42– (S+6). Продукты восстановления серной кислоты определяются активностью взаимодействующих с ней металлов (см. табл. 4). Ряд активности металлов условно разбит на четыре группы.
Таблица 4
I |
II |
|
III |
IV |
|
|
|
|
|
А к т и в н ы е |
Средней активности |
|
Н е а к т и в н ы е |
|
|
|
|
|
|
Li Cs Rb K Ba Sr Ca Na Mg Be Al Mn Zn |
Cr Fe Cd Co Ni Sn Pb |
Н |
Sb Bi Cu Ag Hg |
Pt Au |
|
|
|
|
|
Схемы процессов взаимодействия серной кислоты с металлами (Ме) можно представить следующим образом
Исключением из приведенной схемы являются Al, Cr, Fe, которые не реагируют без нагревания с H2SO4 (конц) ввиду пассивации.
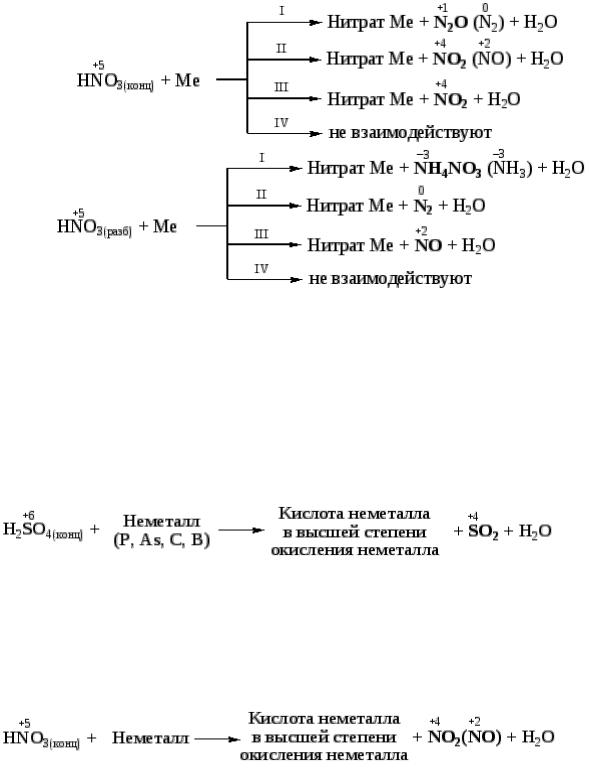
Азотная кислота. Окислителем в молекуле азотной кислоты является ион NO3– (N+5), который в зависимости от концентрации HNO3 и активности металла принимает от 1 до 8 электронов, образуя
NO2 ; NO ; N2O ; N2 ; NH3 (NH4NO3)
увеличение концентрации кислоты увеличение активности металла
Схемы процессов взаимодействия азотной кислоты с металлами (Ме) можно представить следующим образом
20
Так же, как и для концентрированной серной кислоты, Al, Cr, Fe не реагируют без нагревания с HNO3 (конц) ввиду пассивации.
Взаимодействие неметаллов с кислотами
Некоторые неметаллы взаимодействуют с концентрированной серной кислотой, при этом они восстанавливают ее до SO2
Так, P0 окисляется до H3PO4; As0 – до H3AsO4; C0 – до H2CO3 (H2O + CO2).
Неметаллы восстанавливают концентрированную азотную кислоту до NO2 или NO, при этом сами окисляются, как правило, до своей кислоты в высшей степени окисления
Например: HNO3 + S → H2SO4 + NO2 + H2O ; HNO3 + С → H2O + СО2 + NO2 .