Материал: 4140
6
Для того чтобы определить степень окисления элемента, выполняют следующую последовательность действий:
а) записывают значения известных степеней окисления; б) значение неизвестной степени окисления обозначают через х;
в) составляют уравнение равенства электрических зарядов, решая его, находят значение х.
ПРИМЕР 2:
Рассчитать степень окисления азота в веществах:
а) NH3 ; |
NxH3+1 |
: x + 3(+1) = 0; |
x = –3. |
Ответ: N–3. |
||
Б) NO2 ; |
NxO2-2 |
: x + 2(–2) = 0; |
x = +4. |
Ответ: N+4. |
||
В) N2O5 ; |
N2xO5-2 : 2x |
+ 5(–2) = 0; |
x = +5. Ответ: N+5. |
|||
Г) КNO2 ; |
К+1NxO2-2 : |
+1 + x + 2(–2) |
= 0; |
x = +3. Ответ: N+3. |
||
Д) N2O ; |
N2хO–2 : 2х + (–2) = 0; х = |
+1. |
Ответ: N+1. |
|||
Задания для самостоятельного решения Определите степени окисления всех элементов в следующих веществах:
1) |
H2SO4 |
; |
4) |
KmnO4 ; |
7) HclO3 ; |
2) |
H2SO3 |
; |
5) |
MnO2 ; |
8) Na3PO4 ; |
3) |
H2S ; |
|
6) K2Cr2O7 ; |
9) C2H6 . |
|
Окислители и восстановители
Чтобы произошла окислительно-восстановительная реакция, необходимо присутствие атомов, молекул или ионов, взаимно противоположных по своей способности отдавать или присоединять электроны.
В п е р и о д а х периодической системы элементов Д.И. Менделеева с повышением порядкового номера элемента восстановительные свойства простых веществ ослабевают, а окислительные усиливаются, и становятся максимальными у галогенов. Объясняется это строением атомов элементов.
Так, в III периоде натрий – самый активный восстановитель. На внешнем энергетическом уровне атома Na находится всего один электрон. Отдав его, атом натрия превращается в катион: Na0 – 1ē → Na+1.
Атом хлора содержит на внешнем уровне 7 ē. Принимая недостающий до завершения уровня 1 ē, атом хлора превращается в анион: Cl0 + 1ē → Cl–1.

7
Если рассматривать изменение окислительных и восстановительных свойств сверху вниз по г л а в н ы м п о д г р у п п а м периодической системы элементов Д.И. Менделеева, то наблюдается такая закономерность: с повышением порядкового номера элемента возрастают восстановительные свойства его атомов, а окислительные – убывают. Причина этого заключается в том, что сверху вниз возрастает число энергетических уровней, радиус атомов становится больше и, следовательно, слабее удерживаются внешние электроны.
Важнейшие окислители и восстановители приведены в табл. 2.
|
Таблица 2 |
|
|
Окислители |
Восстановители |
|
|
Простые вещества – неметаллы (кисло- |
Простые вещества – металлы, Н2, С. |
род, галогены и др.). |
|
|
|
Соединения, содержащие элемент в мак- |
Соединения, содержащие элемент в ми- |
симальной степени окисления (K2Cr2O7, |
нимальной степени окисления (K2S, H2S, |
K2CrO4, HNO3, KmnO4, H2SO4) |
CH4, HN3, HCl, KI) |
|
|
Соединения, содержащие элемент в про- |
Соединения, содержащие элемент в про- |
межуточной степени окисления (NaNO2, |
межуточной степени окисления (SO2, |
Ag2O, MnO2, H2O2 , «царская водка») |
СО, Na2SO3, HNO2, альдегиды, спирты) |
|
|
Электроток на аноде при электролизе |
Электроток на катоде при электролизе |
|
|
Многие элементы могут выполнять роль окислителей и восстановителей, в зависимости от того, в какой степени окисления они находятся.
ПРИМЕР 3:
S–2 |
S0 |
|
S+4 |
S+6 |
Н2S–2 |
S0 |
|
Н2S+4О3 |
Н2S+6О4 |
Минимальная |
Промежуточные |
Максимальная |
||
степень окисления |
степени окисления |
степень окисления |
||
Безусловный |
Могут выполнять роль |
Безусловный |
||
восстановитель |
как окислителя, так и восстановителя |
окислитель |
||
|
|
|
|
|
Только отдает |
S0 + О20 → S+4º2 |
(S0 – восстановитель) |
Только принимает |
|
электроны |
S0 + Fe0 → FeS–2 (S0 – окислитель) |
электроны |
||
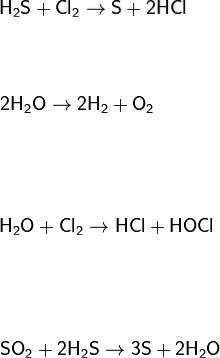
8
Задания для самостоятельного решения Определите, какую роль (окислителя или восстановителя) могут выпол-
нять следующие вещества в ОВР: |
|
||
1) |
HNO3 ; |
4) KmnO4 ; |
7) HclO4 ; |
2) |
Na2SO3 ; |
5) MnO2 ; |
8) Na3PO4 ; |
3) |
Cl2 ; |
6) K2Cr2O7 ; |
9) CH4 . |
Виды окислительно-восстановительных реакций
Межмолекулярные – реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Внутримолекулярные – реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например:
Диспропорционирование (самоокисление-самовосстановление) – реакции, в которых один и тот же элемент выступает и как окислитель, и как восстановитель, например:
Репропорционирование (конпропорционирование) – реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления:
Составление уравнений ОВР
Для нахождения пропорции веществ, вступающих в химическую реакцию, часто требуется уравнять ОВР. Уравнивание ОВР сводится к нахождению стехиометрических коэффициентов (то есть, количества молей каждого соединения). Стехиометрические коэффициенты могут принимать только значения целых величин от 1 и выше, дробные стехиометрические коэффициенты допускаются лишь в некоторых случаях записи термохимических уравнений.
Применяют два методы уравнивания ОВР: метод электронного баланса и метод полуреакций.
9
Метод электронного баланса
Этот метод более прост и используется в случае протекания реакции в газообразной среде (например, процессы горения или термического разложения соединений).
Число электронов, отдаваемых восстановителем, должно равняться числу электронов, присоединяемых окислителем.
Метод электронного баланса основан на сравнении степеней окисления атомов в исходных и конечных веществах.
Для правильного уравнивания следует придерживаться определенной последовательности действий:
1.Определить степени окисления всех элементов в исходных и конечных веществах.
2.Найти элементы, которые изменяют степень окисления (окислитель и восстановитель).
3.Составить для них схемы переходов электронов (электронные уравнения).
4.Уравнять число отданных и принятых электронов.
5.Расставить коэффициенты в уравнении ОВР перед формулами окислителя и восстановителя.
6.Расставить остальные коэффициенты, уравнивая вначале атомы металлов, затем неметаллов, последними уравнять атомы водорода и кислорода.
ПРИМЕР 4:
Уравнять окислительно-восстановительную реакцию:
Al + HCl → AlCl3 + H2.
Решение. Определяем степени окисления всех элементов в исходных и конечных веществах и находим элементы, которые изменяют степень окисления (эти элементы подчеркнуты)
Al0 + H+1Cl-1 → Al+3Cl-13 + H02
10
Записываем уравнения процессов окисления и восстановления. Обязательно учитываем количество атомов, участвующих в процессах:
Al0 3 ē → Al+3
2H+1 + 2 ē → H02
Уравниваем число отданных и принятых электронов (наименьшее общее кратное для трех отданных и двух принятых электронов равно 6).
Определяем коэффициенты при окислителе и восстановителе, то есть первую строку умножаем на 2, вторую на 3:
Al0 3 ē → Al+3 |
| |
| |
2 – процесс окисления, Al0 – восстановитель, |
|
| |
6 | |
|
2H+1 + 2 ē → H02 |
| |
| 3 – процесс восстановления, 2H+1 – окислитель. |
|
2 Al0 +6 H+1 → 2 Al+3 + 3 H02
Переносим полученные коэффициенты в молекулярное уравнение:
3 Al + 6 HCl → 2 AlCl3 + 3 H2
Подсчитываем число атомов каждого элемента в левой и правой частях уравнения (т.е. проверяем соблюдение закона сохранения массы):
В левой части |
|
В правой части |
||
2 |
атома Al |
= |
2 |
атома Al |
6 |
атомов Н |
= |
6 |
атомов Н |
6 |
атомов Сl |
= |
6 атомов Cl |
|
Вывод: реакция уравнена
. ПРИМЕР 5:
Уравнять окислительно-восстановительную реакцию:
H2S + KMnO4 + H2SO4 → S + MnSO4 + K2SO4 + H2 O.
Решение. Определяем степени окисления всех элементов в исходных и конечных веществах и находим элементы, которые изменяют степень окисления
H+12 S-2 + K+1Mn+7О-24 + H+12S+6О-24 → S0 + Mn+2S+6О-24 + K+12S+6 О-24 + H+12О-2