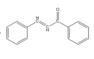
Материал: 3,5-дифенилпиразолин
3,5-дифенилпиразолин
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ НЕФТИ И ГАЗА им. И.М. ГУБКИНА
КАФЕДРА ОРГАНИЧЕСКОЙ ХИМИИ И ХИМИИ
НЕФТИ
КУРСОВАЯ РАБОТА
в практикуме по синтетическим методам органической химии
(Литературный синтез)
на тему: “3,5-дифенилпиразолин”
Студент: Пономаренко А.А.
Группа: ХТ-14-04
Преподаватель: Сокова Н.А.
МОСКВА
г.
Введение
Литературный синтез является заключительной стадией практикума органической химии. Значимость его выполнения состоит не только в получении вещества заданного состава и количества, но и в поиске информации об основных физических и химических свойствах соединения, способах получения, осуществляемых методиках синтеза, ее обработке и грамотном использовании на практике.
Поэтому целью нашей работы можно считать:
· поиск необходимых сведений по данному соединению, сбор информации;
· практическое применение теоретических знаний данного курса;
· получение и изучение свойств этого вещества и исходных соединение;
· умение работать с различными приборами и установками, используемыми в химических лабораториях.
При получении любого органического соединения возможны два случая: необходимый препарат уже известен, для него разработаны и описаны в литературе методы получения, либо необходимое вещество не описано. В нашем случае задача сводится к описанию всех известных методик синтеза и выбору оптимальной.
В ходе синтеза необходимо получить 6г 3,5-дифенилпиразолина.
2.
1. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
1.1 Формула соединения и его названия
Молекулярная формула: C15H14N2
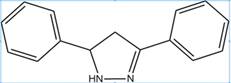
Таблица 1. Названия соединения
|
Систематическая номенклатура (номенклатура IUPAC) |
3,5-дифенилпиразолин |
|
Тривиальная номенклатура |
3,5-дифенилпирроазол |
1.2 Физические свойства соединения
Таблица 2. Физические свойства 3,5-дифенилпиразолина
|
Физические свойства |
|
|
Состояние |
Желтые кристаллы |
|
Молярная масса |
222,291 г/моль |
|
Термические свойства |
|
|
Т. плав. |
88 °C |
Растворитель: бензол, хлороформ.
2.2.
1.3 Химические свойства 3,5-дифенилпиразолина
Пиразолины являются продуктами неполного восстановления пиразола:
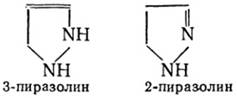
Для пиразолинов известен целый ряд таутомерных превращений, причем
большинство таутомеров можно выделить в чистом виде (в томчисле и незамещенные
по азоту):
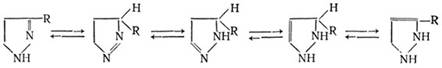
Пиразолины являются довольно реакционноспособными соединениями. Они легко
ацилируются по группе -NH, обычно без миграции двойной связи:
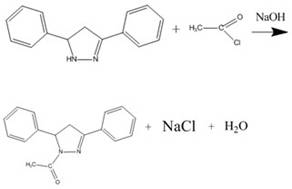
При действии азотистой кислоты на холоду образуют нитрозоамины, дают
комплексные соли с хлорной кислотой и хлорной ртутью, т. е. ведут себя как
алифатические вторичные амины:
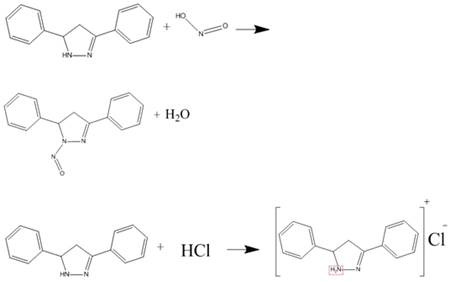
Для пиразолинов известен ряд перегруппировок в процессе некоторых
реакций. 5-Фенилпиразолин при очень жестких условиях (щелочь, 200°С) перегруппировывается
в 3-фенилпиразолин с последующим расщеплением кольца и выделением азота.
Открыта так называемая аминонитрильная перегруппировка, которая происходит при
щелочном расщеплении четвертичных пиразолиниевых солей, незамещенных в
положении 3:
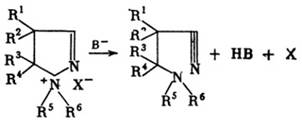
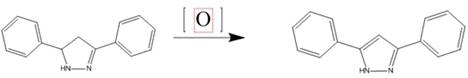
Окисление пиразолинов при помощи брома, перманганата калия, двуокиси
свинца приводит к образованию пиразолов. Селективное окисление в этих реакциях
успешно протекает при наличии электро-акцепторных групп в кольце или заместителей
у атома азота. Хорошие результаты получены при окислении бромом
3,4,5-трифенилпиразолина до соответствующего пиразола, при окислении двуокисью
свинца 1,3- и 1,5-диметилпиразолинов также до соответствующих диметилпиразолов.
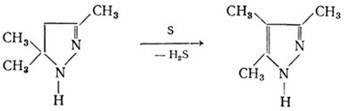
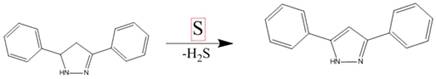
И.И. Грандберг и А.Н. Кост разработали метод дегидрирования разнообразных
пиразолинов при помощи серы или селена при 200-220°С. Производные пиразола при
этом получаются с хорошим выходом, но иногда реакция сопровождается
перегруппировкой, ведущей к образованию изомерных пиразолов:
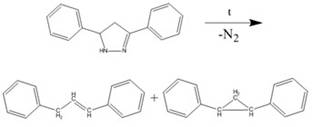
При нагревании пиразолинов выделяется азот и образуются циклопропан или
олефины:
Развитие химии пиразола за последние годы вызвано все большим применением его и производных в качестве лекарственных препаратов, красителей, люминесцентных и флюоресцентных веществ и т. д. К этому надо добавить, что производные пиразола оказались более доступными, чем многие другие гетероциклы. 3,5-дифенилпиразолин является сильным жаропонижающим средством, широко применяемый в фармацевтической промышленности. Другая широкая область применения пиразолиновых производных - химия пиразолиновых красителей. Краситель пиразолинового ряда - тартразин желтый - используется в пищевой промышленности США.
Примерами разнообразного практического применения других производных
пиразола является использование 1-фенил-З-амино-пиразолина для проявления
кинопленки; употребление в аналитической химии пиразолин-1-дитиокарбаматов для
разделения катионов; применение изолана, пиролана, пиразоксона в качестве
инсектицидов.
1.4 Методы получения 3,5-дифенилпиразолина
Мною найдено две методики получения 3,5-дифенилпиразолина.
Синтез пиразольных соединений из гидразина или его
производных
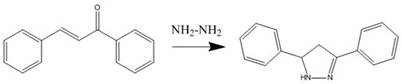
Ход работы: В трехгорлую колбу емкостью 250 мл, снабженную мешалкой, капельной воронкой и обратным холодильником, помещают 16 г бензилиденацетофенона и 36 мл спирта. Смесь перемешивают до получения однородного раствора и постепенно при энергично работающей мешалке добавляют из капельной воронки смесь 8 мл 85%-ного водного раствора гидразингидрата и 8 мл спирта. По окончании реакции перемешивание про- продолжают до тех пор, пока не закончится образование кристаллов 3,5-дифенилпиразолина (около 4 ч). На следующий день отфильтровывают осадок и высушивают его между листами фильтровальной бумаги. Полученный пиразолин очень легко окисляется на воздухе, поэтому фильтрование и высушивание проводят как можно быстрее. Выход около 14г (80% от теоретического); т. пл. 88"С.
Синтез пиразолов и пиразолинов из алифатических
диазосоединений- диазометана или диазоуксусного эфира и ацетиленов или
олефинов.
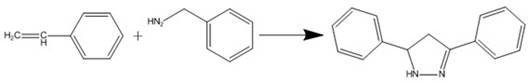
Фенилацетилен с диазометаном образует 3(5)-фенилпиразол с небольшой примесью 4-фенилпиразола: Сам ацетилен реагирует с диазометаном в более жестких условиях P-5 атм, 30-40°С). При взаимодействии эфиров, ненасыщенных кислот, ненасыщенных нитрилов, ненасыщенных кетонов и других олефиновых соединений с алифатическими диазосоединениями в присутствии катализаторов (медный порошок и соли меди) и без катализатора при нагревании или без нагревания можно получить различные пиразолины с удовлетворительным выходом.
Из рассмотренных выше способов синтеза 3,5-дифенилпиразолина наиболее рационально использовать синтез, описанный в п.2.4.1. так как этот способ наиболее удобен для осуществления в лабораторных условиях, вследствие наличия необходимых реактивов для синтеза и времени исполнения. Также этот способ состоит из двух стадий, что является необходимым условием литературного синтеза.
Из найденных мною методик наиболее оптимальна методика [1]
А.Е. Агрономов, Ю.С. Шабаров Лабораторные работы в органическом практикуме, изд.2, Mосква: Издательство «Химия», 1974, с. 214.
пиразолин молекулярный синтез
2. Экспериментальная часть
.1 I стадия. Получение бензальацетофенона
(халкона)
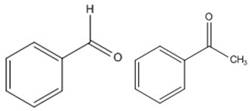
.1.1 Уравнение основной реакции
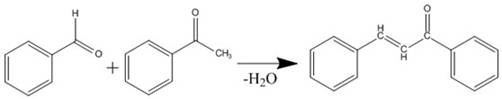
2.1.2 Расчет и таблица характеристик и количеств исходных реагентов
Расчет теоретических количеств реагентов, необходимых для получения 6 г халкона по уравнению реакции:
Молекулярная масса бензальдегида М=106 г/моль;
Молекулярная масса ацетофенона М=120 г/моль;
Молекулярная масса бензальацетофенона М=208 г/моль;
Необходимо получить 6 г бензальацетофенона, т.е. 0,0288 молей.
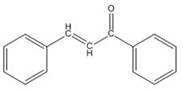
По уравнению реакции для получения 1 моля бензальацетофенона необходимо
взять 1 моль ацетофенона и 1 моль бензальдегида:
Масса необходимого количества ацетофенона равна: m=n*Mr=0,0288*106=3,053г
Масса необходимого количества бензальдегида равна: m=n*Mr=0,0288*120=3,456 г
Перерасчет количества вещества по практикуму
В практикуме О.А. Птицыной для получения 8,6г халкона необходимо 2,2 г гидроксида натрия, 19,6 мл воды, 12,2 мл 95%-ного этилового спирта, 4,8 мл ацетофенона, 5 мл бензальдегида.) По ацетофенону
Для синтеза 8,6 г халкона - 4,8*1,0281 г ацетофенона
г халкона - Х г ацетофенона
Х=3,45г или n=0,0287 моль или 3,36 мл.) По бензальдегиду
Для синтеза 8,6г халкона - 5*1,0415 г бензальдегида
г халкона - Х г бензальдегида
Х=3,63 г или n=0,0343 моль или 3,49 мл.) По этиловому спирту
Для синтеза 8,6г халкона - 12,2*0,79 г этанола
г халкона - Х г этанола
Х=6,72 г или n=0,146 моль или 8,5 мл.) По гидроксиду натрия
Для синтеза 8,6г халкона - 2,2 г гидроксида натрия
г халкона - Х г гидроксида натрия
Х=1,54 г или n=0,0385 моль.) По воде
Для синтеза 8,6г халкона - 19,6 мл воды
г халкона - Х мл воды
Х=13,67 г или n=0,759 моль или 13,67 мл.
Таблица 3. Характеристики и количества исходных веществ
|
Название реактивов |
Брутто-формула |
Молек. масса, г/моль |
Основные константы |
Количества исходных реагентов |
|||||||
|
|
|
|
Ткип, С |
Тпл, С |
d420, г/см3 |
По ур-ию реакции |
По методике |
Избыток |
|||
|
|
|
|
|
|
|
г |
моль |
г |
моль |
мл |
г/моль |
|
Ацетофенон |
С6Н5СОCH3 |
120 |
202 |
19,7 |
1,5342 |
3,053 |
0,0288 |
3,45 |
0,0287 |
3,36 |
0,0001 |
|
Бензальдегид |
С6Н5COH |
106 |
178 |
1,5455 |
3,456 |
0,0288 |
3,63 |
0,0343 |
3,49 |
0,0055 |
|
|
Этанол |
C2H5OH |
46 |
78,4 |
-114 |
1,3611 |
- |
- |
6,72 |
0,146 |
8,5 |
- |
|
Гидроксид натрия |
NaOH |
40 |
1403 |
323 |
- |
- |
- |
1,54 |
0,0385 |
- |
- |
|
Вода |
H2O |
18 |
100 |
0 |
- |
- |
- |
13,67 |
0,759 |
13,67 |
- |
Описание синтеза
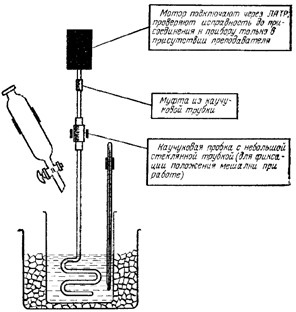
Рисунок 1. Установка для синтеза халкона
Собирают установку как показано на рисунке 1.
В стакан емкостью 200 мл, снабженным мешалкой и термометром, наливают раствор, приготовленный из 1,54 г гидроксида натрия, 13,67 мл воды и 6,72 мл этилового спирта (95%). Стакан помещают в баню со льдом и при перемешивании и температуре раствора 5˚С приливают 3,36 мл ацетофенона и 3,49 мл свежеприготовленного бензальдегида. Реакция конденсации экзотермична, и ее проводят при температуре 24-26˚С (предварительно убрав баню со льдом) и энергичном перемешивании в течении 2-3 часов, пока смесь не превратится в густую эмульсию. В течении всего перемешивания следует поддерживать температурный режим, т.к. при более низкой температуре и слабом перемешивании халкон выделяется в виде масла, при затвердевании которого образуются крупные комки. При повышении температуры уменьшается выход халкона за счет протекания побочных реакций. После окончания реакции смесь оставляют на ночь в холодном месте. Кристаллы халкона выпадают при длительном стоянии смеси на холоде. Перед отсасыванием кристаллов халкона на воронке Бюхнера смесь охлаждают в бане со льдом и солью. Затем промывают на фильтре охлажденным до 0˚С этиловым спиртом и сушат на воздухе.
Для получения чистого халкона его перекристаллизовывают из 95%-ного
этилового спирта в расчете 4 г на 1 г халкона (т.е. спирта д.б. 24г). [2]
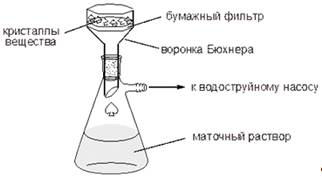
Рисунок 2. Установка для фильтрования на воронке Бюхнера
Таблица 4. Константы полученного соединения, выход продукта реакции
|
Название вещества |
Константы вещества |
Выход вещества |
|||||
|
|
полученного при синтезе |
по литературным данным |
г |
% мас. |
|||
|
|
Тпл, °С |
n20d |
Тпл, °С |
n20d |
|
от указанного в методике |
от теоретического |
|
Бензальаце-тофенон |
60-63 |
- |
62 |
- |
85 |
87 |
|
.2 II стадия. Получение 3,5-дифенилпиразолина
.2.1 Уравнение основной реакции
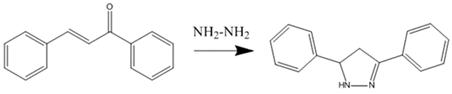
2.2.2 Расчет и таблица характеристик и количеств исходных реагентов
Расчет теоретических количеств реагентов, необходимых для получения 6 г халкона по уравнению реакции:
Молекулярная масса бензальацетофенона М=208 г/моль;
Молекулярная масса гидразина М=32 г/моль;