Материал: 3375
16
обычных условиях вода замерзает при 0 0С и закипает при 100 0С. Такое резкое отклонение от установленной закономерности как раз и объясняется тем, что вода является ассоциированной жидкостью. Таким образом, аномальность температур замерзания и кипения воды связана с тем, что существование ее в условиях Земли в твердом и жидком состояниях само по себе аномально. Нормальным было бы пребывание ее только в парообразном состоянии.
|
20 |
|
|
|
|
0 |
|
|
H2Te |
|
|
|
|
|
C |
|
|
Точки кипения |
-4 |
|
|
|
||
o |
-20 |
|
|
|
Температура, |
|
H2Se |
|
|
|
|
|
||
-40 |
|
|
|
|
|
H2 |
-42 |
|
|
-60 |
H2O |
|
-51 |
|
|
|
|||
|
-61 |
|
|
|
|
|
-64 |
|
|
|
|
|
|
|
|
-80 |
-70 |
Точки замерзания |
|
|
|
-82 |
|
|
|
-100 |
-90 |
|
|
|
0 |
40 |
80 |
120 |
|
|
Молекулярная масса, г/моль |
||
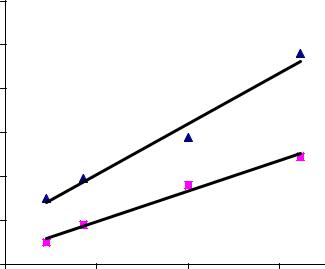
Рис. 4 Зависимость температуры кипения и замерзания гидридов от их молекулярной массы
Температура ассоциации молекул воды позволяет объяснить причину одного из важнейших свойств воды - ее плотностную аномалию. Как известно, максимальная плотность воды (1,0 г/см3) соответствует температуре +4 0С, а лед имеет значительно меньшую плотность - 0,94 г/см3. Предполагается, что в воде при +4 0С присутствует максимальное число удвоенных молекул воды.
Ассоциативность воды сказывается и на очень высокой теплоте ее парообразования. Например, чтобы испарить 1 г воды, уже нагретой до 100 0С, требуется в 6 раз больше тепла, чем для нагревания 1 г воды от 0 до 80 0С. Благодаря этому вода является мощнейшим энергоносителем на нашей планете. Под действием солнца 1 млн т воды за минуту превращается в пар, каждый грамм которого несет в верхние слои атмосферы по 2,26 тыс. Дж солнечной энергии. В результате атмосфера Земли получает количество тепла, эквивалентное тому, которое вырабатывали бы 40 тысяч электростанций, каждая мощностью по 1 млрд кВт.
Способность воды накапливать большие запасы тепловой энергии позволяет сглаживать резкие температурные колебания на земной поверхно-
17
сти в различные времена года и в разное время суток. Вода выступает регулятором температуры на нашей планете.
Среди необычных свойств воды следует отметить ее исключительно высокое поверхностное натяжение (72,7 10-3 Н/м при 20 0С), которое относительно велико по сравнению с большинством других жидкостей и уступает только ртути.
Поверхностное натяжение воды очень чувствительно даже к следам примесей. Величина поверхностного натяжения существенно снижается при наличии примесей поверхностно-активных веществ.
Поверхностное натяжение проявляется в смачивании поверхностей многих тел. Смачивание и поверхностное натяжение лежат в основе явления, называемого капиллярностью. Состоит оно в том, что в узких каналах вода способна подниматься на высоту, гораздо большую, чем та, которая допускается силой тяжести для столбика данного сечения. Капиллярность имеет огромное значение для эволюции жизни на нашей планете. Благодаря этому явлению вода смачивает толщу Земли, лежащую значительно выше грунтовых вод, и доставляет корням растений растворы питательных солей с глубины десятков метров. Капиллярностью во многом обусловлено движение крови и тканевых жидкостей. С величиной поверхностного натяжения связаны такие практически важные вопросы, как расход энергии на распыление воды, степени смачиваемости водой твердых тел в процессе флотации, способность воды подниматься по капиллярам.
В обычных условиях чистая вода практически не диссоциирована, это делает ее плохим проводником электрического тока: электропроводность химически чистой воды при 18 0С составляет 3,8 10-8 Ом-1 см-1, тогда как электропроводность морской воды в миллионы раз больше благодаря ее высокому солесодержанию. Измерение электропроводности является одним из наиболее чувствительных методов анализа воды.
Вязкость воды быстро уменьшается с повышением температуры. Это свойство воды следует учитывать и по возможности использовать в процессах, связанных с фильтрацией водных растворов.
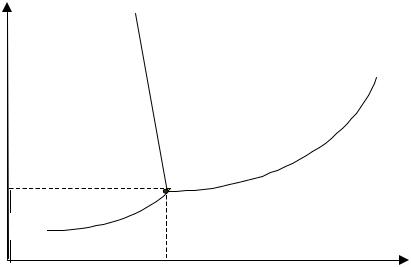
В природе в зависимости от температуры и давления вода может находиться в трех агрегатных состояниях: лед, вода, пар. Это состояние воды можно проследить, если построить диаграмму состояния воды (рис. 5). По оси абсцисс при этом обычно откладывается температура, по оси ординат - давление. Кривая АВ соответствует давлению пара жидкой воды, АБ - давлению пара льда, АГ - зависимости температуры плавления льда.
Напомним, что химической с и с т е м о й называется вещество или смесь веществ в определенном ограниченном объеме. Система может быть г о м о г е н н о й и г е т е р о г е н н о й. Гомогенная система представляет собой единое по составу и внутренней структуре скопление частиц, либо одинаковых, либо разных, но полностью перемешанных друг с другом. Такой системой будет, например, вода, раствор сахара или соли, смесь газов,
18
однородное твердое вещество и т.п. Наоборот, система является гетерогенной, если в ней одновременно содержатся различные по составу или внутренней структуре скопления частиц, ограниченные друг от друга поверхностями раздела.
Г
Давление,
мм рт. ст.
ВВ
|
|
|
ВОДА |
|
ЛЕД |
А |
|
|
|
|
|
4,6 |
|
|
|
Б |
|
|
ПАР |
|
|
+0,01 |
Температура, оС |
|
|
|
Рис. 5 Диаграмма состояния воды
К гетерогенным относятся, например, системы, состоящие из двух несмешивающихся жидкостей, льда и воды, смеси твердых веществ и др.
Разделенные составные части гетерогенной системы носят название ее фаз. Ф а з о й, таким образом, называется гомогенная часть гетерогенной системы.
Если мы обратимся теперь к рис. 5, то увидим, что вся площадь диаграммы разбита на три части, каждая из которых соответствует области устойчивости одного из агрегатных состояний воды, т.е. одной из фаз трехфазной системы: лед - вода - водяной пар. Разделяющие эти области линии отвечают тем условиям температуры и давления, при которых в устойчивом состоянии находятся две фазы:
Линия АВ … равновесие вода |
пар |
Линия АГ … равновесие лед |
вода |
Линия АБ … равновесие лед |
пар |
Все три линии сходятся в точке А. При отвечающей ей температуре (+0,01 0С) и давлении (4,6 мм рт. ст.) в устойчивом равновесии могут, следовательно, сколько угодно долго находиться все три ее фазы. Поэтому эта точка называется тройной. При давлениях и температурах, соответствующих точкам выше кривой АВ, вода находится в конденсированном состоя-
19
нии в виде жидкости. При давлении и температурах, представленных точками ниже этой кривой, вода полностью испаряется. Линия АБ является кривой возгонки льда, выше нее находится область льда, ниже расположена область пара.
Вода является очень слабым электролитом. Из 555 млн. молекул воды диссоциирует на ионы только одна
Н2О Н+ + ОН- Константа диссоциации воды КН2О = 1,810−16 , а ионное произведение
воды Кw = 1 10-14. Ионное произведение воды сильно возрастает при повышении температуры водных растворов. Изменение величины ионного произведения воды в зависимости от температуры очень важно в процессах гидролитического расщепления солей.
В реакциях окисления - восстановления вода обычно играет роль среды. Под действием сильных восстановителей при обыкновенной температуре и особенно при повышенной вода проявляет окислительные свойства, например, окисляет щелочные и щелочноземельные металлы, железо, углерод и др. При действии сильных окислителей (фтор, хлор и т.п.) вода склонна проявлять восстановительные свойства.
Вода способна к комплексообразованию. Существуют три типа присоединения воды к молекулам других веществ, а именно: присоединение по
электролитическому или ионному типу, по координационному типу и по
адсорбционному типу.
По ионному типу соединяются с водой оксиды щелочных, щелочноземельных и редкоземельных металлов и кислотные оксиды. Вода, присоединенная по ионному типу, называется конституционной. Так как все реакции соединения оксидов с водой являются экзотермическими, то полученные соединения устойчивы, и конституционная вода при нагревании удаляется с большим трудом.
Молекулы воды, будучи диполями, способны притягиваться преимущественно к положительным ионам металлов, образуя комплексы. Комплексы, в состав которых входит вода, называются аквакомплексами или кристаллогидратами, а вода, вошедшая в их состав - кристаллизационной. Связь между положительными ионами металлов и кислородом воды является координационной связью. При нагревании, а также при выветривании кристаллогидратов кристаллизационная вода выделяется значительно легче, чем конституционная.
Каждое вещество на своей поверхности адсорбирует некоторое количество воды за счет межмолекулярных сил притяжения. Наличие последних обусловливается, по-видимому, дипольностью молекул воды. Вода, присоединенная к веществу по адсорбционному типу, называется гигроскопической. Гигроскопическая вода удаляется еще легче кристаллизационной.
20
Вода является универсальным растворителем, способным растворять очень многие твердые вещества, жидкости и газы. Способность многих веществ растворяться в воде и диссоциировать на ионы определяется ее высокой диэлектрической проницаемостью. У большинства растворителей диэлектрическая проницаемость находится в пределах от 10 до 50. У воды величина диэлектрической проницаемости максимальна и равна 81. Эта особенность воды определяет самую большую растворяющую способность в отношении веществ с полярной и ионной структурой. Высокая растворяющая способность воды сыграла важную роль в формировании состава природных вод, которые в зависимости от условий образования значительно отличаются друг от друга по своим качественным показателям.
По своим химическим свойствам вода является весьма реакционным веществом. Реакционную способность воды необходимо учитывать при использовании химических методов очистки сточных вод.
В то же время вода является химически устойчивым соединением. То, что вода химически не изменяется под действием тех соединений, которые она растворяет, и не изменяет их, характеризует ее как инертный растворитель. Это свойство воды очень важно для живых организмов нашей планеты, поскольку необходимые их тканям питательные вещества поступают в водных растворах в сравнительно мало измененном виде. Как растворитель вода может использоваться многократно.
Благодаря своей ассоциативности вода обладает удивительными, можно сказать, загадочными свойствами. К примеру, вода, прошедшая сквозь магнитное поле (омагниченная вода), находит применение в промышленности, сельском хозяйстве, строительстве и даже медицине. Омагниченная вода растворяет не только накипь в паровых котлах, но и почечные камни. Лекарства, приготовленные на омагниченной воде, действуют более эффективно.
Аталая вода? Ученые в Томске обнаружили, что замачивание семян в талой снеговой воде повышает урожайность ячменя на четверть. Цыплят поили талой речной водой – через два месяца их вес был на 40 % больше, чем у тех, которые пили обычную воду из той же реки.
Есть и озвученная вода. Был проведен такой опыт: семена сосны одновременно замачивали в ведре обычной воды и в ведре той же воды, над которой час гудел автомобильный клаксон. Вторые саженцы были значительно выше и мощней своих собратьев.
Ав серьезной научной литературе ежегодно печатаются сведения о чудесах воды освещенной, перемешанной, ионизированной, пропущенной через капилляры, обработанной электрическим током.
И вот что интересно, разные воздействия на воду приводят чаще всего
кодинаковым результатам: повышается растворимость веществ в воде, биологическая и химическая активность воды резко снижается. С чем это связано? Почему?