Материал: 3375
11
2 СТРУКТУРА ВОДЫ И ЕЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Каждая жидкость, в том числе и вода, характеризуется определенной структурой. Если у газов структура отсутствует, то жидкостям, в отличие от кристаллов, свойственен так называемый ближний порядок. Современные методы исследования, такие как рассеяние рентгеновских лучей, нейтронов или электронов, позволяют сделать вывод о том, что жидкости в какой-то степени можно сравнить с кристаллами, приписывая им квазикристаллическую структуру.
Причина появления структуры в жидкости связана с возникновением взаимного влияния атомов и молекул, приводящего к уменьшению среднего расстояния между ними и уменьшению их подвижности в сравнении с газом. Силы, которые обеспечивают возможность существования жидкой фазы, имеют различный характер. В основном, это межмолекулярные ван-дер- ваальсовые силы взаимодействия типа диполь - диполь или диполь - индуцированный диполь, либо дисперсионные, описанные Лондоном, и называемые силами взаимодействия Ван-дер-Ваальса – Лондона. Энергия последних зависит от расстояния между центрами взаимодействующих частиц (пропорциональна 1/r6). Поэтому такие взаимодействия могут возникать только на очень близких расстояниях. Энергия межмолекулярных взаимодействий примерно на 2-3 порядка меньше энергии обычных химических связей.
Природные, сточные и другие виды вод представляют собой сложные системы, основу которых составляет химическое соединение, имеющее формулу Н2О. Кажется, что за такой простой формулой стоит ничем не примечательное соединение. Однако при более глубоком ознакомлении со строением молекулы и свойствами воды выясняется, что она обладает рядом удивительных свойств.
2.1 Внутреннее строение молекулы воды
В античную эпоху воду считали элементом. И только в 1781 г. Генри Кавендиш показал, что вода образуется от сгорания водорода и воздуха, а Лавуазье первый пришел к выводу, что вода состоит из двух элементов - водорода и кислорода. В 1805 г. Гей-Люссак и Гумбольдт установили, что молекула воды построена из двух атомов водорода и одного атома кислорода. Относительные весовые количества водорода и кислорода в молекуле воды были установлены в 1842 г. Дюма и оказались равными 2,016 : 16,000.
Весовой состав чистой воды следующий: 11,9 % водорода и 88,81 % кислорода. При определении молекулярной массы пара установлено, что в этом состоянии молекуле воды соответствует простейшая формула Н2О. В
12
жидком состоянии вода ассоциирована, т.е. наряду с простыми молекулами она содержит и надмолекулярные образования, соответствующие общей формуле (Н2О)n, где n = 2,3,4 и т.д.
Способность воды образовывать ассоциаты объясняется особенностями строения молекул. С современных позиций строения атома электронные облака молекул воды расположены в форме неправильного тетраэдра. В молекуле воды имеется 10 электронов, восемь из которых принадлежат атому кислорода 1S2 2S2 2Pz2 2Py1 2Px1 и два - двум атомам водорода 1S1.
|
|
2P |
↓↑ |
↓ |
↓ |
|
|
|
|
|
О8 |
1S22S22p4 |
H1 |
1S1 |
1S |
↑ |
|||||
|
|
|
|
|||||||
|
|
|
px py |
pz |
|
|
|
|||
|
|
2S |
↓↑ |
|
|
H1 |
1S1 |
1S |
↑ |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
1S |
↓↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1S+3p=4Sp - Sp3- гибридизация
При образовании молекулы воды 2S и 2P-орбитали атома кислорода вступают в Sp3-гибридизацию, в результате которой образуется четыре Sp-гибридных облака, расположенных по вершинам тетраэдра (рис. 1). Угол между Sp-орбиталями в тетраэдре молекулы воды составляет 104о5'. Это значение отличается от чисто тетраэдрического (109о), так как две Sp-орбитали атома кислорода заняты неподеленными электронными парами, а две другие
– неспаренными p-электронами. Обобществление р-электронов кислорода с 1S-электронами атомов водорода приводит к образованию молекул воды.
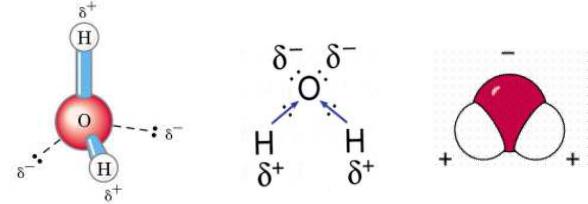
Рис. 1 Электронные орбитали молекулы воды
Таким образом, в молекуле воды существуют четыре полюса зарядов: два отрицательных, обусловленных избытком электронной плотности в местах расположения неподеленных пар электронов, и два положительных вследствие недостатка ее в местах нахождения протонов. В такой структуре
13
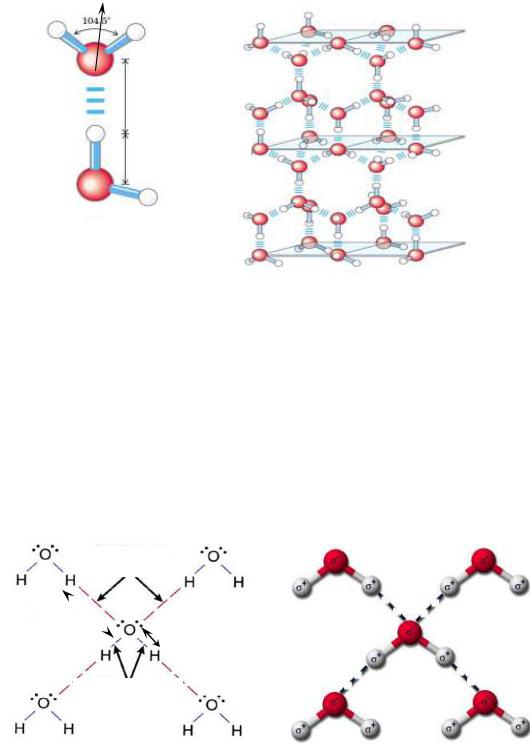
протоны оказываются почти полностью погружены в электронное облако кислорода. Несимметричное распределение электрических зарядов в почти шарообразной молекуле воды обусловливает образование большого дипольного момента молекулы, равного 1,84 Дебая. Этот важный параметр, а также валентный угол и длина связи показаны на рис. 2.
µ=1.8 D
Водородная связь
0,17 нм
Ковалентная связь
0,099 нм
Рис. 2 Схематическое изображение структурных особенностей молекулы воды и водородной связи
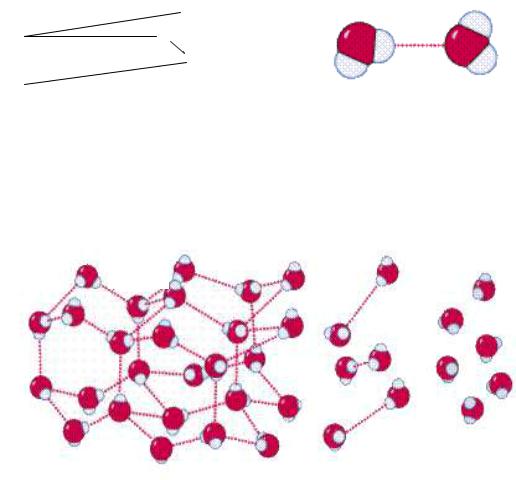
Благодаря большому значению дипольного момента между молекулами воды проявляется сильное взаимодействие за счет образования межмолекулярных водородных связей, которые возникают между ядрами водорода и неподеленными электронами кислорода, насыщая электронную недостаточность водорода одной молекулы воды и фиксируя его по отношению к кислороду другой молекулы. Взаимодействие молекул воды с образованием водородных связей показано на рис. 3.
Н-связи
0,17 нм
0,099 нм
Ковалентные
связи
Рис. 3 Взаимное расположение молекул воды с участием водородных связей
14
Тетраэдрическая направленность электронного облака позволяет образовать четыре водородные связи для каждой водной молекулы, которая благодаря этому может ассоциировать с четырьмя соседними. За счет водородных связей происходит образование надмолекулярных ассоциатов воды. Водородные связи не настолько сильны, чтобы разорвать и перестроить поновому молекулы воды; они в несколько раз слабее ковалентных связей, объединяющих атомы водорода и кислорода в молекуле воды. Достаточно обычных тепловых движений молекул воды, чтобы разрушить водородные связи. Макромолекулярная структура позволяет ей, разорвав водородные связи, присоединять молекулы или части молекул других веществ, тем самым способствуя их растворению.
У воды в жидком состоянии наиболее устойчивые ассоциаты можно представить в виде сдвоенных молекул:
Н
О Н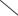 Н
Н О
О
Н
В этом случае образуется более плотная упаковка, и вода будет иметь максимальную плотность. Другие сочетания молекул воды приводят к образованию более рыхлых структур. Так, обычная структура льда может быть схематично представлена следующим образом:
Водородные связи
Лед |
Тающий |
Вода |
лед |
|
|
|
|
В ней каждый атом кислорода связан с двумя "своими" атомами водорода и двумя "чужими", что приводит к образованию кристаллической структуры, характеризующейся наличием пустот.
15
Эти особенности структуры молекул и их ассоциатов на основе водородных связей являются причинами того, что вода не подчиняется многим физико-химическим закономерностям,справедливым для других соединений.
Для объяснения аномальных свойств воды в жидком состоянии созданы различные модели ее структуры. В основе многочисленных моделей жидкая вода рассматривается как кристаллическое вещество (жидкие кристаллы). Упорядоченное (кристаллическое) расположение частиц воды в жидком состоянии доказано экспериментально. Полагают, что при плавлении льда его решетка частично разрушается, и эти пустоты и ажурная структура льда заполняются освободившимися молекулами воды.
Представляет особый интерес модель структуры жидкой воды в виде мерцающих кластеров, состоящих из соединенных водородными связями молекул, плавающих в более или менее "свободной" воде. Кластеры постоянно существуют в текучей жидкости, непрерывно образуясь и разрушаясь в соответствии со случайными тепловыми изменениями в микроучастках жидкости. Френк и Вин определили время полужизни кластера как 10-10-10-11 с, что соответствует времени релаксации процессов в воде.
В классической теории структуры воды, созданной Берналом и Фаулером, существование максимума плотности при температуре + 4 0С объясняется тем, что при этой температуре преобладающая часть молекул воды связана в кварцеподобную структуру, а при других температурах они имеют тридимитоподное кристаллическое строение, соответствующее меньшей плотности.
2.2 Физические и химические свойства воды
Чистая вода представляет собой бесцветную или голубовато-зеленую прозрачную жидкость, не имеющую ни запаха, ни вкуса.
Масса 1 мл очищенной речной воды принята за единицу массы и называется граммом.
Такие фундаментальные физические характеристики воды, как температура кипения и замерзания известны каждому из нас. При давлении 760 мм рт. ст. температура замерзания воды составляет 0,00 оС, а температура кипения - 100,00 оС. Вода по своему молекулярному строению, как гидрид кислорода, подобна гидридам серы, селена и теллура, т.е. гидридам элементов, входящих в одну с кислородом подгруппу периодической системы химических элементов, и для нее должны бы наблюдаться закономерности изменения физических свойств, свойственные гидридам других элементов данной подгруппы. Начиная с более тяжелого из них, проследим, как изменяются температуры кипения и замерзания по мере уменьшения молекулярной массы гидридов (рис. 4).
В соответствии с этими зависимостями следовало бы ожидать, что вода должна кипеть при –70 0С и замерзать при –90 0С. На самом же деле в