Материал: 2465
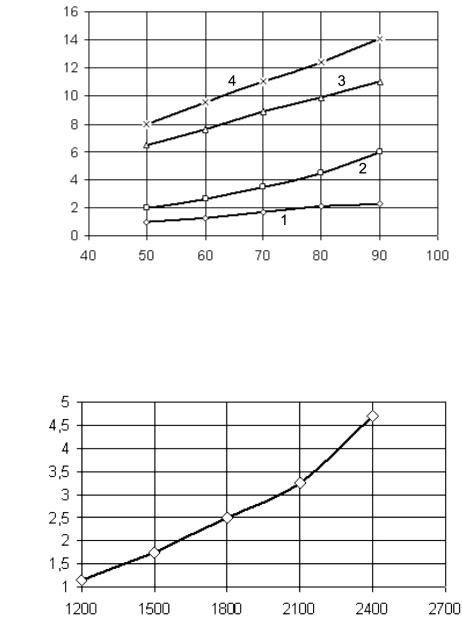
Содержание свободного кислорода, % об.
Температура размягчения, С
Рис. 2.2. Содержание свободного кислорода в газах окисления, отходящих из аппарата: 1 – окисление в трубчатом реакторе при 270 С; 2 – окисление в колонне при 270 С; 3 – окисление в кубе
|
|
при 270 С; 4 – окисление в кубе при 250 С |
|||||
|
|
|
|
|
|
И |
|
|
, % |
|
|
|
|
||
|
|
|
|
Д |
|||
|
|
|
|
|
|||
Содержаниесвободного |
кислорода в газеокисления |
|
|
А |
|
||
|
б |
|
|
||||
и |
|
|
|
||||
Расход воздуха в колонне, м3/ч |
|||||||
|
|
||||||
|
|
||||||
|
|
С |
|
|
|
|
|
Рис. 2.3. Зависимость содержания свободного кислорода в газах окисления от расхода воздуха в окислительной колонне
при получении дорожных битумов
Количество израсходованного кислорода, кг/ч,
G// |
= G |
G/ |
. |
(2.7) |
O2 |
O2 |
O2 |
|
|
Количество образующегося СО2
|
|
0,3 G// |
M |
СO2 |
|
|
G |
|
O2 |
|
, |
(2.8) |
|
|
|
|
||||
СО2 |
|
MO2 |
|
|
|
|
|
|
|
|
|
||
26

где GCO2 |
количество образующегося СО2, кг/ч; MCO2 |
молекуляр- |
||||||||||||||||||||
ная масса СО2; MO2 |
молекулярная масса О2. |
|
|
|
|
|
|
|
||||||||||||||
Количество образующейся воды |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
0,65 G// |
M |
H2O |
|
|
|
|
|
|
|
|
||||
|
|
|
G |
Н2О |
|
|
|
O2 |
|
, |
|
|
|
|
(2.9) |
|||||||
|
|
|
MO2 |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
где MH2O – молекулярная масса Н2О. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Количество гудрона, пошедшее на образование СО2 |
и Н2О, кг/ч, |
|||||||||||||||||||||
[13] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
G = (G |
|
|
– 0,3 G// |
|
) + (G |
|
– 0,65· G// |
), |
(2.10) |
||||||||||||
|
|
|
CO2 |
|
|
O2 |
|
|
H2O |
|
O2 |
|
|
|
||||||||
что составляет (G/Gf) ·100 % масс. от сырья. |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Д |
|
|
|
Таблица 2.5 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Физико-химические характеристики некоторых веществ |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
А |
|
ИТемпература |
|
Критическое |
|
||||||||
Соедине- |
Молекуляр- |
Плотность |
Температура |
|
критическая |
|
давление Р, |
|
||||||||||||||
|
|
|
|
|
20 |
|
3 |
|
|
|
|
о |
|
|
|
|||||||
ние |
ная масса |
|
ρ4 |
|
, кг/м |
кипения, |
С |
|
|
К, оС |
|
|
|
МПа |
|
|||||||
Н2 |
2,016 |
|
|
|
|
б |
-252,8 |
|
|
|
|
33,3 |
|
|
|
1,294 |
|
|||||
|
|
|
0,09 |
|
|
|
|
|
|
|
|
|
|
|||||||||
N2 |
28,0 |
|
|
|
1,25 |
|
|
-195,8 |
|
|
|
|
126,3 |
|
|
|
3,398 |
|
||||
СО |
С |
1,25 |
|
|
-191,58 |
|
|
|
132,9 |
|
|
|
3,489 |
|
||||||||
28,0 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
и |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
СО2 |
44,0 |
1,96 |
|
|
-78,5 |
|
|
|
|
304,3 |
|
|
|
7,381 |
|
|||||||
Н2S |
34,1 |
|
|
|
2,56 |
|
|
|
-60,3 |
|
|
|
|
373,6 |
|
|
|
9,007 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
О2 |
32,0 |
|
|
|
1,43 |
|
|
|
-18 |
|
|
|
|
154,8 |
|
|
|
5,08 |
|
|||
SО2 |
64,0 |
|
|
|
2,86 |
|
|
|
-10 |
|
|
|
|
430,6 |
|
|
|
7,893 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Н2О |
18,0 |
|
|
|
1000 |
|
|
|
100 |
|
|
|
|
647,4 |
|
|
|
22,12 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Черный |
180 |
|
|
|
758 |
|
|
|
250 |
|
|
|
|
681,4 |
|
|
|
1,66 |
|
|||
соляр 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Черный |
210 |
|
|
|
794 |
|
|
|
560 |
|
|
|
|
721,8 |
|
|
|
1,54 |
|
|||
соляр 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
27
Количество углеводородных газов и паров соляра в отходящих газах процесса окисления зависит от температуры окисления, содержания легких фракций в сырье, расхода воздуха. Количество углеводородных газов, образующихся в процессе окисления, кг/ч, принимают равным 1–2 % масс., что составит
Gу.г = К1· Gf /100, |
(2.11) |
где К1 – объём углеводородных газов, % масс.
Расчет жидких продуктов в составе отгона, кг/ч, производится с учётом соблюдения материального баланса:
Gж = К2· Gf /100, |
(2.12) |
где К2 – объём отгона, % масс.
Физико-химические характеристики некоторых веществ
приведены в табл. 2.5 [13].
2.4. Тепловой баланс окислительнойИколонны
Цель расчета теплового баланса колонны – определение избыточного тепла, которое необходимо отводить циркуляционным
орошением или подбором необходимой температуры ввода сырья в |
|||
колонну. |
|
Д |
|
А |
|
||
Приход тепла: |
|
||
|
|
||
1. Тепло с сырьем, кДж/ч, определяется по формуле [18] |
|
||
|
Qс = Gf t · cг, |
(2.13) |
|
|
б |
|
|
где сг теплоёмкость гудрона, кДж/(кг К), на входе в колонну сг = 2,0 |
||
кДж/(кг К); t температураисырья на входе в колонну, С. |
|
|
С |
|
|
2. Тепло, выделяющееся при окислении гудрона, кДж/ч, |
|
|
|
Qр = I · Gf , |
(2.14) |
где I – энтальпия окисления гудрона, кДж/кг. |
|
|
Энтальпия окисления гудрона определяется по рис. 2.3, с учётом температуры размягчения получаемого битума и температуры процесса окисления.
3. Тепло с воздухом на окисление
Qвозд = Gвозд · свозд · tвозд, |
|
(2.15) |
где tвозд температура воздуха, идущего на окисление, |
С; |
свозд |
теплоемкость воздуха при tвозд , кДж/(кг К), свозд=1,023 кДж/(кг К) при
tвозд=50 С.
Всего приход тепла, кДж/ч,
28
Qприход = Qс + Qр + Qвозд . |
(2.16) |
Расход тепла: |
|
1. Тепло с битумом, кДж/ч, [17] |
|
Qб= Gб · t · cб, |
(2.17) |
где сб теплоемкость битума, кДж/(кг К), cб =2,1; t |
температура |
|||||||
процесса окисления, С. |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
гудрона, |
|
|
|
|
|
|
|
|
окисления |
кДж/кг |
|
|
|
|
И |
|
|
Энтальпия |
|
|
|
|
|
|
|
|
|
|
|
|
Д |
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
А |
|
|
|
|
|
|
|
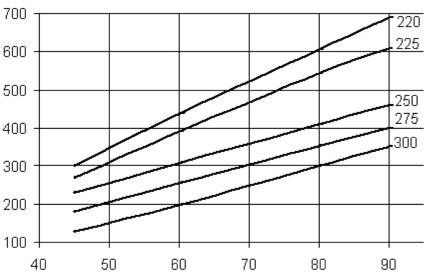
Температура размягчения, С |
|
|||
|
|
|
|
б |
|
|
|
|
|
|
Рис. 2.4. Зависимость теплового эффекта окисления гудрона от |
||||||
|
|
|
и |
|
|
|
|
|
|
|
достигаемой температуры размягчения битума при различной |
||||||
|
|
температуре ок слен я гудрона: 220, 225, 250, 275, 300 С |
||||||
|
|
|
С |
|
|
|
|
|
|
2. Тепло, уходящее с газами окисления и с отгоном, [13] |
|||||||
|
|
|
|
|
Qг.о = ΣGi с i t, |
(2.18) |
||
где Gi количество отдельных составляющих газов окисления, кг/ч;
сi теплоемкость отдельных составляющих газов |
окисления, |
|
кДж/(кг К), сi=1,26; |
t температура процесса окисления, С; |
|
или по формуле [13] |
Qг.о = ΣGi Ii, |
(2.19) |
|
||
где Ii – энтальпия отдельных составляющих газов окисления, кДж/кг.
Энтальпия составляющих вычисляется |
по формуле |
|
Ii = (а + b t) |
t. |
(2.20) |
где а, b коэффициенты, значения которых приведены в табл. 2.6. Энтальпия углеводородов (отгона) Iув, кДж/кг, определяется при
температуре верха колонны и плотности отгона по следующим уравнениям:
29

– энтальпия жидких нефтепродуктов, кДж/кг,
I |
|
|
1,689 t 0,0017 t2 |
|
|||
ж |
|
|
|
|
, |
(2.21) |
|
|
|
|
|
||||
0,9943 420 |
|
||||||
|
|
|
0,00915 |
|
|||
где ρ420 – плотность жидкости при температуре 20 С, отнесенная к плотности воды при 4 С; t – температура, при которой определяется энтальпия, С;
– для углеводородных газов и паров при невысоких давлениях
Iп = (210 + 0,457 t + 0,000584 t2) (4,013 – ρ4) –309. (2.22)
Потери тепла в окружающую среду Qпот |
принимаются в |
|
количестве 5–10 % от количества тепла, приходящего в колонну: |
||
Qпот= S (tc t0), |
И |
(2.23) |
где коэффициент теплоотдачи, кДж/(м2 ч К), можно принять =25
кДж/(м2 ч К); S теплопередающая поверхность, м2; tc температура
|
|
|
|
|
Д |
|
|
|
на наружней оболочке, С; t0 температура окружающей среды, С. |
||||||||
|
|
|
|
|
|
|
Таблица 2.6 |
|
|
Коэффициенты для расчета энтальпии составляющих газов окисления |
|||||||
|
Вещество |
|
|
а |
|
в ·10-4 |
|
|
|
|
|
|
|
|
|
|
|
|
Кислород |
|
б |
0,909 |
|
1,5 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Азот |
|
и |
А1,014 |
|
1,21 |
|
|
|
|
|
|
|
||||
|
Углекислый газ |
|
|
0,845 |
|
3,93 |
|
|
|
|
|
|
|
|
|
|
|
|
Водяной пар |
|
|
|
1,944 |
|
1,00 |
|
|
|
|
|
|
|
|||
|
Всего расход тепла составляет, кДж/кг, |
|
|
|||||
|
|
СQрас |
= Qб + Qг.о + Qпот. |
(2.24) |
||||
Определение температуры сырья на входе в колонну
Температура сырья на входе в колонну вычисляется, исходя из равенства прихода и расхода тепла, то есть по формуле Qприх=Qрас, или
. |
(Gf t c) + Qр = Qб +Qг.о+ (0,05 0,1) (Gf t c) +Qр. (2.25) |
Если имеет место избыток тепла (Qизб = Qприх–Qрас), то его можно снять разными способами:
30