Материал: 2254
Следует помнить, что сумма в процентах всех составляющих газа должна быть равна 100%.
Для определения плотности упругих паров нефтепродукта у вос-
пользуемся формулой Клапейрона – Менделеева, которая устанавливает связь между абсолютным давлением Р, Н/м2 (Па), абсолютной температурой Т, К, объемом V, м3, массой газа m, кг, и газовой постоянной R, Дж/(кг∙К):
P V m R T . |
(3.6) |
|
Теплота сгорания различных газов |
Таблица 3.1 |
|||
|
|
||||
|
|
|
|
|
|
Газ |
Обозначение |
Плотность |
Теплота сгорания |
||
|
|
|
паров, кг/м3 |
МДж/м3 |
МДж/кг |
Метан |
СН4 |
0,71 |
35,8 |
50,0 |
|
Этан |
С2 Н6 |
1,32 |
63,8 |
48,0 |
|
Пропан |
С3 |
Н8 |
1,85 |
85,5 |
46,0 |
Бутан |
С4 |
Н10 |
2,45 |
111.6 |
45,4 |
Этилен |
С2 Н4 |
1,25 |
63,8 |
51,0 |
|
Бензол |
С6 Н6 |
3,48 |
140,0 |
40,2 |
|
Пентан |
С5 Н12 |
3,21 |
146,0 |
45,4 |
|
Сероводород |
Н2 S |
1,5 |
23,4 |
15,5 |
|
Окись |
СО |
1,26 |
12,6 |
10,0 |
|
углерода |
|
|
|
|
|
Водород |
Н2 |
0,086 |
10,8 |
125,0 |
|
Один кмоль паров нефтепродукта занимает объем V 22,4 м3. Для кмоля объёмом 22,4 м3 уравнение состояния газа примет вид
PV m |
8314 |
T ; |
P |
|
m |
|
8314 |
T |
или |
P у |
8314 |
T . |
|
|
|
||||||||||||
|
|
|
|
||||||||||
|
|
|
V |
|
|
|
|
|
|||||
|
|
|
|
|
|||||||||
Откуда |
|
|
|
у |
|
P |
, |
(3.7) |
|||||
|
|
|
8314 T |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
где – молекулярная (молярная) масса нефтепродукта, кг/кмоль; 8314 Дж/(кмоль∙К) – универсальная газовая постоянная.
~16 ~
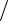
Для примерного определения плотности нефтепродукта для давления и температуры (Р = 736 мм рт. ст. = 0,98 ∙ 105 Н/м2 и Т = 293 К), который находится в газовом состоянии, используется выражение
у |
22,4. |
(3.8) |
Например, молекулярная |
(молярная) |
масса метана СН4 равна |
16 кг/кмоль. Если данный газ сосредоточить при атмосферных условиях в объеме 22,4 м3, то его плотность будет равна 0,714 кг/м3. Зная плотность газа, можно удельную теплоту сгорания в МДж/м3 перевести в МДж/кг.
В жидкой фазе плотность метана равна 424 кг/м3. Объём метана в жидком состоянии занимает в 600 раз меньше, чем объём в газовой фазе. Это является важным фактором при транспортировке метана и использовании его в качестве топлива.
По ГОСТ Р 52087 – 2003. Газы углеводородные сжиженные топливные, согласно техническим условиям, на автомобилях применяют в качестве топлива пропан автомобильный (ПА), 85±10% пропана, остальное бутан (для зимних условий), пропан-бутан автомобильный (ПБА),
50±10% пропана, остальное бутан.
Втабл. 3.2 дан состав автомобильных газовых топлив ПА и ПБА.
|
|
Таблица 3.2 |
Характеристики сжиженных газов |
||
|
|
|
Содержание газов, % |
ПА (зимний) |
ПБА |
Пропан |
90 |
40 |
Бутан |
5 |
55 |
Метан, этан, этилен |
5 (3; 1; 1) |
5 (3; 1; 1) |
3.3. Экспериментальное определение теплоты сгорания топлив
Сущность калориметрического экспериментального метода определе-
ния теплотворной способности топлива с использованием бомбы заключается в сжигании навески топлива определенной массы (примерно 1 г) в адиабатическом режиме в среде сжатого кислорода.
Калориметрическая бомба помещается в калориметрический сосуд объёмом 2000 – 2500 см3, заполненный водой. Теплота, выделяющаяся при
~17 ~

сгорании топлива, поглощается водой. Для выравнивания температуры внутри сосуда предусматривается вертикальная мешалка, которая приводится в действие от электродвигателя. Температура воды в сосуде измеряется термометром или другим точным прибором. На рис. 3.1 показана схема установки для определения теплотворной способности топлива.
Рис. 3.1. Схема установки для определения теплотворной способности топлива
Калориметрическая бомба представляет собой стальной стакан ёмкостью 300 см3 (рис. 3.2). На стакан плотно навинчивается крышка. В крышке имеется отверстие с запорным краном для подвода кислорода под давлением 2 МПа.
Рис. 3.2. Калориметрическая бомба в разобранном виде
~18 ~
Вкрышке прибора установлены два электрода. Один электрод выполнен из платины и соединен с массой. На нём есть устройство типа петли, в которую устанавливается тигель (горшочек). Тигель служит для помещения спрессованного брикета твердого топлива массой около 1 г или налива жидкого топлива примерно той же массы. Другой электрод изолирован от массы. К двум электродам подведено напряжение 12 В. Между электродами установлена запальная проволочка, которая должна касаться поверхности топлива. При подаче напряжения и под действием тока проволочка нагревавается, сгорает и воспламеняет твердое или жидкое топливо.
Впроцессе сгорания топлива выделяется теплота. Вода массой 2 кг нагревается и перемешивается с целью обеспечения в объёме одинаковой температуры. Зная массу, теплоёмкость воды и изменение температуры при сгорании топлива, можно найти его теплотворную способность.
На практике для каждой калориметрической бомбы определяется её энергетический эквивалент W путем сжигания высокочистой бензойной кристаллической кислоты (БК), которая является эталонным топливом. Теплота сгорания Q БК равна 26 434 кДж/кг. Химическая формула данной кислоты С7Н6О2, она белого цвета с хорошей воспламеняемостью.
Численное значение энергетического эквивалента W определяют из выражения
W = m1∙ Q БК / T1, |
(3.9) |
где m1 – масса БК, обычно равная 1,0 г (0,001 кг); T1 – повышение температуры воды в опыте с БК (разность между наибольшим показанием термометра и температурой, при которой началось сжигание топлива, например 5,3 оС).
Для калориметрической бомбы с приведенными выше данными
величина W будет равна 5 кДж / оС. |
|
Если известно численное значение энергетического |
эквивалента |
W калориметрической бомбы, то для любого вида топлива (например, |
|
жидкого) высшую теплоту сгорания можно определить из выражения |
|
Qтоп = W ∙ T2 / m2, |
(3.10) |
где m2 – масса жидкого топлива, равная 0,8 г (0,0008 кг); T1 – повышение температуры воды в опыте с исследуемым топливом, например 7 оС. Величина Qтоп с учетом формулы (3.10) будет равна
~19 ~

Qтоп = 5 ∙103 ∙ 7 / 0,0008 = 43 750 000 Дж /кг.
Для более точного определения теплотворной способности данного топлива необходимо отнять от Qтоп теплоту сгорания запальной проволочки. Теплота сгорания стальной проволочки равна 6690 кДж/кг. При массе стальной проволочки 1 г теплота её сгорания составит
6,69 кДж/кг.
Для определения теплоты сгорания топлив применяют современные приборы с использованием персональных компьютеров и другой техники. На рис. 3.3 представлена установка для определения теплоты сгорания топлив. Калориметр В-08 МА-К служит для автоматического определения энергии сгорания жидких, газообразных и твердых топлив. Конструкция калориметрических бомб практически не изменилась.
Рис. 3.3. Калориметр В-08 МА - К
Контрольные вопросы и задания
1.Чем отличаются высшая и низшая теплотворные способности топлив?
2.Что представляет собой процесс сгорания топлив?
3.Запишите конечные уравнения процесса сгорания углерода и водорода.
4.Запишите уравнения для определения низшей теплотворной способности бензина и газа, состоящего из 50% пропана и бутана.
5.Как определяется плотность упругих паров нефтепродукта, находящегося в газовом состоянии?
6.Поясните методику экспериментального определения теплоты сгорания топлив.
~20 ~