Материал: 1968
Окисление – это реакция взаимодействия молекул углеводородного топлива с молекулами кислорода. Если температура воздуха достигает требуемого значения, то окисление переходит в процесс горения.
В жидком топливе имеют место легкие, средние и тяжелые молекулы.
В процессе распыливания топлива легкие фракции уже являются газифи- |
|
цированными и в окружении кислорода воздуха под действием темпера- |
|
С |
|
туры электрической искры (10 000 0С) воспламеняются, образуя началь- |
|
ную зону пламени (бензиновые двигатели). Далее действует принцип цеп- |
|
ной реакц |
. У д зеля топливо должно самостоятельно воспламеняться |
при нагреве его в к слороде воздуха до температуры самовоспламенения |
|
циальных |
|
250 – 300 |
0 . Для надежного пуска и работы дизеля температура в конце |
такта сжат я должна быть не менее 500 – 600 0С. |
|
Теплота сгоран я может ыть определена сжиганием топлива в спе- |
|
|
пр борах, которые называют калориметрами (1 кал = 4,187 Дж), |
а также подсч тана по формулам, если известен состав топлива. |
|
В табл. 1.1 представлены удельные значения теплоты сгорания раз- |
|
личных газовых топл в для 1 м3 и 1 кг при атмосферных условиях |
|
(Р = 736 мм рт. ст. = 0,98 ∙ 105 Н/м2 и Т = 293 К). |
|
1.3. Расчетное определение теплоты сгорания топлив |
|
В расчетных формулах наи олее распространенной является форму- |
|||
ла Д.И. Менделеева, основанная на том, что общая теплота сгорания рав- |
|||
|
Дж |
|
|
на сумме теплоты, полученной от сгорания отдельных элементов, вхо- |
|||
дящих в составбАтоплива. Эта формула для жидких топлив имеет вид [1, 2] |
|||
Qи = [34 С + 125,6 Н – 10,9 (О – S) – 2,5 (9Н + W)] 106 /кг , |
(1.2) |
||
|
И |
||
где С, Н, О, S, W – содержание в рабочей массе топлива углерода, водо- |
|||
рода, кислорода, серы, влаги в процентах (по массе). При изучении топ- |
|||
лив и их состава различают рабочую и сухую (без влаги) массу. Общая |
|||
масса всех составляющих топлива должна быть равна 100%. |
|
||
Например, для бензина |
марки Аи-98 и наличии |
С = 0,85 |
(85%), |
Н = 0,15 (15%), но без присутствия кислорода, серы, |
влаги величина |
||
низшей теплотворности равна |
|
|
|
Qи = [34∙ 0,85 + 125,6∙ 0,15 – 2,5∙ (9∙ 0,15) ] ∙ 106 = |
(1.3) |
||
= (28,9 + 18,84 - 3,37) ∙10 6 |
= 44,37 ∙106 Дж/кг = 44,37 МДж/кг. |
||
6

Для природного газа, содержащего 95% метана СН4 и 5% пропана С3 Н8, низшая теплотворность равна
|
Qи = [35,8∙ 0,95 + 85,5∙ |
0,05 ] ∙ 106 =38,28 106 |
Дж / м3. |
(1.4) |
||||||
|
Для газа произвольного состава теплоту сгорания расчетным путем |
|||||||||
С |
|
|
|
|
|
|
|
|
||
можно определить по формуле, используя данные табл. 1.1 [3], |
|
|
||||||||
|
Q = [35,8∙ СН4 + 10,8 Н2 + 12,6 СО +63,8 С2 Н6 +111,6 С3 Н8 + |
|
|
|||||||
|
|
|
+146 С5 Н12 +23,4 Н2 S] |
∙ 106 Дж/м3. |
|
|
(1.5) |
|||
|
и |
3 |
3 |
|
|
|
|
|||
|
ледует помн ть, что сумма |
в процентах всех составляющих газа |
||||||||
должна быть равна 100%. |
|
|
|
Таблица 1.1 |
||||||
|
Бутан ОбозначенС4 Н10 2,45 |
111.6 |
45,4 |
|
|
|||||
|
|
|
Теплота сгорания различных газов |
|
|
|
|
|||
|
Газ |
|
|
Плотность |
Теплота сгорания |
|
|
|||
|
|
|
|
паров, кг/м |
МДж/м |
|
МДж/кг |
|
||
|
Метан |
|
СН4 |
|
0,71 |
35,8 |
|
50,0 |
|
|
|
Этан |
С2 Н6 |
А |
|
48,0 |
|
|
|||
|
|
1,32 |
63,8 |
|
|
|
||||
|
Пропан |
С3 Н8 |
|
1,85 |
85,5 |
|
46,0 |
|
|
|
|
Этилен |
С2 Н4 |
|
1,25 |
63,8 |
|
51,0 |
|
|
|
|
Бензол |
С6 Н6 |
|
3,48 |
140,0 |
|
40,2 |
|
|
|
|
Пентан |
С5 Н12 |
|
Д |
45,4 |
|
|
|||
|
|
3,21 |
146,0 |
|
|
|
||||
|
Сероводород |
Н2 S |
|
1,5 |
23,4 |
|
15,5 |
|
|
|
|
Окись угле- |
|
СО |
|
1,26 |
12,6 |
|
10,0 |
|
|
|
рода |
|
|
|
|
|
|
|
|
|
|
Водород |
|
Н2 |
|
0,086 |
10,8 |
|
125,0 |
|
|
пользуемся формулой Клапейрона – Менделеева, которая устанавливает связь между абсолютным давлением Р, Н/м2 (Па), абсолютной температу-
рой Т, К, объемом V, м3, массой газа m, кг, и газовой постоянной
R, Дж/(кг∙К):
Для определения плотности упругих паровИнефтепродукта у вос-
P V m R T . |
|
(1.6) |
Один кмоль паров нефтепродукта занимает объем V |
22,4 |
м3. Для |
кмоля объёмом 22,4 м3 уравнение состояния газа имеет вид
7
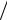
PV m |
8314 |
T ; |
P |
m |
|
8314 |
T , |
или |
|
P у |
8314 |
T . |
|
|
|||||||||||
|
|
|
|
|||||||||
|
|
V |
|
|
|
|
|
|
||||
|
|
P |
|
|
||||||||
|
|
|
Откуда |
|
у |
, |
(1.7) |
|||||
|
|
|
|
8314 T |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
где – молекулярная (молярная) масса нефтепродукта, кг/кмоль; 8314 Дж/(кмоль∙К) – универсальная газовая постоянная.
Для пр мерного нахождения плотности нефтепродукта (Р = 736 мм
рт. ст. = |
0,98 ∙ 105 Н/м2 Т = 293 К), который находится в газовом со- |
|||
стоянии, |
спользуется выражение |
|
||
С |
у 22,4. |
(1.8) |
||
|
|
|||
Напр мер, |
молекулярная (молярная) масса |
метана СН4 равна |
||
16 кг/кмоль. |
данный газ сосредоточить при атмосферных условиях в |
|||
объемеЕсли22,4 м3, то его плотность удет равна 0,714 кг/м3. Зная плотность газа, можно удельную теплоту сгорания в МДж/м3 перевести в МДж/кг.
В ж дкой фазе плотность метана равна 424 кг/м3. Объём метана в жидком состоянии занимает в 600 раз меньше, чем объём в газовой фазе. Это является важным фактором при транспортировке метана и использовании его в качестве топлива.
По ГОСТ Р 52087–2003 «Газы углеводородные сжиженные топлив-
|
|
Д |
||
ные» на автомобилях применяют в качестве топлива пропан автомобиль- |
||||
ный (ПА), 85±10%бАпропана, остальное бутан (для зимних условий), про- |
||||
пан – бутан автомобильный (ПБА), 50 ±10% пропана, остальное бутан. |
||||
|
В табл. 1.2 дан состав автомобильных газовых топлив ПА и ПБА. |
|||
|
|
|
Таблица 1.2 |
|
|
Характеристики сжиженных газов |
|||
|
|
|
|
|
|
Содержание газов, % |
ПА (зимний) |
ПБА |
|
|
Пропан |
90 |
40 |
|
|
Бутан |
5 |
55 |
|
|
|
|
И |
|
|
Метан, этан, этилен |
5 (3; 1; 1) |
5 (3; 1; 1) |
|
1.4. Экспериментальное определение теплоты сгорания топлив
Сущность калориметрического экспериментального метода определения теплотворной способности топлива с использованием бомбы за-
8

ключается в сжигании навески топлива определенной массы (примерно 1 г) в адиабатическом режиме в среде сжатого кислорода.
Калориметрическая бомба помещается в калориметрический сосуд объёмом 2000 – 2500 см3, заполненный водой. Теплота, выделяющаяся при сгорании топлива, поглощается водой. Для выравнивания температу-
ры внутри сосуда предусматривается вертикальная мешалка, которая при- Сводится в действие от электродвигателя. Температура воды в сосуде измеряется термометром или другим точным прибором. На рис. 1.1 показана схема установки для определения теплотворной способности топлива.
и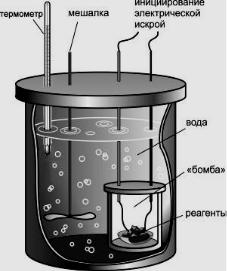
КалориметрическаябАбомба представляет собой стальной стакан ёмкостью 300 см3 (рис. 1.2). На стакан плотно навинчивается крышка. В крышке имеется отверстие с запорным краном для подвода кислорода под
Рис. 1.1. Схема установки для определения теплотворной способности топлива
Д давлением 2 МПа. И
Рис. 1.2. Калориметрическая бомба в разобранном виде
9
В крышке установлены два электрода. Один электрод платиновый
соединен с массой. На нём есть устройство типа петли, в которую |
уста- |
|
навливается тигель (горшочек). Тигель служит для помещения |
спрес- |
|
сованного брикета твердого топлива массой около 1 г или налива жидкого |
||
топлива примерно той же массы. Другой электрод изолирован от массы. |
||
К двум электродам |
подведено напряжение 12 В. Между электродами |
|
С |
|
|
установлена запальная проволочка, которая должна касаться поверхно- |
||
сти топлива. При подаче напряжения и под действием тока проволочка |
||
нагревается, сгорает |
воспламеняет твердое или жидкое топливо. |
|
В процессе сгоран я топлива выделяется теплота. Вода массой 2 кг
температуры. Зная массу топлива, теплоёмкость воды и изменение тем-
нагреваетсяприперемеш вается с целью обеспечения в объёме одинаковой
пературы сгоран топлива, определяют его теплоту сгорания.
На практ ке для каждой калориметрической бомбы определяется её энергетическ й экв валент W путем сжигания высокочистой бензойной кристалл ческой к слоты (БК), которая является эталонным топливом. Теплота сгоран я Q БК равна 26 434 кДж/кг. Химическая формула данной
кислоты С7Н6О2, она |
елого цвета с хорошей воспламеняемостью. |
||
Численное значен |
е энергетического эквивалента W равно |
||
бW = m1∙ Q БК / T1, |
(1.9) |
||
где m1 – масса БК, о ычно равная |
1,0 г (0,001 кг); T1 – повышение тем- |
||
|
|
Д |
|
пературы воды в опыте с БК (разность между |
наибольшим показанием |
||
термометра и температуройА, при которой началось сжигание топлива, на- |
|||
пример, 5,3 0С). |
|
|
|
Для калориметрической бомбы с приведенными выше данными вели- |
|||
чина W будет равна 5 кДж / 0С. |
И |
||
Если известно численное значение энергетического эквивалента |
|||
W калориметрической бомбы, то для любого |
вида топлива (например, |
||
жидкого) высшую теплоту сгорания можно определить из выражения |
|||
|
Qтоп = |
W ∙ T2 / m2, |
(1.10) |
где m2 – масса жидкого топлива, равная 0,8 г (0,0008 кг); T1 – повышение температуры воды в опыте с исследуемым топливом (например, 7 0С). Величина Qтоп с учетом формулы (1.10) будет равна
Qтоп = 5 ∙103 ∙7 / 0,0008 = 43 750 000 Дж /кг.
10