Материал: 105-109
Гликозилирование гидроксилизина происходит в коллагене, ещё не претерпевшем
спирализации, и завершается после образования тройной спирали.
Число углеводных единиц в молекуле коллагена зависит от вида ткани:
В коллагене сухожилий (тип I) их 6,
В коллагене капсулы хрусталика (тип IV) – НО).
Роль этих углеводных групп неясна; но при наследственном заболевании,
причиной которого является дефицит лизилгидроксилазы (синдром Элерса-Данло-Русакова, тип VI), содержание гидроксилизина и углеводов в коллагене снижено.
3. Образование проколлагена, его секреция в межклет. Пространство
После гидроксилирования и гликозилирования просвете ЭР каждая про-α-цепь
соединяется водородными связями с двумя другими про-α-цепями, образуя тройную спираль проколлагена. Из ЭР молекулы проколлагена перемещаются в аппарат Гольджи, включаются в секреторные пузырьки и секретируются в межклеточное пространство.
Образование тропоколлагена: в межклет. матриксе концевые пропептиды
коллагенов I, II и III типов отщепляются специфическими проколлагенпептидазами, в результате чего обр. молекулы тропоколлагена, кот. е и явл. структурной ед. коллагеновых фибрилл.
При снижении активности этих ферментов (с. Элерса-Данло-Русакова, тип VII)
концевые пропептиды проколлагена не отщепляются, вследствие чего нарушается образование тропоколлагена и далее нарушается образование нормальных коллагеновых фибрилл. Нити коллагена видны под микроскопом в виде дезорганизованных пучков. Клинически это проявляется малым ростом, искривлением позвоночника, привычными вывихами суставов, высокой растяжимостью кожи.
У коллагенов некоторых типов (IV, VIII, X) концевые пропептиды не отщепляются.
Это связано с тем, что такие коллагены образуют не фибриллы, а сетеподобные структуры, в формировании которых важную роль играют концевые N- и С-пептиды.
Вопрос 108 Строение и функции гликозаминогликанов (гиалуроновой кислоты, хондроитинсульфатов, гепарина). Структура протеогликанов.
Гликозаминогликаны – линейные отрицательно заряженные гетерополисахариды.
Протеогликаны – высокомолекулярные соединения, состоящие из белка (5-10%) и гликозаминогликанов (90-95%). Они образуют основное вещество межклеточного матрикса соединительной ткани.
Функции протеогликанов и гликозаминогликанов в организме:
Явл. структурными компонентами межклеточного матрикса
Специфически взаимодействуют с коллагеном, эластином, фибронектином,
ламинином и другими белками межклет. матрикса;
Все протеогликаны и гликозаминогликаны, являясь полианионами, могут
присоединять, кроме воды, большие кол-ва катионов (Na+, K+, Са2+) и т.о. участвовать в формировании тургора различных тканей
Они играют роль молекулярного сита в межклет. матриксе, препятствуют
распространению патогенных микроорганизмов;
Гиалуроновая кислота и протеогликаны выполняют амортизирующую функцию
в суставных хрящах
Гепарансульфатсодержащие протеогликаны способствуют созданию
фильтрационного барьера в почках
Кератансульфаты и дерматансульфаты обеспечивают прозрачность роговицы
Гепарин – антикоагулянт
Гепарансульфаты – компоненты плазматических мембран клеток, где они могут
функционировать как рецепторы и участвовать в клеточной адгезии и межклеточных взаимодействиях. Они также выступают компонентами синаптических пузырьков.
СТРОЕНИЕ И КЛАССЫ ГЛИКОЗАМИНОГЛИКАНОВ: они представляют
собой длинные неразветвлённые цепи гетерополисахаридов, кот. построены из повторяющихся дисахаридных единиц (2 мономеров):
Гексуроновая кислота (D-глюкуроновая кислота или L-идуроновая)
Производное аминосахара (глюкоз- или галактозамина).
NH2-rpyппa аминосахаров обычно ацетилирована, что приводит к исчезновению присущего им положительного заряда. Кроме гиалуроновой кислоты, все гликозаминогликаны содержат сульфатные группы в виде О-эфиров или N-сульфата.
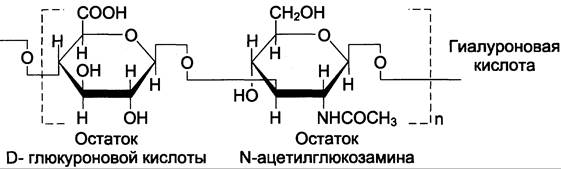
Гиалуроновая кислота находится во многих органах и тканях.
В хряще она связана с белком и участвует в образовании протеогликановых агрегатов, в некот. органах (стекловидное тело глаза, пупочный канатик, суставная жидкость) встречается и в свободном виде. В суставной жидкости гиалуроновая кислота выполняет роль смазочного вещества, уменьшая трение между суставными поверхностями.
Гиалуроновая кислота содержит несколько тысяч дисахаридных единиц
Хондроитинсульфаты – самые распространённые гликозаминогликаны в
организме человека; содержатся в хряще, коже, сухожилиях, связках, артериях, роговице глаза. Явл. важным составным компонентом агрекана – основного протеогликана хрящевого матрикса.
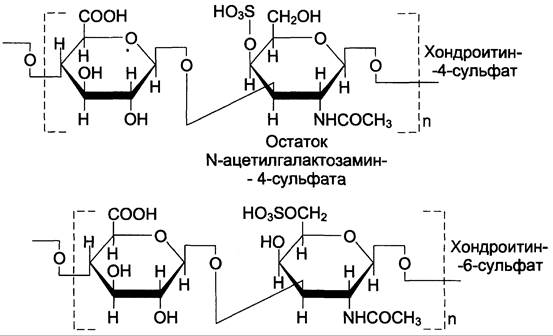
В организме человека встречаются 2 вида хондроитинсульфатов, кот. построены одинак. образом, но отл. положением сульфатной гр. в молекуле N-ацетилгалактозамина.
Хондроитин-4-сульфат
Хондроитин-6-сульфат
Одна полисахаридная цепь хондроитинсульфата содержит около 40 повторяющихся дисахаридных единиц
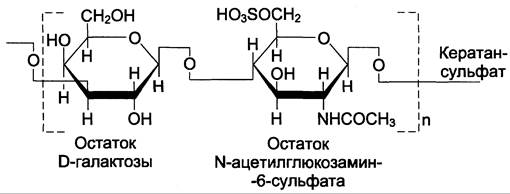
Кератансульфаты – наиболее гетерогенные гликозаминогликаны; отличаются друг от друга по суммарному содержанию углеводов и распределению в разных тканях.
Кератансульфат I находится в роговице глаза и содержит кроме повторяющейся
дисахаридной единицы L-фукозу, D-маннозу и сиаловую кислоту.
Кератансульфат II находится в хрящевой ткани, костях, межпозвоночных дисках.
В его состав помимо сахаров дисахаридной единицы входят N-ацетилгалактозамин,
L-фукоза, D-манноза и сиаловая кислота. Он входит в состав агрекана и некот. малых протеогликанов хрящевого матрикса
В отл. от других гликозаминогликанов, кератансульфаты вместо гексуроновой
кислоты содержат остаток галактозы.
Дерматансульфат характерен для кожи, кровеносных сосудов, сердечных
клапанов. В составе малых протеогликанов (бигликана и декорина) дерматансульфат содержится в межклеточном веществе хрящей, межпозвоночных дисков, менисков
Гепарин – компонент противосвёртывающей системы крови (его применяют как
антикоагулянт при лечении тромбозов). Синтезируется тучными клетками и находится в гранулах внутри этих клеток. Наибольшие количества гепарина обнаруживаются в лёгких, печени и коже.
Гепарансульфат входит в состав протеогликанов базальных мембран и является
постоянным компонентом клеточной поверхности.
Структура дисахаридной единицы гепарансульфата и гепарина одинаковая.
Отличие этих гликозаминогликанов заключается в том, что в гепарине больше
N-сульфатных групп, а в гепарансульфате больше N-ацетильных групп.
CТРОЕНИЕ И ВИДЫ ПРОТЕОГЛИКАНОВ: в межклеточном матриксе
присутствуют очень крупные (агрекан и версикан) и малые протеогликаны
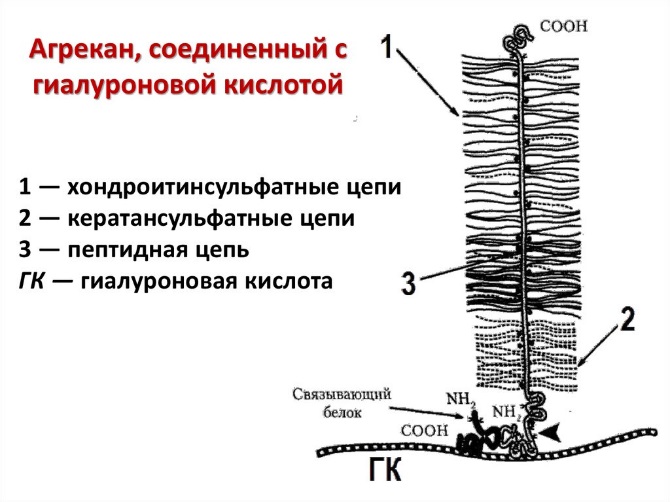
Агрекан – протеогликан хрящевого матрикса, очень большая молекула, в которойк
одной ППЦ присоединены до 100 цепей хондроитинсульфатов и 30 цепей кератансульфатов. По форме молекула агрекана напоминает бутылочный "ёршик".
В хрящевой ткани молекулы агрекана собираются в агрегаты с гиалуроновой
кислотой и связывающим белком, кот. присоединяются к агрекану нековалентными связями в области домена G1.
Домен G1 взаимодействует с 5 дисахаридными единицами гиалуроновой кислоты,
далее этот комплекс стабилизируется связывающим белком; домен G1 и связывающий белок вместе занимают 25 дисахаридных единиц гиалуроновой кислоты.
Конечный агрегат состоит из 1 молекулы гиалуроновой к-ты и 100 молекул
агрекана (и такого же кол-тва связывающего белка). Процесс агрегации полностью завершается в межклет. матриксе.
Гиалуроновая кислота образуется на поверхности хондроцитов специфической
синтетазой и "выталкивается" в межклеточное пространство, чтобы связаться с агреканом и связывающим белком.
Малые протеогликаны – протеогликаны с низкой молекул. массой (декорин,
бигликан, фибромодулин, люмикан, перлекан), содержатся в хрящах, сухожилиях, связках, менисках, коже и других видах соединительной ткани.
Они имеют небольшой коровый белок, к которому присоединены одна или две
цепи гликозаминогликанов. Коровые белки бигликана и декорина похожи по размерам и структуре. Они имеют несколько тандемных повторов, богатых лейцином, которые образуют α-спирали или β-структуры. На N- и С-концах этих белков имеются домены, содержащие S-S-связи.
Коровые белки значительно различаются по первичной структуре в N-концевых
областях, что определяет различия в присоединении гликозаминогликанов.
Бигликан содержит серин в положениях 5 и 11 => присоед. 2 полисахар. цепей.
Декорин содержит один серии в положении 4 => присоед. 1 полисахаридная цепь.
Фибромодклин имеет области тандемных повторов, богатые лейцином, но его
N-концевая область не содержит серина, а имеет несколько сульфатированных остатков тирозина, поэтому 1 или 2 цепи кератансульфата присоединяются к коровому белку фибромодулина в области, богатой лейцином, через NH2-группу аспарагина.
Малые протеогликаны могут связываться с другими компонентами соединит.
ткани и оказывать влияние на их строение и функции:
Декорин и фибромодулин присоединяются к фибриллам коллагена II типа и
ограничивают их диаметр (т.е. препятствуют образованию толстых фибрилл).
Декорин и бигликан, присоединяясь к фибронектину, подавляют клеточную
адгезию, а присоединяясь к фактору роста опухолей (3, снижают его митогенную активность.
Участвуют в процессах развития и восстановления соединительной ткани.
Протеогликаны базальных мембран отличаются гетерогенностью.
Это преимущественно гепарансульфатсодержащие протеогликаны (ГСПГ), представленные 2 видами: высокой и низкой плотности
Вопрос 109 Структурная организация межклеточного матрикса. Адгезивные белки межклеточного матрикса: фибронектин и ламинин, их строение и функции
По функции белки межклет. матрикса можно разделить на:
1. Aдгезивные белки – белки с выраженными адгезивными свойствами
2. Белки, подавляющие адгезию клеток
Адгезивные белки:
Фибронектин – неколлагеновый структурный гликопротеин, синтезируемый и
выделяемый в межклеточное пространство многими клетками. Построен из двух идентичных ППЦ, соединённых дисульфидными мостиками у своих С-концов.
ППЦ содержит 7-8 доменов, на каждом из которых расположены специфические
центры для связывания коллагена, протеогликанов, гиалуроновой к-ты, углеводов плазматических мембран, гепарина, фермента трансглутаминазы. Может способствовать адгезии клеток.
Существует несколько форм фибронектина:
Растворимый, или плазменный, фибронектин синтезируется гепатоцитами
Нерастворимый, или тканевый фибронектин синтезируется фибробластами или
эндотелиоцитами, глиоцитами и эпителиальными клетками.
Обе формы способствуют адгезии и распространению эпителиальных и
мезенхимальных клеток, стимулируют пролиферацию и миграцию эмбриональных и опухолевых клеток, контролируют дифференцировку и поддержание цитоскелета клеток, активно участвуют в воспалительных и репаративных процессах.
Каждая субъединица фибронектина содержит последовательность Арг-Гли-Асп
(RGD), с помощью которой он может присоединяться к клеточным рецепторам (интегринам). Эти рецепторы опосредованно взаимодействуют с актиновыми микрофиламентами, которые находятся в цитозоле. В этом процессе участвуют так называемые белки прикрепления: талин, винкулин, α-актинин. С помощью таких белок-белковых взаимодействий информация может передаваться из межклеточного матрикса внутрь клетки, а также в обратном. Фибронектин участвует в миграции клеток.
Ламинин – наиболее распространённый неколлагеновый гликопротеин базальных
мембран. Состоит из трёх ППЦ: А, В1 и В2, имеет крестообразную форму с 3 одноцепочечными ветвями и одной трёхцепочечной ветвью
Каждая цепь ламинина содержит несколько глобулярных и стержневидных
доменов, на которых имеются специфические центры связывания для различных веществ.
Ламинин взаимодействует со всеми структурными компонентами базальных
мембран, включая коллаген IV типа, нидоген, фибронектин, ГСПГ. Молекула ламинина имеет несколько центров связывания с клетками.
Главные функции ламинина определяются его способностью связывать клетки и
модулировать клеточное поведение. Он может влиять на рост, морфологию, дифференцировку и подвижность клеток. Ламинин выполняет роль адгезивного белка для различных эпителиальных и мезенхимальных клеток.
Нидоген – сульфатированный гликопротеин базальных мембран, образует с
ламинином плотный, нековалентно связанный комплекс. Состоит из одной ППЦ, содержащей три глобулярных домена. Один из доменов нидогена имеет центр связывания ламинина, в области другого домена находится центр связывания коллагена IV типа.
Нидоген может выступать в качестве одного из связывающих мостов между
различными компонентами межклет. матрикса и участвовать в образовании тройных комплексов ламинин-нидоген-коллаген.